Introducción
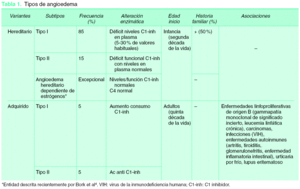
El déficit del inhibidor de la esterasa de la fracción de complemento C1 se caracteriza por la aparición de edema subcutáneo y submucoso en cualquier parte de la superficie cutánea y del tracto respiratorio y/o gastrointestinal. La incidencia se estima entre 1/10.000 y 1/50.000 habitantes1, sin diferencias de raza2. Este síndrome se ha asociado en un 24 % de los adultos y en un 14 % de los pacientes de más de 10 años de edad con atopia, bien con antecedentes familiares o personales3. Existen principalmente dos tipos de déficit de C1 inhibidor (C1-inh): hereditario (autosómico dominante) y adquirido, cuyas principales características se recogen en la tabla 1. Bork et al4 describieron en el año 2000 un tercer tipo dentro del angioedema hereditario, con características clínicas idénticas a los dos tipos descritos previamente, dependiente de estrógenos, sólo en mujeres y relacionado en la mayor parte de los casos con el embarazo o con terapias hormonales. Posiblemente se encuentre ligado al cromosoma X, ya que esta patología sólo se ha observado en mujeres.
El C1-inh es una enzima que se caracteriza por ser el principal regulador de los pasos de la activación temprana de la vía clásica del complemento y de la activación de kalicreína, de la plasmina en el sistema fibrinolítico, de la activación del factor XI en la cascada de la coagulación y del factor XIIa. En ausencia de C1-inh, la vía clásica del complemento puede ser activada de forma no apropiada o excesiva. El resultado es un aumento de la permeabilidad vascular y un edema masivo local incontrolado2, causantes de la sintomatología propia de este síndrome. Los niveles de evidencia utilizados a lo largo de este artículo se encuentran recogidos en la tabla 2.
Diagnóstico
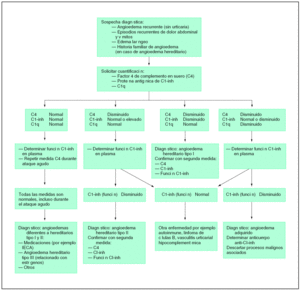
Los dos tipos principales de angioedema (hereditario y adquirido) se manejan de forma similar. En la figura 1 se expone un algoritmo diagnóstico del déficit de C1-inh.
Figura 1. Algoritmo diagnóstico del déficit de C1-inhibidor. Modificada de Bowen T, et al1. IECA: inhibidores de la enzima conversora de angiotensina.
Clínico
1.Angioedema recurrente (tumefacción) sin urticaria que habitualmente no es pruriginoso. Un eritema prodrómico (eritema marginado) se ha descrito en un 25 % de los casos, que puede ser confundido con una urticaria5,6. El angioedema no suele ser doloroso, a menos que afecte a zonas de presión o donde el tejido celular subcutáneo es limitado.
2.La tumefacción puede afectar a las extremidades, la cara, el tronco, el tracto gastrointestinal, la región genitourinaria o las vías respiratorias superiores, pero en general a cualquier parte del cuerpo.
3.Los síntomas abdominales pueden simular cólicos de la infancia, apendicitis aguda o abdomen agudo, y estos síntomas incluyen náuseas, vómitos, dolor abdominal y diarrea tras el episodio agudo.
4.Los síntomas respiratorios incluyen alteraciones de la voz y disfagia, al poder afectar tanto a la lengua como a la faringe y laringe.
5.Raramente puede cursar con edema cerebral, pleural o síntomas sugestivos de afectación vesical.
6.La edad de aparición es variable, y el paciente puede comenzar con los síntomas antes del año de edad, principalmente con cólicos y raramente tumefacción (los ataques empeoran con la pubertad). Los episodios laríngeos suelen iniciarse más tarde que otros síntomas, pero podrían iniciarse en la infancia.
7.El ataque agudo de angioedema se ha relacionado con múltiples desencadenantes, que habitualmente no se identifican (tabla 3).
8.Los ataques agudos tienden a ser prolongados y normalmente aumentan en intensidad durante las primeras 24 horas y posteriormente van disminuyendo durante las 48-72 horas siguientes. Algunos ataques pueden durar más de 72 horas, ya que la tumefacción va migrando de un sitio a otro.
9.Los ataques suelen ser periódicos y normalmente se continúan después de varias semanas de remisión. No suelen ocurrir diariamente.
Laboratorio
1.Las pruebas de laboratorio deberían ser realizadas en un laboratorio acreditado con un esquema que asegure la calidad apropiada. Las determinaciones deberían realizarse sin tratamiento, e idealmente con al menos 7 días de diferencia desde el último brote.
2.La determinación de la proteína C4 en suero es un buen método de cribaje para la determinación del déficit de C1-inh, ya que se encuentra disminuida en pacientes no tratados (C4 < 30 % de valores medios habituales)14. Si la determinación de C4 fuera normal, habitualmente no sería necesario proceder a determinar los valores de C1-inh, ya que aunque los valores de C1-inh estuvieran disminuidos habría que cuestionar el diagnóstico (nivel de evidencia 4). Se ha visto que la combinación de un valor de C4 disminuido y una disminución de la función de C1-inh tiene un 98 % de especificidad y un 96 % de valor predictivo negativo para el déficit de C1-inh15.
3.La baja prevalencia de esta enfermedad nos indica que los falsos positivos son frecuentes14. Las determinaciones obtenidas antes del año de edad pueden no ser fiables, ya que existe una alta prevalencia de falsos positivos y negativos. En este caso, se deberían repetir las determinaciones después del año de edad16.
4.Una vez establecido el diagnóstico, la determinación de los niveles de C4 y niveles y función de C1-inh serían útiles para monitorizar la respuesta al tratamiento.
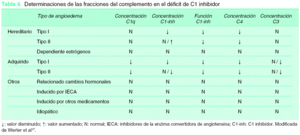
5.La determinación de la proteína antigénica C1q podría ser de valor para diagnosticar el angioedema hereditario, ya que está normalmente disminuido en estos casos y es normal en caso de angioedema adquirido. Las diferentes determinaciones de los valores de complemento para los distintos tipos de angioedema se encuentran recogidas en la tabla 4.
6.En el estudio genético, de forma similar a otros cuadros con herencia autosómica dominante, se pueden observar mutaciones de novo en un 25-33 % de los pacientes. El estudio genético no es necesario para confirmar el diagnóstico.
7.En el caso del angioedema hereditario se aconseja el estudio familiar, ya que es importante la detección de los niños asintomáticos.
En el año 2004 se establecieron los criterios diagnósticos del déficit de C1-inh durante el Third C1 Esterase Inhibitor Deficiency Workshop (tabla 5).
Terapéutico
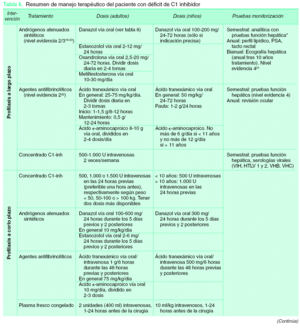
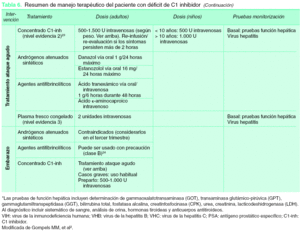
En primer lugar la prevención primaria consistiría en evitar en la medida de lo posible los factores desencadenantes de un ataque agudo de angioedema. De forma general, el manejo del paciente con déficit de C1-inh debe incluir profilaxis a largo y a corto plazo y tratamiento del ataque agudo (tabla 6). Es una entidad a tener en cuenta, ya que sin tratamiento puede alcanzar una mortalidad de hasta un 30-40 % en la mayor parte de los casos por obstrucción de la vía aérea25. Los efectos secundarios de los diferentes medicamentos están reflejados en la tabla 7.
Profilaxis a largo plazo
Indicaciones:
1.Más de un episodio severo al mes o más de 5 días discapacitado para funciones habituales en un mes.
2.Más de un episodio de dolor abdominal severo en un año.
3.Algún episodio de angioedema en la cabeza o el cuello.
4.Episodios frecuentes de angioedema periférico o genital.
5.Requerimiento de más de un concentrado de C1-inh al año.
Los andrógenos atenuados son considerados como de primera elección, ya que en general presentan mayor efectividad que el resto de tratamientos. En caso de falta de eficacia o efectos secundarios de éstos, se deben utilizar los agentes antifibrinolíticos, y en último lugar los concentrados de C1-inh. En el caso del angioedema adquirido, el uso de antifibrinolíticos ha demostrado mayor eficacia que el resto de tratamientos disponibles (nivel evidencia 2)26. Los agentes antifibrinolíticos están contraindicados en caso de enfermedad tromboembólica activa.
En el caso de los pacientes infantiles se deben considerar de primera elección los agentes antifibrinolíticos, por el menor número y severidad de efectos secundarios. En caso de no funcionar éstos, de segunda elección es el concentrado C1-inh, y en caso de no funcionamiento de ninguno de ellos, el uso de antiandrógenos, el cual está especialmente indicado si existe más de un ataque abdominal al mes, aunque deben utilizarse con precaución por sus potenciales efectos en el crecimiento.
Se puede realizar combinación de diferentes tratamientos (por ejemplo agentes fibrinolíticos con andrógenos sintéticos atenuados) y es aconsejable el uso de la dosis mínima eficaz.
No está clara la eficacia de los andrógenos atenuados en el tratamiento del angioedema adquirido tipo II, ni tampoco lo está la eficacia de los fármacos antifibrinolíticos ni de los andrógenos atenuados en el angioedema hereditario dependiente de estrógenos, aunque al menos un paciente perteneciente a este último grupo ha respondido a danazol27.
En el caso de utilizar danazol como profilaxis existen dos pautas internacionalmente aceptadas para su uso a largo plazo (tabla 8).
Se recomienda la vacunación para el virus de la hepatitis B a todos los pacientes que estén recibiendo derivados sanguíneos de forma habitual (concentrados de C1-inh y plasma fresco congelado).
Profilaxis a corto plazo
Indicaciones de la profilaxis a corto plazo:
1.Manipulación dental.
2.Cirugía oral.
3.Intubación.
4.Otras manipulaciones, principalmente de zonas donde habitualmente se manifiesta clínicamente el angioedema.
En este caso es considerado como de primera elección el uso de concentrado de C1-inh, y en caso de no disponer del mismo se podrían utilizar bien andrógenos atenuados, bien agentes antifibrinolíticos.
En caso de procedimientos menores (por ejemplo manipulación dental) y si está disponible el concentrado de C1-inh, existe la posibilidad de no hacer nada y sólo utilizar el medicamento en caso de un ataque agudo. En caso de no estar disponible el concentrado de C1-inh se debe hacer profilaxis previa con andrógenos atenuados o con agentes antifibrinolíticos. Está aceptado el uso de plasma fresco congelado, pero siempre considerando la posibilidad de transmisión de enfermedades víricas. En el caso de manejo dental hay que tener precaución, ya que se pueden dar ataques durante las 36 horas siguientes al procedimiento.
En caso de procedimientos mayores o intubación se debe hacer profilaxis desde el inicio, bien con andrógenos atenuados o agentes antifibrinolíticos (si hay tiempo suficiente) o bien con concentrado de C1-inh (si está disponible). Si no se dan ninguna de estas dos circunstancias se debería hacer profilaxis con plasma fresco congelado.
Tratamiento ataque agudo
No siempre es necesario el tratamiento del ataque agudo. En ocasiones, si el cuadro no es generalizado, la mejor opción es esperar a la resolución espontánea del angioedema o sólo proceder a la reposición de fluidos.
Se debería ofrecer a todos los pacientes la oportunidad de tener en casa C1-inh, en dosis suficiente para tratar una emergencia laríngea, ya que en un 50-75 % de los casos presentan un brote que amenaza su vida. El producto debe ser reconstituido a temperatura ambiente antes de su administración, no se debe agitar y se debe administrar en una vena periférica durante 10 minutos aproximadamente.
En el caso del plasma fresco congelado puede empeorar los síntomas durante la fase aguda. Se debe tener en cuenta la posible transmisión, cada vez menos frecuente, de enfermedades como el virus de la hepatitis B, hepatitis C, etc.
No existe evidencia de la efectividad de la adrenalina28, pero es relativamente eficaz comparada con otros tratamientos (corticosteriodes29 y antihistamínicos).
En el caso de un ataque agudo se debe añadir al tratamiento habitual los analgésicos apropiados para el alivio del dolor, si éste está presente (antiinflamatorios no esteroideos [AINE] para el dolor abdominal).
En caso de que el paciente estuviera en tratamiento previamente con danazol y tuviera un episodio agudo, se puede doblar la dosis durante varios días.
Es importante el mantenimiento de la vía aérea. Si se produjese edema laríngeo severo podría ser necesaria la práctica de una traqueotomía.
Nombres comerciales de los diferentes fármacos empleados
Danazol: Danatrol® cápsulas 50, 100 y 200 mg (Sanofi-Winthrop Pharmaceuticals, Nueva York, EE. UU.).
Estanozolol: Winstrol® 2 mg y depot 1 ml 50 mg (Zambon, Vicenza, Italia).
Oxandrolona: Oxandrin® (Savient Pharmaceuticals, Nueva Jersey, EE. UU.).
Metiltestosterona: Longivol oral® grageas 1, 5, 10 y 25 mg (Medical S. A., España).
Ácido tranexámico: Amchafibrin® comprimidos 500 mg o ampollas 500 mg (Fides Rottapharm, Valencia, España).
Ácido ε-aminocaproico: Caproamin Fides® sobres 2,5 g o ampollas 4 g (Fides Rottapharm, Valencia, España).
Concentrado C1-inhibidor: Berinert® viales 500 U (Immuno AG, Viena, Austria). No comercializado en España (solicitar como medicación extranjera).
Nuevos tratamientos
Inhibidor de la kalicreína plasmática DX88 (Dyax Corp., Cambridge, Massachussets, EE. UU.).
Inhibidor del receptor de la bradiquinina B2 Icatibant (Jerini AG, Berlín, Alemania)30.
Inhibidor de las proteasas séricas. No es específico, ya que inhibe antitrombina III, beta2-microglobulina, alfa1-antitripsina y alfa2- antiplasmina, entre otras.
C1-inh recombinante (Pharming Group NV, Leiden, Países Bajos)31.
Conclusiones
El déficit de C1-inh es un síndrome poco frecuente, pero que es conveniente conocerlo debido a su potencial afectación de las vías aéreas superiores, que pueden provocar la muerte del paciente. El tipo de angioedema por déficit de C1-inh más frecuente es el congénito, que habitualmente se manifiesta en la segunda década de vida con sintomatología abdominal. El tipo adquirido es menos frecuente y puede estar desencadenado por diversos fármacos o cambios hormonales. El diagnóstico de esta enfermedad comienza con la sospecha clínica (tumefacción cutánea con ocasional afectación de vías respiratorias superiores y/o abdomen). La sospecha clínica se debe confirmar con la determinación de C4 y la cuantificación de C1-inh en plasma y, si procede, la determinación de la función de C1-inh. El diagnóstico no siempre es fácil, ya que son frecuentes los falsos positivos y existe mucha variabilidad entre los diferentes laboratorios. En cuanto al tratamiento existen diversos fármacos habitualmente utilizados para el manejo del ataque agudo y otros novedosos que todavía no están en el mercado. La realización de profilaxis tiene unas indicaciones precisas que es aconsejable seguir.
Conflicto de intereses
Declaramos no tener ningún conflicto de intereses.
Correspondencia:
Javier Pedraz Muñoz.
Servicio de Dermatología.
Hospital Universitario de la Princesa.
C/ Diego de León, 62. 28006 Madrid. España.
Correo electrónico: javierpedraz@aedv.es
Aceptado el 15 de enero de 2007.