Es sabido que la cirugía micrográfica de Mohs (CMM) es un procedimiento economizador de tiempo y recursos. Por tanto, siempre son bienvenidos los métodos que optimicen el flujo de trabajo de la CMM.
En esta comunicación breve, nuestro objetivo es compartir nuestro modo de realizar el procesamiento de la CMM mediante inclusión en agua del grifo y tinción de azul de metileno (azul M). Hasta donde sabemos, no se ha reportado nunca la inclusión en agua del grifo y la tinción de azul M para el procesamiento de la CMM. Sin embargo, estas técnicas han sido utilizadas históricamente para la evaluación patológica intraoperatoria de otras muestras quirúrgicas1,2. Por tanto, la aplicación de este método de procesamiento de la CMM es como una «vuelta a los principios» de la patología intraoperatoria. La idoneidad de este procesamiento viene respaldada por los datos de 261 casos consecutivos de CMM recopilados en una base de datos prospectiva de febrero de 2022 a agosto de 2024.
La inclusión estándar con el compuesto de temperatura de corte óptima (OCT) implica el uso de dispositivos y moldes de inclusión, así como laminillas y un nivel de burbuja o un extractor de calor. El motivo de utilizar la OCT es lograr la temperatura óptima de corte de manera rápida, para evitar los bien conocidos artefactos de congelación. Sin embargo, según nuestra experiencia, el agua del grifo no genera más artefactos de congelación que la OCT, con tiempos de congelación más rápidos.
Nuestro procesamiento de la CMM sigue los pasos siguientes: 1) tras realizar las extirpaciones quirúrgicas, se procesan las muestras de CMM siguiendo una técnica estándar; 2) se prepara en el criostato un soporte para tejidos (seta) con una capa de agua del grifo congelada (es decir, una cama de hielo) a fin de disponer de una superficie lisa donde sujetar y colocar las secciones planas; 3) se retira la seta del criostato y se coloca la sección de la CMM en él; 4) se añaden gotas de agua del grifo alrededor de la sección para completar la inclusión; 5) seguidamente se vuelve a colocar la seta en el criostato y se aplica el extractor de calor; 6) transcurridos de 10 a 15s, la sección está lista para ser recortada y cortada. El recorte es normalmente reducido, ya que no existe capa de OCT ni otro medio de inclusión que eliminar. El técnico de Mohs sitúa capas progresivas en una laminilla, asegurándose de incluir la sección completa. Por último, se tiñen las láminas con azul M conforme al protocolo ultrarrápido siguiente: 5s de inmersión en azul M (Kühne's Methylene Blue Phenicated solution, QCA, Amposta, España) y 5s de lavado en agua del grifo. Seguidamente se secan las láminas con papel y se entregan al patólogo y al cirujano de Mohs para su evaluación. Para acelerar aún más el procesamiento, no se aplican cubreobjetos ni se necesitan medios de montaje. Estos se aplicarán más tarde, cuando las láminas estén listas para ser escaneadas (Aperio GT450, Leica, Wetzlar, Alemania). Los pasos de este procesamiento de la CMM y algunos trucos de ejecución se muestran en el Anexo Vídeo 1. La calidad de las láminas obtenidas con nuestro método se muestra en las figuras 1 y 2 y en el Anexo Vídeo 1.
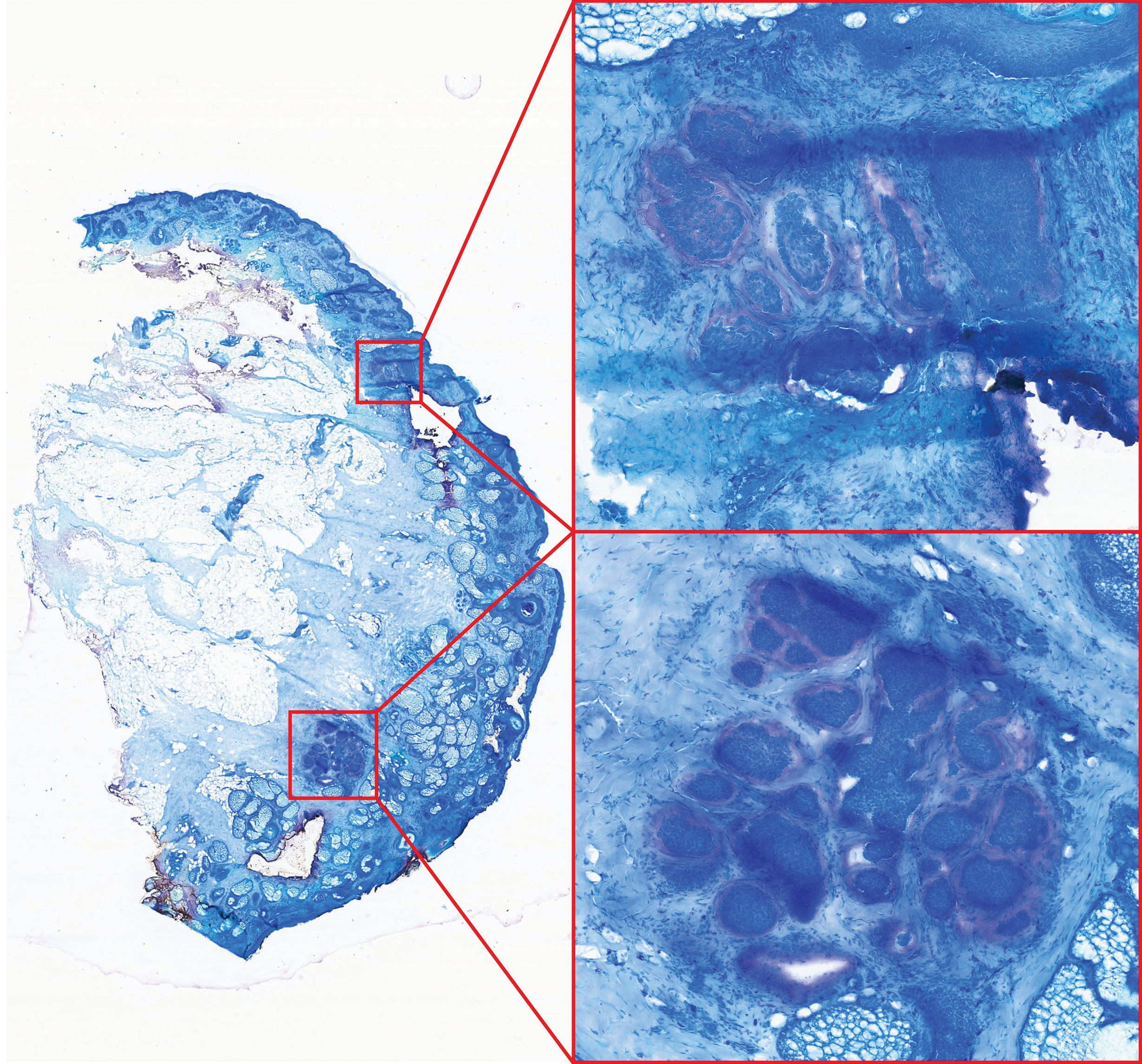
La metacromasia es visible como halo violeta que rodea 2 focos (263nm/píxel, superior ×7, inferior ×10) de un carcinoma basocelular nodular en esta capa final de una muestra de cirugía micrográfica de Mohs en 2 secciones (263nm/píxel, ×1,08). La calidad de la lámina es buena, y presenta tejido adiposo.
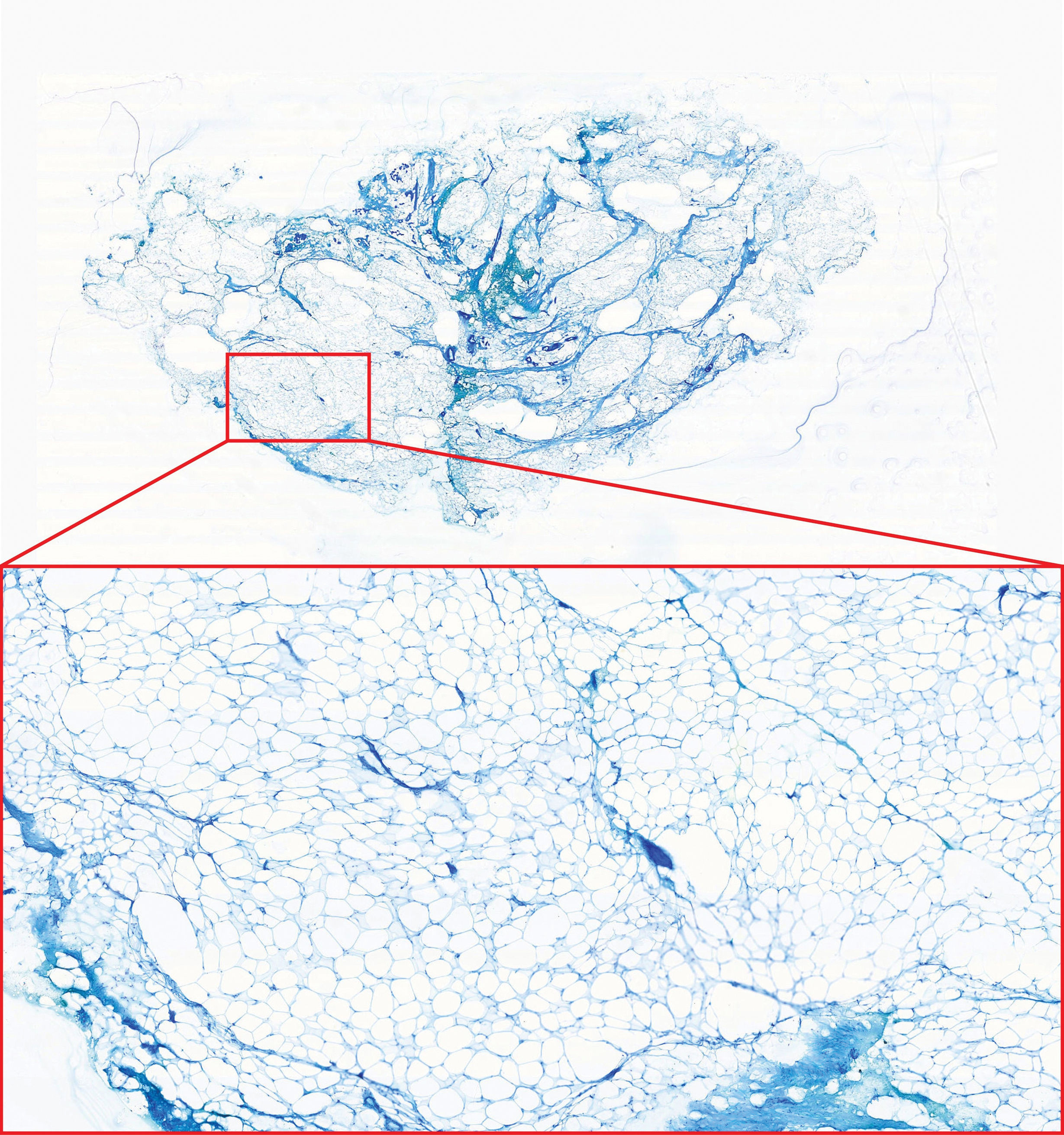
Utilizar la inclusión en agua del grifo puede ser un motivo de duda para algunos lectores. También dudaba el autor principal (RM) cuando empezó a realizar CMM tras su fellowship. Sin embargo, transcurridos más de 2 años, coincidimos en que la inclusión en agua del grifo no afecta negativamente a la calidad de las láminas. De hecho, parece ser muy útil para realizar el corte a través del tejido adiposo, un problema conocido de la CMM3. Por tanto, la inclusión en agua del grifo mantiene la calidad de la sección de piel congelada, a la vez que mejora la calidad de la grasa, sin necesidad de realizar una congelación adicional con un pulverizador de hielo o nitrógeno líquido (figs. 1 y 2). Además, reduce el tiempo de recorte dado que ninguna capa del medio de inclusión cubre la superficie de la muestra. Por último, el uso de agua del grifo en lugar del OCT reduce el coste del procesamiento de la CMM.
Un inconveniente de la inclusión en agua del grifo puede ser la dificultad para mantener aplanada la sección de CMM una vez volteada sobre la seta, dado que no estará «flotando» en el OCT. De hecho, el borde epidérmico puede caer bajo el plano horizontal de la sección, especialmente si se corta una sección única de CMM. Sin embargo, los bordes epidérmicos pueden ser elevados (Anexo Vídeo 1). La comparación entre la inclusión en agua del grifo y OCT se muestra en la tabla 1.
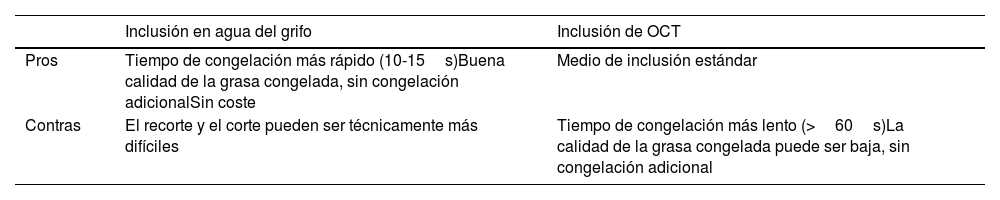
Comparación entre la inclusión de agua del grifo y temperatura óptima de corte
| Inclusión en agua del grifo | Inclusión de OCT | |
|---|---|---|
| Pros | Tiempo de congelación más rápido (10-15s)Buena calidad de la grasa congelada, sin congelación adicionalSin coste | Medio de inclusión estándar |
| Contras | El recorte y el corte pueden ser técnicamente más difíciles | Tiempo de congelación más lento (>60s)La calidad de la grasa congelada puede ser baja, sin congelación adicional |
El uso de tinción de azul M puede ser menos sorprendente. La tinción de azul M es prácticamente idéntica a la tinción de azul de toluidina (azul T). El azul T es muy conocido en la literatura para realzar la visualización de los cánceres de piel tratados normalmente mediante CMM. Este realce es debido a un fenómeno denominado metacromasia, donde la tinción de azul T del estroma de mucopolisacáridos que rodea a las células tumorales vira a rosa o magenta4. El azul M muestra el mismo fenómeno metacromático que el azul T (fig. 1 y Anexo Vídeo 1), pero no ha sido reportado nunca como tinción de las capas de CMM. No existen ventajas ni inconvenientes claros asociados al uso de azul M en lugar de azul T. Se trata solo de una cuestión de preferencia, coste y disponibilidad. De manera destacada, nuestro protocolo de 10s de tinción con azul M es más rápido que los protocolos de azul T previamente descritos4,5.
Aunque no se han observados recidivas de los cánceres de piel tratados mediante este procesamiento de la CMM, el tiempo de seguimiento de 2,5 años es muy corto para extraer conclusiones sobre las tasas de recaída.
En conclusión, reportamos nuestra manera de realizar el procesamiento de la CMM, ilustrando 2 aspectos noveles: la inclusión en agua del grifo y la tinción ultrarrápida con azul M. Estos 2 nuevos aspectos aceleraron el procesamiento de la CMM sin afectar aparentemente a la calidad de las láminas y los resultados clínicos. La revisión de las láminas sin medios de montaje ni cubreobjetos acelera aún más el proceso, lo cual es especialmente importante cuando se requieren múltiples secciones. Son necesarios seguimientos más prolongados y estudios comparativos para confirmar nuestra experiencia.
Conflicto de interesesLos autores declaran la ausencia de conflicto de intereses.