Los procedimientos vasculares invasivos son en el momento actual ampliamente utilizados para el diagnóstico y tratamiento de muchas patologías del sistema cardiovascular, con un buen perfil de seguridad y eficacia, aunque entrañan potenciales complicaciones que ocasionalmente pueden comprometer la vida del paciente. Presentamos un nuevo caso de pseudoaneurisma infeccioso postangioplastia complicado con embolismos sépticos cutáneos. Se trata de una entidad infrecuente caracterizada por bacteriemia persistente, sepsis sin foco aparente y embolismos sépticos regionales. El análisis histopatológico de las lesiones cutáneas habitualmente permite evidenciar la presencia de cocobacilos Gram positivos y de vasculitis séptica. Es una entidad con una importante morbimortalidad, por lo que el diagnóstico precoz resulta esencial. Por ello, ante lesiones cutáneas tras procedimientos vasculares invasivos deben considerarse en el diagnóstico diferencial no solo los embolismos de colesterol, sino también los embolismos sépticos.
Invasive vascular procedures have good efficacy and safety profiles and are now widely used for the diagnosis and treatment of many cardiovascular disorders. However, they do have potential complications that can occasionally be life-threatening. We present a new case of infectious pseudoaneurysm following percutaneous transluminal coronary angioplasty and complicated by septic emboli to the skin. It is a rare condition characterized by persistent bacteremia, sepsis of unknown origin, and regional septic emboli. Histopathology of the skin lesions typically reveals gram-positive coccobacilli and septic vasculitis. The condition carries a significant morbidity and mortality, making early diagnosis essential. Both cholesterol and septic emboli should be considered in the differential diagnosis of skin lesions after invasive vascular procedures.
La angioplastia es un procedimiento vascular invasivo ampliamente utilizado como técnica de revascularización por su seguridad y eficacia1. No obstante, no está exenta de complicaciones, entre ellas las sépticas, que son relativamente infrecuentes presentándose en menos del 1% de estos procedimientos2,3. Entre las complicaciones infecciosas las más habituales son las bacteriemias postangioplastia y las infecciones locales en el lugar de acceso, siendo excepcionales la endocarditis y la endarteritis séptica postangioplastia4. Presentamos un caso de embolismos sépticos cutáneos secundarios a un pseudoaneurisma infeccioso postangioplastia. Se trata de una entidad infrecuente, aunque con una presentación clínica e histopatológica característica5.
Caso clínicoUn varón de 70 años con antecedentes de diabetes mellitus tratada con insulina, hipertensión arterial, cardiopatía isquémica, cáncer renal y vesical intervenidos en 2005, sin evidencia de recidiva local ni metastásica, ingresó en nuestro hospital por reagudización de su insuficiencia renal crónica y dolor asociado a impotencia funcional aguda en el miembro inferior derecho, tres días después de haber sido sometido a una revascularización coronaria de la arteria descendente anterior mediante angioplastia e implantación de stent farmacoactivo a través de la arteria femoral derecha. En su anterior ingreso también se revascularizó la arteria coronaria derecha, accediendo por la misma arteria con un intervalo de 6 días entre ambos procedimientos.
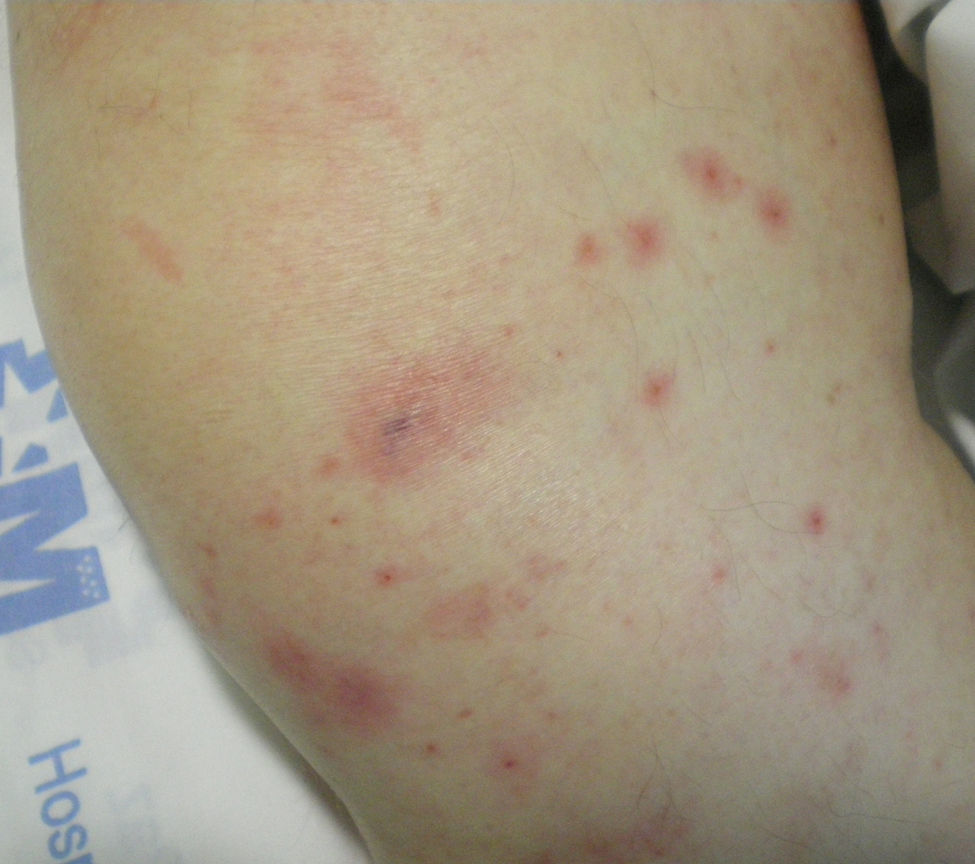
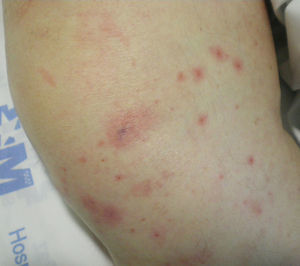
Desde su ingreso el paciente estaba febril (temperatura de 39°C) e hipotenso (90/60mmHg). En la exploración física se evidenció un aumento de diámetro asociado a una pérdida de fuerza muscular en el miembro inferior derecho, junto con una masa no pulsátil en la región inguinal derecha compatible con un hematoma postangioplastia. Exclusivamente en dicha extremidad se constató la presencia de placas redondeadas y ovaladas de diferentes tamaños que oscilaban entre uno y tres centímetros de diámetro aproximadamente, eritematoedematosas de centro purpúrico y bordes mal definidos, siendo más numerosas en la porción acra del mismo y con cierta tendencia a la agrupación (fig. 1), sin otros hallazgos significativos.
En la analítica destacaba una anemización aguda (hemoglobina: 9g/dl; normal: 13-17,3g/dl), un aumento de la creatinina plasmática (4,24mg/dl; basal: 2,3mg/dl; normal: 0,60-1,30mg/dl), neutrofilia del 90% sin leucocitosis (normal: 41-74%) y una proteína C reactiva elevada de 150mg/l (normal: 0-5,00mg/l). Se realizó de forma aguda y diferida una TC cerebral, una ecografía doppler arterial del miembro inferior derecho y una TC abdominopélvica que resultaron rigurosamente normales. En el fondo de ojo no se objetivaron signos retinianos de embolismos de colesterol.
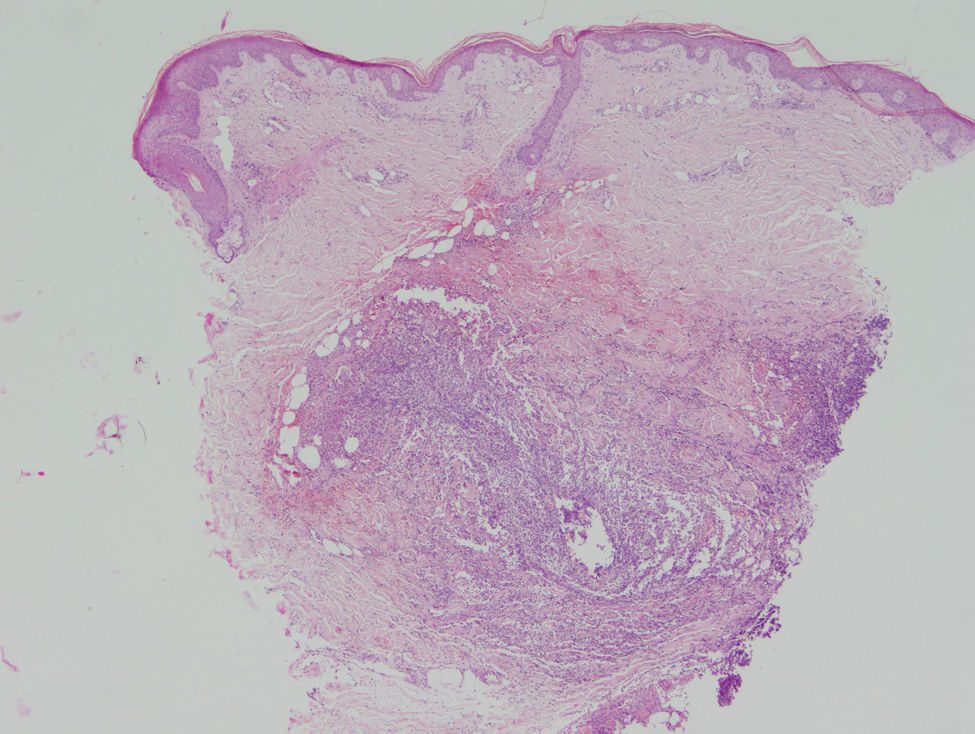
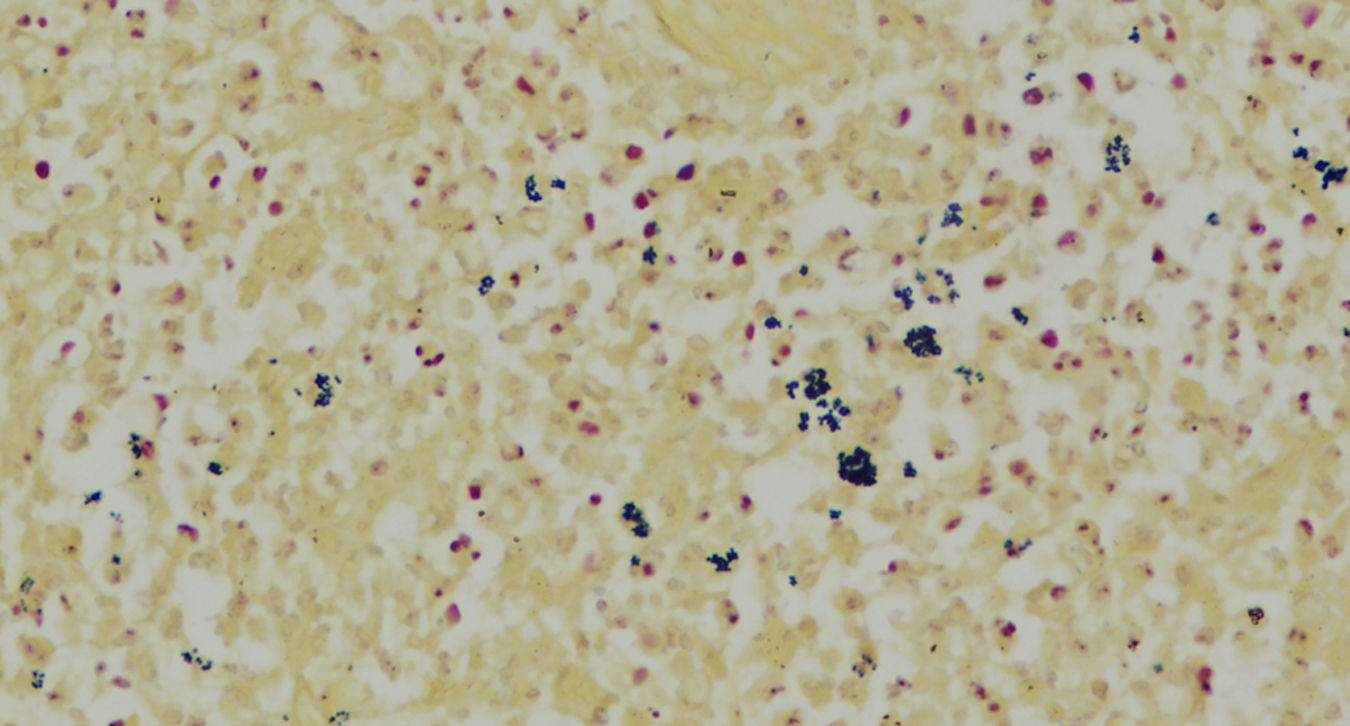
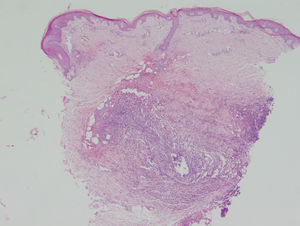
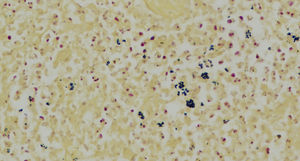
El estudio histopatológico de las lesiones dermatológicas permitió evidenciar una epidermis normal y densos infiltrados inflamatorios neutrofílicos multicéntricos con hematíes extravasados, tanto en la dermis media como profunda (fig. 2). Los vasos mostraban un endotelio prominente, trombos intraluminales y neutrófilos intraluminales, intraparietales e intersticiales. Se realizó una tinción de Gram que reveló la existencia de cocobacilos Gram positivos aislados, en parejas y arracimados en las zonas correspondientes a los densos infiltrados inflamatorios de neutrófilos (fig. 3). Todos los cultivos resultaron estériles excepto los hemocultivos y el cultivo de piel en los que se aisló un Staphylococcus aureus meticilín sensible (SAMS).
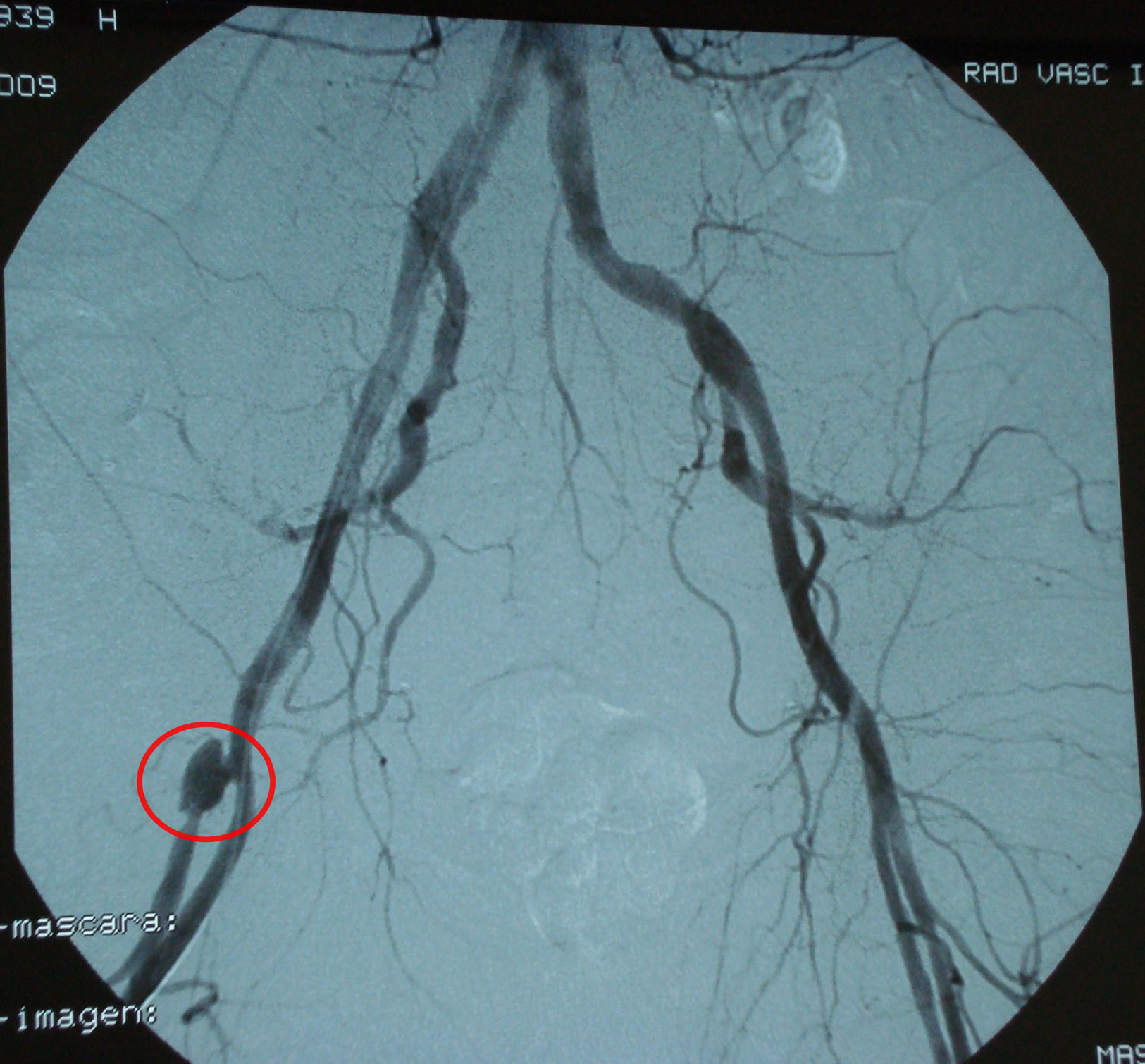
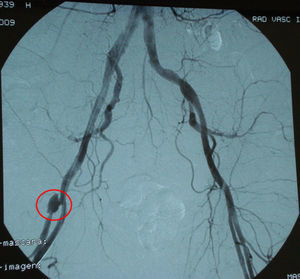
Con el diagnóstico de vasculitis séptica por SAMS se solicitó un ecocardiograma transesofágico que no evidenció vegetaciones ni datos sugestivos de endocarditis infecciosa, y una arteriografía que reveló la existencia de un pseudoaneurisma en la arteria femoral profunda derecha (fig. 4).
Con el diagnóstico definitivo de sepsis secundaria a pseudoaneurisma infeccioso postangioplastia de la arteria femoral profunda derecha, complicado con embolismos sépticos cutáneos locales, el paciente completó tratamiento con cloxacilina 1g/4 horas por vía intravenosa durante las dos primeras semanas y 1g/6 horas por vía oral durante las siguientes cuatro semanas, junto con reparación quirúrgica del pseudoaneurisma infeccioso, con resolución completa del cuadro.
DiscusiónEn 1985 Krupski et al publicaron el primer caso de pseudoaneurisma infeccioso postangioplastia6. Previamente, los casos descritos de endarteritis infecciosa complicada con embolismos sépticos locales eran secundarios al empleo de catéteres arteriales para la monitorización de constantes vitales en pacientes críticos7. La endarteritis séptica es la infección de la pared arterial. Su evolución natural es hacia la destrucción y dilatación de la misma, con la subsiguiente formación de un aneurisma o pseudoaneurisma infeccioso que eventualmente puede llegar a romperse. Frazee y Flaherty establecieron unos criterios para diferenciar entre infección local y endarteritis séptica postangioplastia2,5. Según ambos autores, esta última se definía por la evidencia clínica de infección local en el lugar de acceso del cateterismo y uno o más de los siguientes criterios: hemocultivos persistentemente positivos en ausencia de endocarditis infecciosa, evidencia de embolismos sépticos locales o el hallazgo en la exploración quirúrgica de un pseudoaneurisma macroscópicamente purulento.
En la etapa preantibiótica la causa más frecuente de endarteritis séptica y de aneurisma o pseudoaneurisma infeccioso era la endocarditis infecciosa, bien por la bacteriemia persistente con implante bacteriano en la pared arterial previamente dañada, bien como consecuencia de los microembolismos sépticos a través de la vasa vasorum. En la actualidad la causa más frecuente es el traumatismo vascular, debido al creciente empleo de procedimientos vasculares invasivos tanto diagnósticos como terapéuticos y al uso de drogas por vía parenteral6. El Staphylococcus aureus es el agente microbiológico más frecuentemente implicado en las endarteritis sépticas y en los pseudoaneurismas micóticos postangioplastia8.
Los factores de riesgo para desarrollar una endarteritis séptica postangioplastia son: a) la enfermedad arteriosclerótica avanzada; b) el antecedente de traumatismo vascular; y c) la inmunodeficiencia congénita o adquirida9. También existen factores de riesgo relacionados con la técnica de la angioplastia, como la dificultad en el acceso arterial, la duración del procedimiento o el mantenimiento de la vaina guía arterial entre 24 y 72 horas postangioplastia, pues se ha observado que, una vez transcurridas 24 horas, el 100% de las mismas presentan un trombo en su superficie. Asimismo, también predispone a la endarteritis séptica realizar una segunda revascularización coronaria accediendo por la misma arteria entre tres y siete días después de un primer procedimiento, y la formación de un hematoma posrevascularización en el lugar de acceso arterial, ya que daña la inmunidad local y favorece la proliferación bacteriana1-3,5,8,10. En nuestro caso se realizó una segunda angioplastia a través de la arteria femoral derecha, empleada también en una primera revascularización, con menos de una semana de diferencia, y existía un hematoma postangioplastia en la raíz del muslo derecho, lo que favoreció la formación de una endarteritis séptica que evolucionó hacia un pseudoaneurisma infeccioso.
La endarteritis séptica y su complicación evolutiva, el pseudoaneurisma infeccioso, pueden cursar con complicaciones potencialmente letales, como bacteriemia persistente, sepsis, rotura de la pared arterial con el subsiguiente shock hipovolémico, síndrome compresivo de estructuras neurovasculares adyacentes, artritis séptica u osteomielitis regional. En nuestro caso, la debilidad muscular aguda del miembro inferior derecho probablemente fue debida a una neuropatía femoral aguda compresiva. De hecho, los pseudoaneurismas de la arteria femoral profunda pueden cursar de forma exclusiva con este signo clínico11,12. Por otro lado, las manifestaciones cutáneas derivadas de un pseudoaneurisma infeccioso postangioplastia, consecuencia de los embolismos sépticos cutáneos regionales, son variadas y pueden presentarse como púrpura palpable, petequias, pústulas, cianosis digital y livedo reticularis1,5,11,13,14.
Ante lesiones cutáneas unilaterales en miembros intervenidos mediante procedimientos vasculares, el diagnóstico diferencial debe plantearse con el síndrome de embolismos de colesterol y con la endocarditis infecciosa aguda postangioplastia. El primero es un síndrome con una elevada morbimortalidad, típico de varones de edad avanzada con arteriosclerosis evolucionada, tras procedimientos vasculares invasivos, anticoagulación o trombólisis. Las manifestaciones cutáneas, como la livedo reticularis, la cianosis digital, la púrpura palpable, las petequias, los nódulos y las úlceras acras, entre otras, son las más frecuentes y habitualmente son el primer signo clínico15. En nuestro caso no se objetivaron cristales de colesterol intravasculares en la histopatología. Por otro lado, la endocarditis infecciosa es una complicación séptica excepcional tras una angioplastia. En nuestro paciente se descartó no solo por la unilateralidad de las lesiones dermatológicas y la ausencia de datos ecocardiográficos compatibles con esta entidad, sino también por la ausencia tanto clínica como radiológica de embolismos sépticos en otros órganos, tales como el sistema nervioso central, el bazo y los riñones, entre otros.
Algunos autores recomiendan, como medidas preventivas para minimizar las complicaciones infecciosas postangioplastia, retirar la vaina arterial lo antes posible tras la revascularización y emplear el miembro contralateral cuando sea necesaria una segunda angioplastia con una diferencia de tiempo inferior a una semana con respecto al primer procedimiento. Si por razones técnicas el miembro contralateral es inadecuado y el paciente es de alto riesgo, tal vez debería emplearse antibioterapia profiláctica, aunque no existen suficientes estudios que avalen esta recomendación2,3,5,8.
Como conclusión, resulta esencial sospechar precozmente esta entidad cuando un paciente, tras haber sido sometido a un procedimiento vascular invasivo, presente fiebre sin foco aparente con hemocultivos persistentemente positivos y sin evidencia de endocarditis infecciosa en el ecocardiograma. En este contexto clínico, si aparecen lesiones cutáneas ipsilaterales al miembro intervenido, se debe considerar en el diagnóstico diferencial no solo los embolismos cutáneos de colesterol, sino también los embolismos sépticos secundarios a esta entidad. La confirmación diagnóstica se obtendrá a través de la biopsia cutánea, demostrando la existencia del microorganismo no solo en la histopatología, sino también en el cultivo microbiológico, lo que permitirá solicitar pruebas de imagen arteriales que descarten la existencia de un aneurisma o pseudoaneurisma infeccioso como complicación evolutiva de una endarteritis séptica postangioplastia.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.