Hasta hace pocos años, los casos graves de dermatitis atópica (DA) se trataban con corticosteroides e inmunosupresores clásicos. Sin embargo, dichos tratamientos no eran adecuados para el tratamiento a largo plazo, debido a cuestiones de seguridad, especialmente en niños y adolescentes. La aprobación de terapias biológicas e inhibidores de JAK para uso en adolescentes con DA de moderada a grave ha ampliado las opciones terapéuticas1. Se ha añadido upadacitinib al armamento terapéutico de los adolescentes (≥12 años) con DA y al plan de cuidados escalonado para este grupo en la última versión de las guías europeas de práctica clínica sobre el manejo del eccema atópico2. Se han publicado estudios que reportan experiencias de la vida real con upadacitinib en pacientes adultos con DA3–6 aunque, sin embargo, la evidencia sobre su uso en adolescentes es escasa7–10. El objetivo de este estudio es evaluar el perfil de seguridad y eficacia a medio plazo de upadacitinib en adolescentes (12-18 años) con DA de moderada a grave en la práctica clínica del mundo real.
Realizamos un estudio retrospectivo multicéntrico y no intervencionista que incluyó a 16 hospitales españoles de enero de 2022 a 2023. La gravedad de la enfermedad se midió mediante las escalas EASI (Eczema Area and Severity Index), IGA (Investigator Global Assessment) validada, y NRS (Numerical Rating Scale) de prurito. El criterio de valoración primario fue el análisis de la efectividad de upadacitinib en términos de puntuaciones EASI absolutas en las semanas 4, 16 y 24 (de existir), así como el porcentaje de pacientes que lograron respuesta EASI-75 y EASI-90. Los criterios de valoración secundarios incluyeron la evaluación de IGA, NRS de prurito, y el perfil de seguridad del fármaco. El análisis estadístico incluyó medidas de tendencia central y dispersión para las variables continuas, y frecuencias para las variables categóricas. La regresión logística evaluó el impacto del peso, la duración de la enfermedad, el sexo y el asma en la respuesta EASI.
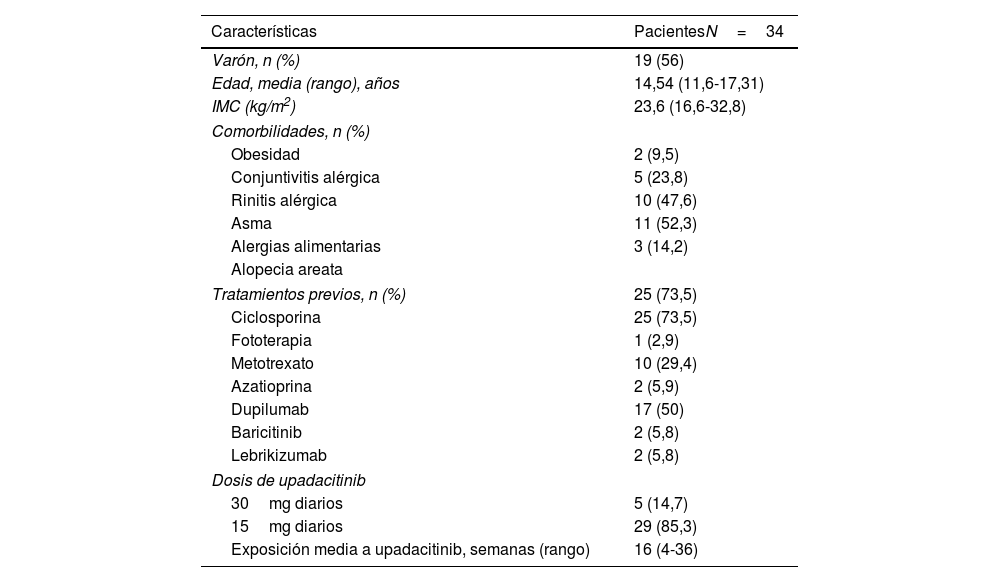
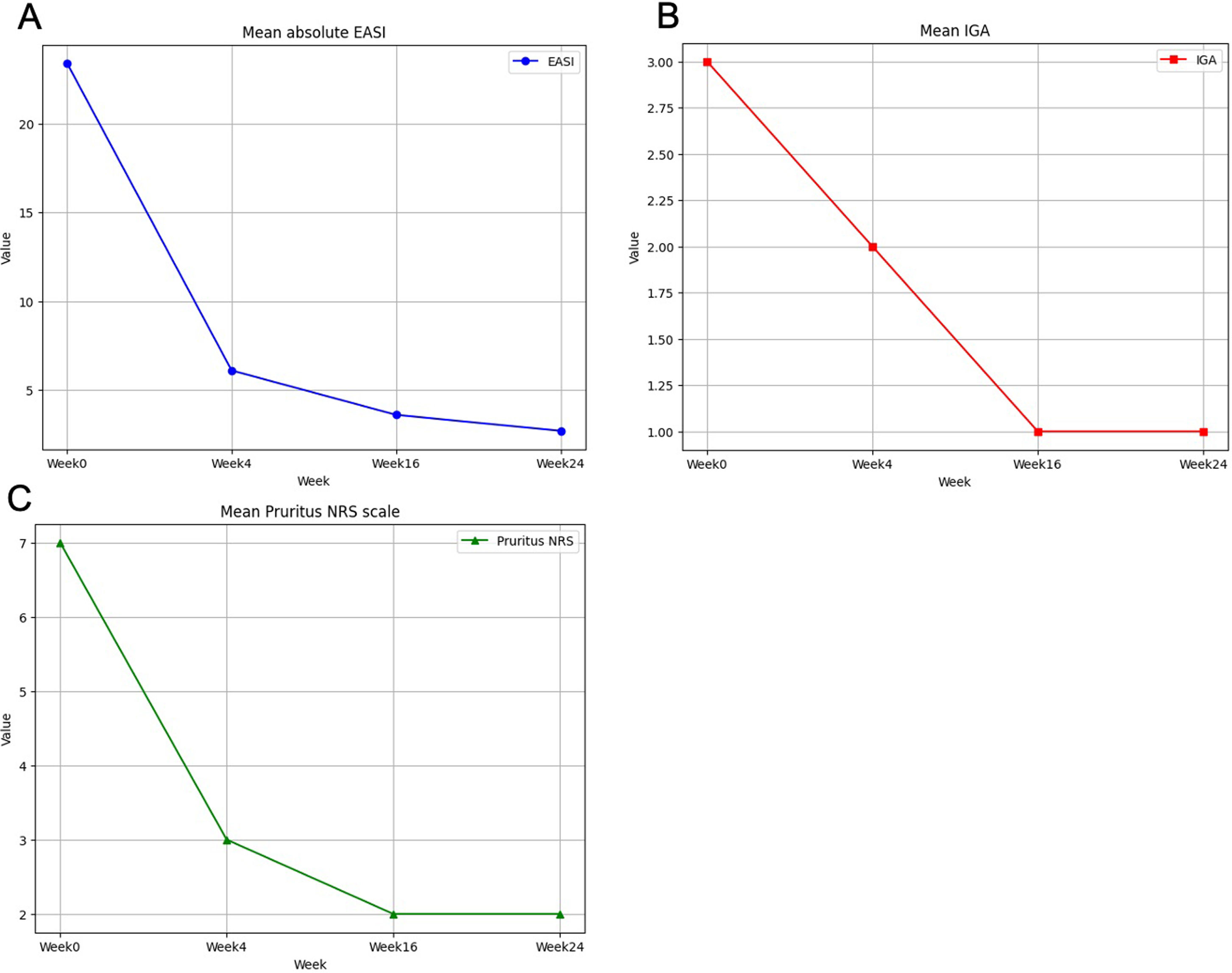
Se incluyó un total de 34 pacientes. Las características demográficas y clínicas se muestran en la tabla 1. La duración media de la enfermedad fue de 6,3 (0,4-15) años. El IMC medio fue de 22,5 (16,6-32,8), siendo 6 (17,6%) pacientes obesos (IMC >30kg/m2). Las comorbilidades atópicas concomitantes más comunes fueron asma (23,5%) y rinitis alérgica (20,6%). Aproximadamente el 73,5% de los pacientes habían recibido terapias sistémicas previamente al inicio de upadacitinib (73,5%, ciclosporina y 50%, dupilumab). Se permitió el uso ocasional de corticosteroides tópicos de baja potencia. Upadacitinib fue el primer inmunomodulador sistémico para 9 pacientes (sin tratamiento). Muchos pacientes (85,3%) recibieron una dosis diaria de upadacitinib de 15mg. Se observó una respuesta rápida a este fármaco. La puntuación EASI media (rango) fue de 23,4 (intervalo de confianza del 95%, 21,3-25,3) en la reducción basal a 6,1 (4,7-7,6), 3,6 (2,6-4,6) y de 2,7 (0-6) en las semanas 4.a, 16.a y 24.a, respectivamente. Se produjo una reducción rápida de la puntuación de NRS de prurito, que se redujo de una media de 7 puntos durante el descenso basal, a 3 puntos en la semana 4 (tabla 2 y fig. 1 del material adicional). Ya en una etapa temprana (semana 4), 26 y 20 pacientes lograron respuestas EASI-75 y EASI-90, respectivamente. No se encontró una relación estadísticamente significativa en las variables de sexo, peso, duración de la DA o presencia de asma y probabilidad de lograr una respuesta EASI-90 (tabla del material adicional). En los pacientes que siguieron previamente tratamiento de dupilumab y baricitinib, la efectividad del fármaco fue tan buena como los pacientes «sin tratamiento bio». Tres pacientes no lograron respuesta EASI-75 a lo largo del periodo evaluado. No se reportaron infecciones graves ni episodios cardiovasculares adversos mayores (MACE). Hasta 4 pacientes reportaron un empeoramiento leve del acné, que fue tratado con productos tópicos, mientras que 3 pacientes experimentaron un empeoramiento de su DA.
Características demográficas y clínicas basales
| Características | PacientesN=34 |
|---|---|
| Varón, n (%) | 19 (56) |
| Edad, media (rango), años | 14,54 (11,6-17,31) |
| IMC (kg/m2) | 23,6 (16,6-32,8) |
| Comorbilidades, n (%) | |
| Obesidad | 2 (9,5) |
| Conjuntivitis alérgica | 5 (23,8) |
| Rinitis alérgica | 10 (47,6) |
| Asma | 11 (52,3) |
| Alergias alimentarias | 3 (14,2) |
| Alopecia areata | |
| Tratamientos previos, n (%) | 25 (73,5) |
| Ciclosporina | 25 (73,5) |
| Fototerapia | 1 (2,9) |
| Metotrexato | 10 (29,4) |
| Azatioprina | 2 (5,9) |
| Dupilumab | 17 (50) |
| Baricitinib | 2 (5,8) |
| Lebrikizumab | 2 (5,8) |
| Dosis de upadacitinib | |
| 30mg diarios | 5 (14,7) |
| 15mg diarios | 29 (85,3) |
| Exposición media a upadacitinib, semanas (rango) | 16 (4-36) |
Efectividad de upadacitinib a lo largo del estudio
| Basal | S4(N=34) | S16(N=34) | S24(N=18) | |
|---|---|---|---|---|
| Media EASI (rango) | 23,4 (21,3-25,3) | 6,1 (4,7-7,6) | 3,6 (2,6-4,6) | 2,7 (0-6) |
| Media IGA (rango) | 3 (2-4) | 2 (0-3) | 1 (0-3) | 1 (0-2) |
| Media de NRS de prurito (rango) | 7 (4-10) | 3 (0-8) | 2 (0-6) | 2 (0-5) |
DE: desviación estándar; EASI: Eczema Area and Severity Index; IGA: Investigator Global Assessment; NRS: Numerical Rating Scale; S: semana. Calculado para un IC (intervalo de confianza) del 95%.
Este estudio demuestra la respuesta rápida y sostenida de upadacitinib en el tratamiento de la DA de moderada a grave en adolescentes en el ámbito del mundo real. Los pacientes tuvieron perfiles de la enfermedad graves y fueron refractarios a múltiples terapias sistémicas, incluyendo tratamientos biológicos y otros inhibidores de JAK (baricitinib) que difieren de los incluidos en ensayos clínicos1. Un hallazgo interesante es que muchos de nuestros sujetos tratados con 30mg o 15mg diarios lograron respuestas EASI-75 y EASI-90 muy tempranas (76,4% y 58,8%, respectivamente) en la semana 4.a. Nuestros resultados reflejaron unas tasas de respuesta EASI-75 en la semana 16.a, en comparación con los ensayos clínicos de adolescentes con DA que recibieron upadacitinib, lo cual es consistente con los hallazgos reportados por Hagino et al.8. Dicha respuesta rápida en adolescentes ha sido también reportada y confirmada por otros autores7–10. Los pacientes experimentaron una reducción rápida de RNS de prurito pocos días después de iniciar el tratamiento, aún mayor que la obtenida en los ensayos de upadacitinib1. Las limitaciones de este estudio incluyen su diseño observacional y retrospectivo, el pequeño tamaño de la muestra, y el corto seguimiento. En conclusión, a nuestro saber, esta es una de las mayores series clínicas del mundo real hasta la fecha, con un número significativo de pacientes adolescentes que recibieron upadacitinib, y que reporta la eficacia a corto plazo y la respuesta rápida de upadacitinib a la hora de lograr el control del prurito incluso en casos recalcitrantes de larga duración, y aquellos que discontinuaron el tratamiento con dupilumab debido a la pérdida de eficacia o los efectos secundarios.
Declaración de contribución de autoría CRediTF.J. Melgosa Ramos y Sergio Santos Alarcón contribuyeron de igual modo a la concepción, diseño, recopilación y análisis de los datos, interpretación, redacción–preparación del borrador y revisión del presente trabajo. La versión final a publicar ha sido aprobada por todos los autores. El resto de los autores contribuyó al diseño de concepción, a la recopilación de los datos y a la revisión del presente trabajo.
Declaración éticaEl estudio 59 fue realizado de acuerdo con los principios contenidos en la Declaración de Helsinki para estudios que incluyen humanos. Todos los pacientes (y padres) aportaron su consentimiento informado escrito.
FinanciaciónLos autores no han recibido ningún tipo de financiación (institucional, privada y corporativa) para el estudio reportado en este documento.
Conflicto de interesesEl(los) autor(es) declara(n) que no existen conflictos de interés con relación a la publicación de este documento.
AgradecimientosA Antonio Torrelo Fernández, Raúl de Lucas Laguna, Salvador Arias Santiago, Almudena Mateu Puchades, Altea Esteve Martínez, Carlos Abril Pérez, Laia Curto Barredo, Minia Campos Domínguez, Juan José Pereyra-Rodriguez, Mónica Munuera Campos, Ana Martín Santiago, Gloria Garnacho Saucedo, Eulalia Baselga Torres, Juan Francisco Silvestre Salvador, Lucero Noguera Morel, Esther Fiz Benito, José Mª Sánchez Motilla, Violeta Zaragoza Ninet, Mercedes Rodríguez Serna, Ana Llull Ramos and Victor González Delgado por su contribución a la recopilación de los datos.
Disponibilidad de los datosPuede disponerse de todos los datos previa solicitud a los autores.