El carcinoma basocelular (CBC) representa el 80% de cáncer cutáneo no melanoma y su incidencia va en aumento1. La mayoría de los CBC son de lento crecimiento y el tratamiento quirúrgico es curativo en la mayoría de los casos. Pero, ocasionalmente, el tumor progresa localmente, invadiendo estructuras vecinas, o sistémicamente, hasta convertirse en inabordable con intención curativa mediante la cirugía o la radioterapia. Para estos casos se ha acuñado el término CBC localmente avanzado (CBC-LA) y se calcula que representan el 0,8% de todos los CBC2.
La vía de señalización Hedgehog (Hh), involucrada en el crecimiento y polarización celular e inactiva en los adultos, desempeña un papel importante en la patogénesis del CBC al activarse mediante mutaciones en las moléculas de la vía de señalización Hh3. El vismodegib y el sonidegib inhiben la vía de señalización Hh, uniéndose a la proteína SMO e inactivando el crecimiento tumoral. Actualmente, el vismodegib está indicado en el CBC-LA y metastásico, mientras que el sonidegib solo tiene indicación para CBC-LA2-5. A pesar de que ambos fármacos alcanzan una tasa de respuesta objetiva superior al 47 y al 60%, respectivamente, la combinación con otras terapias permite alcanzar unas tasas de respuesta mejores2,5.
Describimos a continuación una paciente con un CBC-LA en el que la combinación entre el tratamiento sistémico (vismodegib) y diferentes terapias físicas permitieron conseguir una respuesta clínica completa y de larga duración.
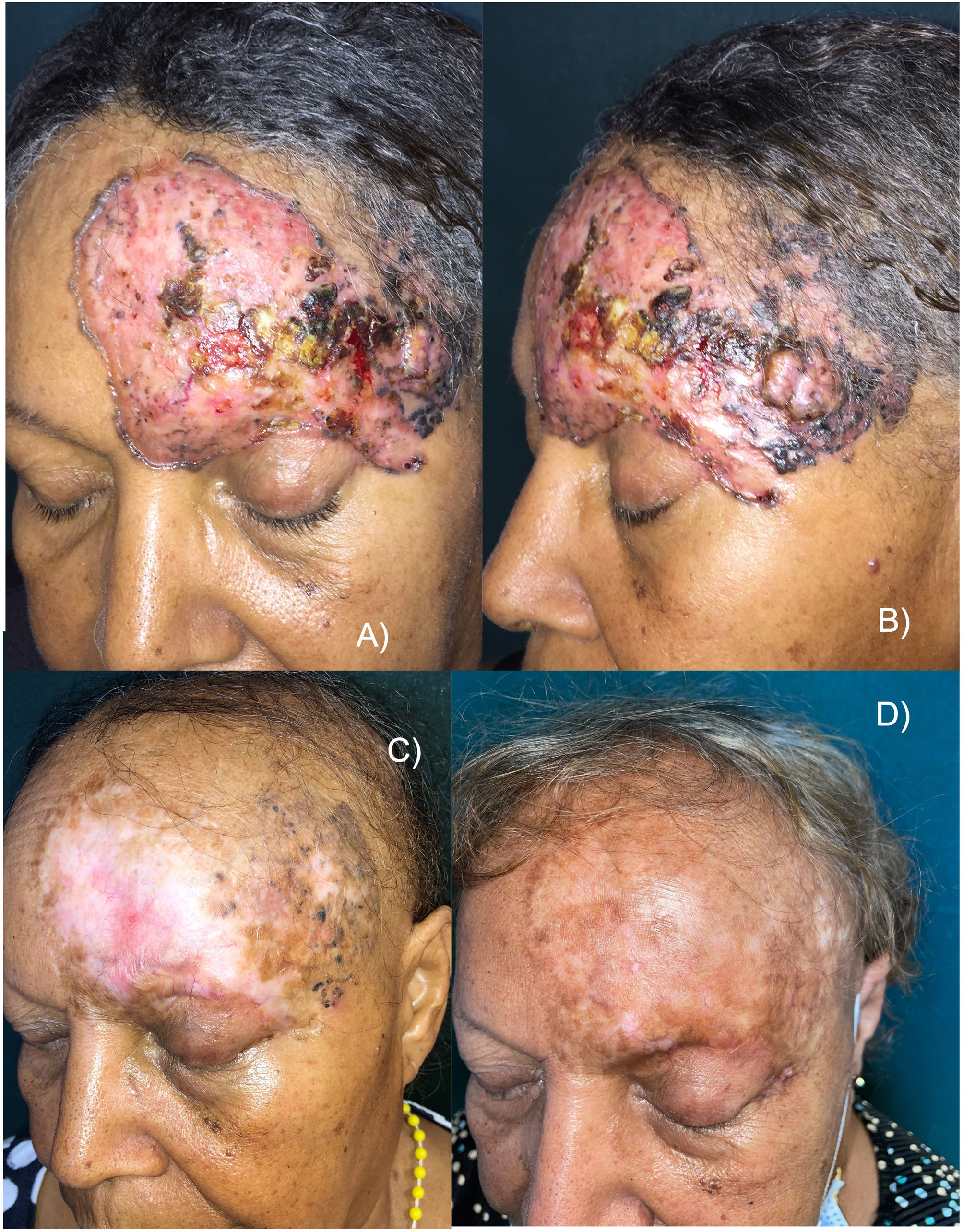
Una mujer de 65 años, sin antecedentes personales de interés, consultó por una lesión frontal de 30 años de evolución. A la exploración física, en la región frontal izquierda, se constató una placa nodular tumoral, ulcerada de 12×8cm con erosiones y áreas de pigmento (fig. 1A y B). Una biopsia confirmó el diagnóstico de CBC sólido pigmentado. Las pruebas de imagen mostraron la afectación del párpado superior y la región tarsal interna, en contacto con el hueso frontal sin signos de invasión y sin metástasis a distancia. El estudio de extensión descartó la presencia de adenopatías, masas y megalias. El diagnóstico definitivo fue de CBC en estadio III (T3N0M0)6. En el comité multidisciplinar de tumores cutáneos se descartaron tanto la cirugía como la radioterapia como opciones curativas, por lo que se administró vismodegib 150mg/día, por vía oral. A los 2meses se observó una respuesta clínica lenta pero progresiva, con una disminución del tamaño y una desaparición progresiva del eritema, así como una epitelización de las erosiones. No obstante, persistía una zona de pigmento. La paciente desarrolló algunas toxicidades características del vismodegib: disgeusia (grado 2), calambres musculares (grado 1), alopecia (grado 2) y pérdida de peso (grado 1), que no requirieron de la suspensión del fármaco.
A y B) Aspecto del tumor antes de comenzar el tratamiento. Placa eritematosa, con áreas erosionadas, ulceradas, costrosas y con abundante pigmento. C) Tras 18 meses con vismodegib. Respuesta parcial del tumor. Observamos alopecia como toxicidad característica de este fármaco. D) A los 30 meses de seguimiento (12 meses tras la suspensión de vismodegib). Remisión clínica completa, repigmentación significativa y alopecia en repoblación.
Tras 18 meses de tratamiento y alcanzándose una disminución de la masa tumoral superior al 95%, se apreció una estabilización de la respuesta y se suspendió el vismodegib (fig. 1C). Se biopsió la lesión residual, donde se apreciaban nidos residuales de CBC sólido pigmentado. A pesar de que en las guías se reconoce que la TFD no es efectiva en CBC pigmentados1, de acuerdo con la elección de la paciente se aborda la zona pigmentada residual secuencialmente con 4 sesiones de terapia fotodinámica (aminolevulinato de metilo con 3 h de exposición y dosis 37J/cm2), imiquimod tópico (5 días por semana durante 4 meses) y una escisión conservadora del último resto tumoral apreciable, confirmándose la persistencia de CBC sin afectar los márgenes quirúrgicos.
A los 6 meses de suspendido el tratamiento, se apreció una recidiva del CBC (confirmada histológicamente) en el canto externo del ojo izquierdo, que se trató con radioterapia en todo el campo, con fotones (80kV) y electrones (6 MeV) alcanzando una dosis total de 4.000 cGy. Tras el tratamiento la paciente quedó en remisión clínica completa, que continúa 30 meses después de la finalización de la radioterapia. Todas las biopsias realizadas tras vismodegib fueron informadas como CBC sólido.
La ageusia y los calambres desaparecieron y la alopecia estaba en proceso de repoblación. Es reseñable también la recuperación parcial pero muy llamativa de la hipopigmentación observada tras el tratamiento con vismodegib (fig. 1D).
La literatura muestra la eficacia del vismodegib en el tratamiento del CBC-LA, tanto en monoterapia como en neoadyuvancia, mostrando unas tasas altas de remisión con un buen resultado funcional y estético, y un buen perfil de seguridad7-9. En nuestro caso, con el vismodegib se consiguió una respuesta clínica lenta pero progresiva, suficiente como para que mediante el uso combinado de diferentes terapias físicas y quirúrgicas pudiera obtenerse una respuesta completa, con una toxicidad tolerable.
En la práctica diaria, la combinación del vismodegib con terapias tópicas, cirugía, radioterapia o terapias sistemicas8-10 constituye una opción terapéutica eficaz y segura. Sin embargo, se requieren más estudios para saber qué pacientes van a responder, durante cuánto tiempo van a responder, así como conocer la secuencia adecuada de la combinación de terapias para conseguir el mejor resultado con la mínima toxicidad.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.