En esta revisión se pretenden abarcar todos los aspectos relacionados con el tratamiento de la artritis psoriásica así como la evaluación de la respuesta al tratamiento. Por este motivo, se definen los diferentes métodos de evaluación que se utilizan en la actualidad para valorar la respuesta al tratamiento de los pacientes con artritis psoriásica y las exploraciones complementarias que deben realizarse para el correcto seguimiento de estos pacientes. A través de estas herramientas, tanto el dermatólogo como el reumatólogo pueden evaluar la evolución, gravedad y pronóstico de la enfermedad en cada momento. En relación al tratamiento se exponen las líneas de tratamiento propuestas por la GRAPPA y la Sociedad Española de Reumatología (SER) y se introduce la aparición de nuevas terapias emergentes para el tratamiento de esta enfermedad y la mejora de su pronóstico.
This review aims to cover all aspects related to the treatment of psoriatic arthritis and the evaluation of the response to treatment. We define the various evaluation methods currently used to assess response to treatment in patients with psoriatic arthritis and the complementary examination techniques used to ensure adequate follow-up. These tools enable both the dermatologist and the rheumatologist to carry out an ongoing evaluation of the clinical course, severity, and prognosis of the disease. The treatment lines proposed by the Group for Research and Assessment of Psoriasis and Psoriatic Arthritis and the Spanish Society of Rheumatology are discussed. Emerging strategies for treating this condition and improving prognosis are examined.
Los métodos de evaluación de la artritis psoriásica (APso) surgen de la necesidad de evaluar la actividad de la enfermedad en un momento dado de su evolución, los cambios que aparecen en esta y las modificaciones que sufre al aplicar un tratamiento determinado. Son necesarios para comprender la historia natural de la enfermedad y la efectividad de los tratamientos, y se aplican sistemáticamente en los ensayos clínicos, aunque su utilización clínica es algo limitada. Además, la propia enfermedad sufre fluctuaciones de la actividad durante periodos de tiempo cortos, por lo que el resultado de la aplicación de un método de evaluación en un momento puntual puede no ser válido en un periodo de tiempo relativamente corto.
Además de los métodos de evaluación de la enfermedad también son importantes las medidas de evaluación de la funcionalidad y calidad de vida de los pacientes con APso. Las más utilizadas son el Health Assessment Questionnaire (HAQ), destinado a valorar el grado de pérdida de funcionalidad articular, y el Study Short Form 36 (SF-36), más específico para valorar la calidad de vida de los pacientes.
Los métodos de evaluación actualmente utilizados para la APso han sido adaptados a partir de los previamente existentes para la artritis reumatoide (Disease Activity Score o DAS), las espondiloartropatías (Bath Ankylosing Spondylitis Disease Activity Index o BASDAI) y la psoriasis (Psoriasis Area and Severity Index o PASI). El Group for Research and Assessment of Psoriasis and Psoriatic Arthritis (GRAPPA) y el grupo Outcome Measures in Rheumatology Clinical Trials (OMERACT)1 proponen los métodos de evaluación a utilizar en ensayos clínicos, aunque los únicos que se consideran válidos en la práctica clínica diaria son el DAS-28 para la artritis reumatoide y el BASDAI para las espondiloartropatías. Con el fin de aumentar su especificidad se están elaborando nuevas escalas que incluyen datos objetivos como la velocidad de sedimentación globular (VSG) o la proteína C reactiva (PCR) (ASAS-Endorsed Disease Activity Score o AS-DAS)2.
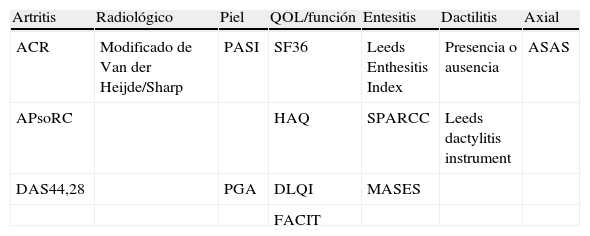
Estos métodos (tabla 1) pretenden evaluar los diferentes dominios de la APso, que son los diferentes aspectos clínicos, reumatológicos, cutáneos y psicológicos que afectan a los pacientes con APso y que deben evaluarse y tratarse específicamente. De este modo, se evalúan los síntomas y signos de afectación articular y cutánea, evaluación de la entesitis, dactilitis y espondilitis, así como la valoración de la funcionalidad, calidad de vida, fatiga y cambios estructurales, determinados mediante radiología simple.
Métodos de evaluación en la APso
| Artritis | Radiológico | Piel | QOL/función | Entesitis | Dactilitis | Axial |
| ACR | Modificado de Van der Heijde/Sharp | PASI | SF36 | Leeds Enthesitis Index | Presencia o ausencia | ASAS |
| APsoRC | HAQ | SPARCC | Leeds dactylitis instrument | |||
| DAS44,28 | PGA | DLQI | MASES | |||
| FACIT |
ACR: American College of Rheumatology; APsoRC: APso response criteria; ASAS: Assessment in Ankylosing Spondylitis; DAS: Disease Activity Score; DLQI: Disability Index Dermatology Life Quality Index; FACIT: Functional Assessment of Chronic Illness Therapy; HAQ: Health Assessment Questionnaire; MASES: Maastricht Ankylosing Spondylitis Enthesis score; PASI: Psoriasis Area and Severity Index; PGA: Physician Global Assessment of Psoriasis; SF36: Short Form 36 Health Survey; SPARCC: Canadian Spondyloarthropathy Group. Modificado de Mease5.
El criterio del American College of Rheumatology (ACR) y el DAS fueron desarrollados para evaluar la actividad de la artritis reumatoide. Son los métodos aceptados por la European League against Rheumatism (EULAR).
El criterio de la ACR consiste en el recuento de articulaciones afectas teniendo en cuenta un total de 68 posibles articulaciones dolorosas (interfalángicas distales, proximales, metacarpofalángicas de las manos, metatarsofalángicas de los pies, carpometacarpianas, muñecas, hombros, codos, acromioclaviculares, esternoclaviculares, caderas, rodillas, talo-tibiales y mediotarsales) y 66 posiblemente inflamadas (las mismas excepto las caderas (coxofemorales). Ambos parámetros se evalúan de 1 a 3. La respuesta ACR 20, 50 y 70 consiste en la mejoría del 20, 50 y 70% respectivamente de las articulaciones afectas. Este criterio aplicado a la APso se denomina APsoRC (APso response criteria)1.
El DAS fue desarrollado en Europa para evaluar la actividad de la AR y los cambios de esta enfermedad con el tratamiento. La ventaja del DAS sobre el ACR es que el ACR solo mide cambios en la actividad de la enfermedad mientras que el DAS además permite evaluar la intensidad real de la enfermedad en un momento dado. La aplicación del DAS permite clasificar a los pacientes en 3 grupos: no respondedores, respondedores moderados y buenos respondedores. El más utilizado es el DAS28, con un recuento total de 28 articulaciones1.
Dado que la APso es una enfermedad que afecta otros componentes del sistema musculoesquelético, además de las articulaciones periféricas, a continuación resumimos los criterios de evaluación de la afectación axial, entesitis y dactilitis.
Afectación axialLa afectación axial se presenta en aproximadamente el 50% de los pacientes con APso, con sacroileítis en el 25% de los casos.
El diagnóstico de enfermedad axial responde a la presencia de 2 de los 3 siguientes criterios:
- 1.
Dolor de espalda de carácter inflamatorio (incluye edad <45 años, duración de los síntomas >3 meses, rigidez matutina >30min, inicio insidioso, mejora con el ejercicio, dolor alternante en glúteos).
- 2.
Limitación del movimiento cervical, torácico o lumbar en el plano sagital y frontal.
- 3.
Criterio radiológico.
Si bien la afectación axial en los pacientes con APso suele ser más variable y asimétrica que en la espondilitis anquilosante, los criterios de evaluación que se utilizan suelen ser los correspondientes a esta última enfermedad y propuestos por la Assessment in Ankylosing Spondylitis Working Group (ASAS), como el Bath Ankylosis Spondylitis Disease Activity Index (BASDAI), el Bath Ankylosis Spondylitis Function Index (BASFI) y el Bath Ankylosis Spondylitis Metrology Index (BASMI)1.
El criterio de evaluación de la actividad de la enfermedad axial más utilizado habitualmente en la consulta es el BASDAI, considerándose la enfermedad como activa cuando la puntuación es ≥4. Cuando se evalúa la respuesta al tratamiento, el BASDAI debe aplicarse a las 6 semanas de haber iniciado el tratamiento. Se considera que existe respuesta al tratamiento cuando la puntuación del BASDAI es <3 o se produce una disminución de 2 puntos.
EntesitisEl diagnóstico de entesitis puede realizarse actualmente mediante tres aproximaciones; a través de la exploración física y la palpación de tendones, ligamentos y cápsulas de inserción, la ecografía y la RMN.
Los índices de evaluación que se usan para valorar la entesitis en las espondiloartropatías (y por ende en la APso) fueron elaborados para la evaluación de la entesitis en la espondilitis anquilosante, y no existe un acuerdo generalizado en cuanto a su utilización. Se trata del Mander Enthesitis Index (MEI), el Maastricht Ankylosing Spondylitis Enthesis Score (MASES) y el Major Enthesitis Index. El índice Mander o MEI valora 66 puntos mientras que el MASES se focaliza en los 13 puntos más relevantes del anterior. El MEI es un índice poco rentable por el tiempo que requiere para su aplicación y porque no discrimina algunos puntos también afectados por la fibromialgia. El MASES fue elaborado precisamente por la necesidad de obtener una medida de aplicación más sencilla con una sensibilidad similar. El índice SPARCC del Canadian Spondyloarthropathy Group se centra en la entesitis de la fascia plantar, el tendón de Aquiles, la tuberosidad tibial y las inserciones del manguito de los rotadores.
Healy propone el Leeds Enthesitis Index, elaborado a partir de los anteriores, junto al Major index y el Gladman index, de modo que valora las inserciones de los tendones de Aquiles, los cóndilos mediales femorales y los epicóndilos laterales del húmero3. La ventaja de este índice respecto a los anteriores es que solo analiza 6 puntos y es de rápida aplicación.
DactilitisLa valoración más frecuente de la dactilitis usada en la práctica clínica habitual consiste en registrar su presencia o ausencia. Su presencia es de gran ayuda para confirmar una elevada sospecha para el diagnóstico de APso.
Exploraciones complementariasAunque el diagnóstico de la APso es fundamentalmente clínico, para evaluar la presencia y grado de afectación en los diferentes dominios de la enfermedad es importante efectuar diversas exploraciones complementarias.
VSG y PCRTanto la VSG como la PCR son parámetros marcadores de inflamación. La persistencia de niveles elevados de VSG y/o PCR sérica en un paciente con APso indican persistencia de la actividad inflamatoria, incluso a pesar de que el paciente persista asintomático. En los pacientes bajo tratamiento los cambios en los niveles de marcadores de la inflamación pueden ser utilizados para monitorizar la respuesta al tratamiento, de modo que niveles persistentemente elevados indican falta de respuesta al mismo.
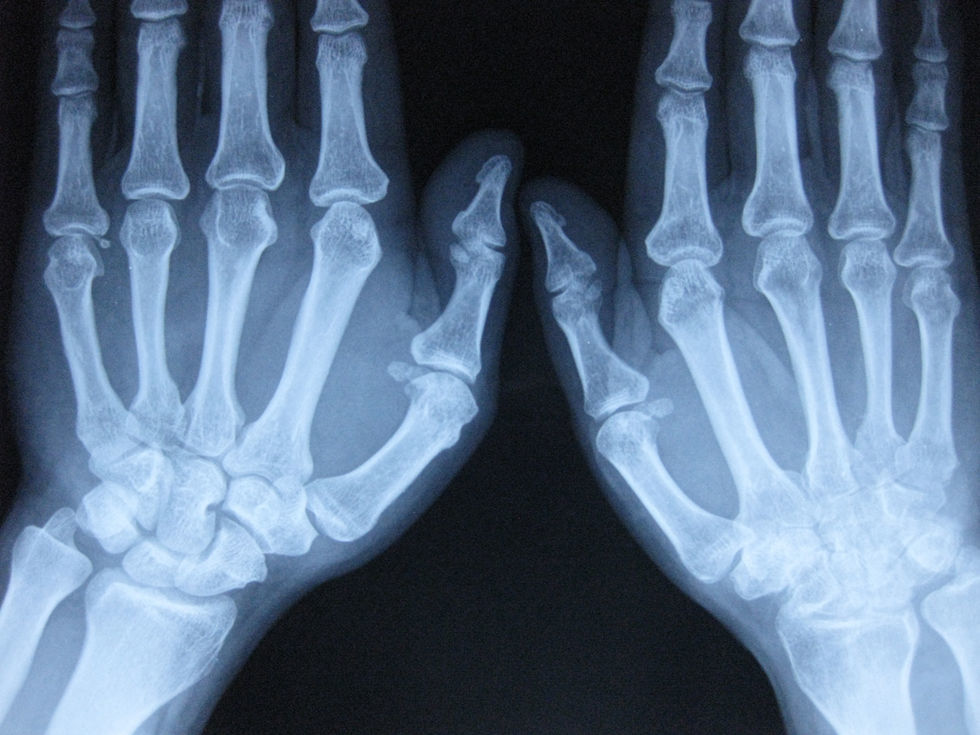
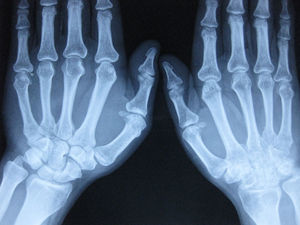
Radiología simpleHasta el momento es la única prueba de imagen validada para valorar el grado de afectación articular en la APso, la progresión y la respuesta terapéutica, pero no es útil para valorar la afectación de otras estructuras musculoesqueléticas como las entesis, los tendones y ligamentos. La solicitud de radiografías a un paciente determinado para valorar el nivel de afectación articular se realizará según la clínica y la exploración física del paciente, de forma dirigida (fig. 1).
EcografíaLa utilización de la ecografía como prueba de imagen complementaria en el estudio de la APso es de especial importancia en la valoración de la entesitis, aunque su eficacia no ha sido determinada. La afectación de la fascia plantar es la que muestra mayor correlación clínica con la ecografía. Asimismo se puede valorar la presencia de sinovitis en las articulaciones afectadas, y el grado de vascularización de dicha sinovitis, mediante el uso de la ultrasonografía Power Doppler.
RESONANCIA MAGNÉTICA NUCLEAR (RMN)La RMN detecta, con buena correlación clínico-patológica, las diferentes estructuras del sistema musculoesquelético, aunque no está validada como herramienta de diagnóstico en la práctica clínica habitual. En el caso de la sospecha clínica de entesitis, la RMN detecta el edema óseo y la osteitis asociados a esta. Asimismo, en articulaciones de difícil exploración, como las sacroilíacas, el uso de la RMN es de gran ayuda para valorar la presencia de sinovitis o erosiones, confirmando la sospecha diagnóstica.
Evolución y gravedad de la enfermedadLos factores clínicos que predicen un peor pronóstico de la APso son la afectación poliarticular, la elevación de los reactantes de fase aguda, la evidencia de enfermedad erosiva y osteoproliferativa, con destrucción anatómica e irreversibilidad del deterioro funcional, y la falta de respuesta a agentes terapéuticos.
Aproximadamente el 20% de los pacientes con APso evolucionan hacia formas severas y debilitantes de artritis que dan lugar a una gran alteración de la calidad de vida y funcionalidad del paciente.
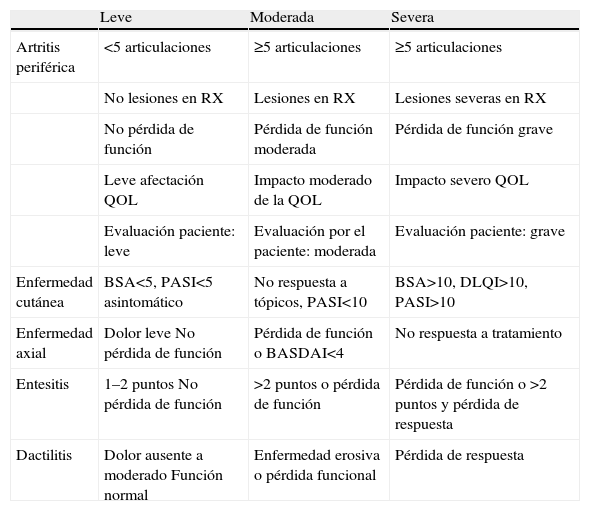
En la consulta clínica habitual es importante poder clasificar al paciente con APso en categorías según el nivel de gravedad de su enfermedad articular y musculoesquelética, teniendo en cuenta los diferentes dominios de afectación y poder establecer el tratamiento más adecuado para cada paciente y cada estadio de gravedad. El GRAPPA propone una herramienta que utiliza algunos métodos de evaluación descritos con anterioridad como el BASDAI y algunos parámetros valorados por el médico en la consulta4. Este método de clasificación se describe en la tabla 2.
Niveles de gravedad de la artritis psoriásica según el GRAPPA
| Leve | Moderada | Severa | |
| Artritis periférica | <5 articulaciones | ≥5 articulaciones | ≥5 articulaciones |
| No lesiones en RX | Lesiones en RX | Lesiones severas en RX | |
| No pérdida de función | Pérdida de función moderada | Pérdida de función grave | |
| Leve afectación QOL | Impacto moderado de la QOL | Impacto severo QOL | |
| Evaluación paciente: leve | Evaluación por el paciente: moderada | Evaluación paciente: grave | |
| Enfermedad cutánea | BSA<5, PASI<5 asintomático | No respuesta a tópicos, PASI<10 | BSA>10, DLQI>10, PASI>10 |
| Enfermedad axial | Dolor leve No pérdida de función | Pérdida de función o BASDAI<4 | No respuesta a tratamiento |
| Entesitis | 1–2 puntos No pérdida de función | >2 puntos o pérdida de función | Pérdida de función o >2 puntos y pérdida de respuesta |
| Dactilitis | Dolor ausente a moderado Función normal | Enfermedad erosiva o pérdida funcional | Pérdida de respuesta |
Modificado de Richlin4. RX: radiografía.
Se considera que los factores asociados a un peor pronóstico de la enfermedad articular periférica son: número de articulaciones inflamadas (enfermedad poliarticular), VSG elevada, falta de respuesta a tratamiento, presencia de alteración radiológica, pérdida de funcionalidad (valorada por el HAQ) y disminución de la calidad de vida (SF 36, DLQI o APsoQOL).
TratamientoEl tratamiento de la APso debe abordarse teniendo en cuenta los diferentes dominios que forman parte de esta enfermedad, ya que la afectación articular, cutánea, así como la entesitis, dactilitis y espondilitis pueden requerir abordajes terapéuticos distintos. Además, el grado de afectación de cada dominio resulta habitualmente diferente en cada paciente, por lo que el tratamiento de la APso deberá ser individualizado en cada caso5. En la decisión del abordaje terapéutico en cada momento también deberán considerarse los dominios de la enfermedad expresados por el paciente, que son la afectación funcional y de la calidad de vida relacionada con la enfermedad.
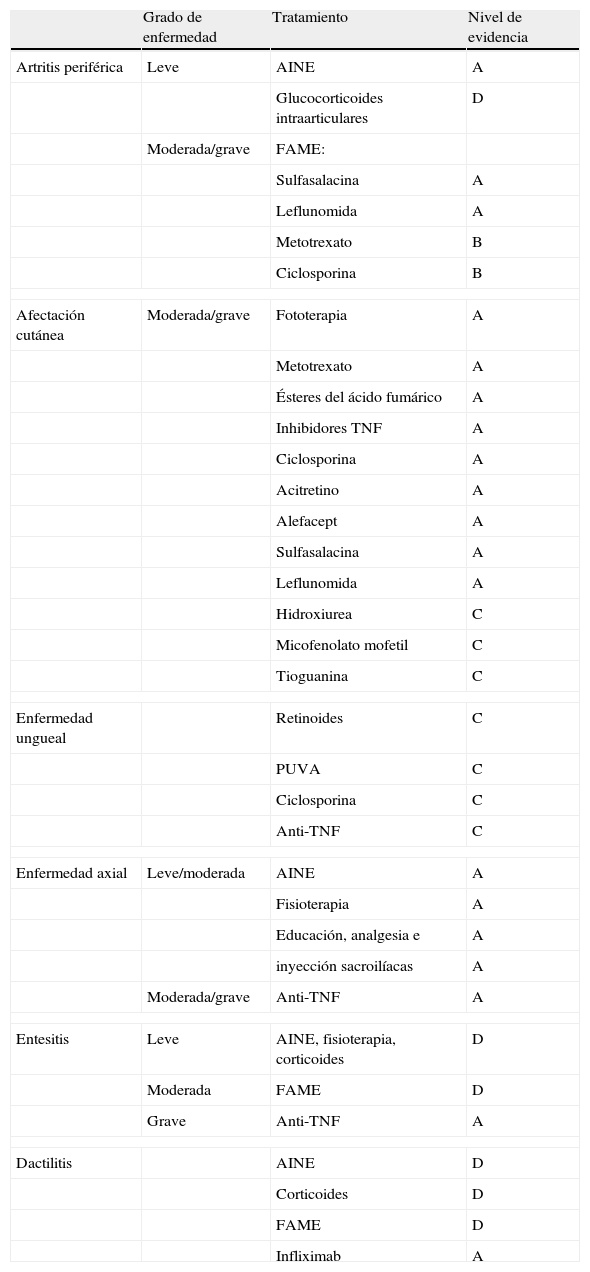
La tabla 3 muestra las recomendaciones de tratamiento según el GRAPPA4.
Recomendaciones de tratamiento según el GRAPPA
| Grado de enfermedad | Tratamiento | Nivel de evidencia | |
| Artritis periférica | Leve | AINE | A |
| Glucocorticoides intraarticulares | D | ||
| Moderada/grave | FAME: | ||
| Sulfasalacina | A | ||
| Leflunomida | A | ||
| Metotrexato | B | ||
| Ciclosporina | B | ||
| Afectación cutánea | Moderada/grave | Fototerapia | A |
| Metotrexato | A | ||
| Ésteres del ácido fumárico | A | ||
| Inhibidores TNF | A | ||
| Ciclosporina | A | ||
| Acitretino | A | ||
| Alefacept | A | ||
| Sulfasalacina | A | ||
| Leflunomida | A | ||
| Hidroxiurea | C | ||
| Micofenolato mofetil | C | ||
| Tioguanina | C | ||
| Enfermedad ungueal | Retinoides | C | |
| PUVA | C | ||
| Ciclosporina | C | ||
| Anti-TNF | C | ||
| Enfermedad axial | Leve/moderada | AINE | A |
| Fisioterapia | A | ||
| Educación, analgesia e | A | ||
| inyección sacroilíacas | A | ||
| Moderada/grave | Anti-TNF | A | |
| Entesitis | Leve | AINE, fisioterapia, corticoides | D |
| Moderada | FAME | D | |
| Grave | Anti-TNF | A | |
| Dactilitis | AINE | D | |
| Corticoides | D | ||
| FAME | D | ||
| Infliximab | A | ||
Aunque en líneas generales, las guías de tratamiento son similares en los diferentes países y se elaboran a partir de las guías de consenso internacionales, puede existir cierta variabilidad de acuerdo a los sistemas nacionales de salud de cada país.
Criterios actuales de la Sociedad Española de ReumatologíaEl consenso de la Sociedad Española de Reumatología (SER) propone utilizar los siguientes métodos de evaluación y criterios de actividad6.
Métodos de evaluación:- •
Afectación periférica: se recomienda el recuento de articulaciones dolorosas y tumefactas, la evaluación general por el médico y por el paciente, evaluación general del dolor, reactantes de fase aguda (VSG y/o PCR), función física (HAQ) y evaluación del daño estructural.
- •
Afectación axial: BASDAI.
- •
Entesitis: número y localización. MASES es el índice más aceptado para valorar la entesitis.
- •
Formas poliarticulares: los criterios APsoRC, ACR20, 50, 70 y DAS28 son los más ampliamente utilizados en ensayos clínicos pero no se utilizan de forma habitual en la práctica clínica. De estos, el más utilizado es el DAS28, aunque no evalúa las articulaciones interfalángicas distales ni las articulaciones de los pies. Se considera criterio de actividad un DAS28 ≥3,2 durante ≥3 meses.
- •
Formas oligoarticulares/entesitis (≤4 localizaciones): se considera criterio de actividad la artritis y/o entesitis en una o más localizaciones junto al menos una de las siguientes: a) valoración del estado de la enfermedad por el paciente ≥4cm, b) elevación de los reactantes de fase aguda (VSG y/o PCR) durante un periodo de ≥3 meses.
Según la SER, el objetivo terapéutivo consiste en lograr la remisión de la enfermedad, aunque esto solo se produce en un porcentaje muy bajo de pacientes. Por lo tanto, se considera aceptable conseguir en los pacientes con afectación poliarticular un DAS28 <2,6 (casi remisión) y en su defecto <3,2 (baja actividad). En las formas oligoarticulares el objetivo debería ser el de conseguir la desaparición de la inflamación de las articulaciones afectadas, y en su defecto, conseguir un número de articulaciones inflamadas <3, con una valoración por parte del paciente <4 y/o VSG o PCR normales.
Debe realizarse un replanteamiento terapéutico ante persistencia de la progresión radiológica, afectación aislada de interfalángicas proximales, distales (o cualquier otra localización) y/o entesitis que ocasionen importante deterioro funcional así como la persistencia de manifestaciones extraarticulares de la enfermedad, ya sea uveítis o afectación cutánea.
Indicaciones de terapia biológica en artritis psoriásicaAntes de emplear fármacos biológicos es necesario haber realizado un tratamiento correcto con un antiinflamatorio no esteroideo (AINE) y fármacos antirreumáticos modificadores de la enfermedad (FAME) para las formas articulares, e infiltraciones con corticoides intralesionales en las formas oligoarticulares, dactilitis o entesitis. Las pautas recomendadas para los FAME con eficacia documentada para el tratamiento de la APso son las siguientes:
- •
Metotrexato: 7,5mg/semana el primer mes. Aumentar a 15mg/semana al cabo de un mes si persiste la artritis y a 20–25mg/semanas al mes siguiente. Debe cambiarse el tratamiento al cabo de 2 meses si no hay respuesta terapéutica con esta dosis.
- •
Sulfasalazina: 2–3g/d durante al menos 3 meses.
- •
Leflunomida: 20mg/d durante 3 meses (10mg/d si intolerancia). Se puede realizar una dosis inicial de carga de 300mg repartidos en 100mg/día durante los 3 primeros días, seguido de la dosis de 20mg/día.
- •
Ciclosporina A: 3–5mg/kg/d durante 3 meses o la dosis máxima tolerada.
- •
Etanercept: 50mg s.c./semana que es igual de eficaz que 25mg dos veces a la semana, tanto para la artritis reumatoide como para la espondilitis anquilosante y la APso.
- •
Infliximab: 5mg/kg en infusión e.v. a las semanas 0,2 y 6 seguidas de infusiones cada 8 semanas7.
- •
Adalimumab: 40mg s.c. a semanas alternas.
Estos fármacos pueden usarse en monoterapia o asociarse con metotrexato, aunque no existe evidencia suficiente de que esta asociación aumente su eficacia o disminuya su toxicidad.
Estos tres fármacos anti-TNFα fueron aprobados en dermatología a partir de su uso en la APso. En general, todos muestran una eficacia similar en el tratamiento de la APso consiguiendo mejorías importantes en el PsARC, ARC y PASI. Aunque se cree que los anticuerpos monoclonales (infliximab y adalimumab) tienen una eficacia ligeramente superior a etanercept al inicio del tratamiento, los resultados al cabo de un año de tratamiento son equivalentes. En cuanto a la pérdida de eficacia a lo largo del tiempo de tratamiento también es similar en los tres.
Así pues, en todos los dominios clínicos de la APso, excepto en la dactilitis, pueden usarse alternativamente infliximab, adalimumab o etanercep. De estos, aunque se ha descrito la respuesta al tratamiento con todos ellos, el único aprobado para ser utilizado en tratamiento de la dactilitis es infliximab a las dosis anteriormente descritas8–10.
Terapias emergentes- •
Golimumab: anti-TNF de administración subcutánea mensual que ha mostrado beneficios significativos en los diferentes dominios clínicos de la APso11,12.
- •
Abatacept (CTLA4-Ig): se une al receptor de células presentadoras de antígeno CD80/86 bloqueando la interacción de células T con CD28. Se desconoce su eficacia en APso.
- •
Denosumab: inhibidor de la osteoclastogénesis. Es un inhibidor del ligando RANK11. Su indicación podría estar dirigida a evitar o reducir la presencia de osteoporosis.
- •
Certolizumab pegol: primer anti-TNF-α pegilado.
Recientemente se han propuesto los criterios de definición de actividad mínima de la APso, los cuales suponen el objetivo de los tratamientos actuales para la enfermedad y también una herramienta útil para comparar terapias en ensayos clínicos13. Cualquier criterio de medida de la actividad de la APso debe comprender la evaluación de los diferentes aspectos que incluye, es decir, la evaluación de la afectación articular periférica, la entesitis, la dactilitis y la espondilitis, así como la alteración funcional y los aspectos relacionados con la calidad de vida del paciente. Según la OMERACT los parámetros que deben ser objeto de evaluación para determinar la actividad de la APso son: la actividad articular periférica, la actividad cutánea, el dolor, la evaluación global del paciente, la función física y la calidad de vida.
Se considera que un paciente ha alcanzado la actividad mínima de la enfermedad cuando cumple 5 de los 7 criterios siguientes:
- 1.
Número de articulaciones dolorosas ≤1.
- 2.
Número de articulaciones inflamadas ≤1.
- 3.
PASI≤1 o BSA≤3.
- 4.
Dolor escala analógica visual (VAS) ≤15.
- 5.
Actividad global valorada por el paciente ≤20.
- 6.
HAQ ≤0,5.
- 7.
Puntos de entesitis ≤1.
La definición de remisión clínica en la APso todavía no está del todo establecida ni existe acuerdo entre los diferentes autores. Para algunos puede referirse a la ausencia de actividad de la enfermedad en lo que se refiere a signos y síntomas de esta, mientras otros pueden definirla como la ausencia de actividad en todos los dominios de la enfermedad. Para poder enunciar una definición adecuada de la remisión es necesario tener en cuenta la enfermedad subclínica que puede persistir en algunos pacientes, las consecuencias de esta enfermedad y la calidad de vida del paciente en cada momento, además de disponer de los instrumentos de medida de los diferentes dominios de la APso8. Mientras el 20% de los pacientes con APso evolucionan hacia formas destructivas e incapacitantes de la enfermedad, otros pacientes alcanzan la remisión. Según Gladman14, el concepto de remisión se define como la ausencia de articulaciones inflamadas activas durante 12 meses, y según sus resultados, esto se produce en aproximadamente el 17,6% de los casos. Este estudio fue realizado en pacientes con APso que fueron seguidos longitudinalmente durante 20 años. Gladman apunta también que la media del tiempo de remisión es de 2,6 años y que el 52% de los pacientes vuelven a presentar una reactivación de la enfermedad después de este período de remisión.
ConclusionesLa APso suele aparecer en pacientes diagnosticados previamente de psoriasis que acuden de forma regular al dermatólogo para el control de la enfermedad cutánea. Por otro lado, la afectación articular requiere el diagnóstico y tratamiento precoz para evitar la progresión del daño articular. Por tanto, es importante que el dermatólogo conozca esta enfermedad y las herramientas necesarias para detectarla, así como que sepa en qué momento debe realizar la interconsulta al reumatólogo para ofrecer al paciente la mejor opción disponible para el adecuado control de su enfermedad.
Desde la aplicación de los criterios CASPAR para la clasificación de la APso, el dermatólogo ha pasado a ocupar un papel importante en el diagnóstico y manejo de la APso, ya que dos de los criterios menores en consisten en la detección de enfermedad cutánea activa y en saber reconocer las características clínicas de la afectación ungueal. Además, el concepto actual de objetivo terapéutico para la APso supone la mejora de todos los dominios clínicos de la enfermedad, incluyendo la forma cutánea. Así, el papel del dermatólogo en el manejo de la APso es importante, tanto en el diagnóstico como en el seguimiento de la enfermedad además de para conseguir un tratamiento óptimo.
En relación al papel del reumatólogo, éste es imprescindible para la elaboración y aplicación de medidas de actividad de la mayoría de dominios clínicos de la enfermedad, ya que el mejor conocimiento de la APso permitirá el acceso de un mayor número de pacientes al tratamiento de forma precoz, consiguiendo así detener la progresión de la enfermedad.
Con este fin, la creación de unidades de tratamiento multidisciplinar para el abordaje de la psoriasis y la APso que incluyan a especialistas conocedores de los diferentes aspectos y comorbilidades de esta enfermedad sería muy importante para ofrecer las mejores opciones terapéuticas y un óptimo control en la enfermedad de estos pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses en relación con este artículo.