La psoriasis es una afección crónica de la piel que afecta aproximadamente el 1-3% de la población mundial con gran impacto negativo en la calidad de vida de los pacientes. Sin embargo, aún no se ha determinado en qué medida la ubicación específica en el cuerpo de las lesiones psoriasis influye en la calidad de vida.
MétodoSe realizó una revisión sistemática con una búsqueda en las bases de datos Medline, Embase y Web of Science. En la revisión se descartaron los artículos referidos a casos clínicos y revisiones, incluyéndose solo aquellos en los que se indicó de forma explícita la evaluación por regiones corporales afectadas por psoriasis.
ResultadosNo pudo identificarse una relación entre la presencia de placas de psoriasis en diferentes áreas del cuerpo y la calidad de vida de los pacientes.
ConclusionesSi bien la evidencia es limitada y presenta resultados no estandarizados, los resultados de esta revisión permiten indicar que la presencia de placas de psoriasis disminuye la calidad de vida de los pacientes, sin diferencias en función de la región afectada.
Psoriasis is a chronic skin condition that affects approximately 1–3% of the world's population and is known to decrease patients’ quality of life. However, it is yet to be ascertained whether the specific location of psoriatic lesions on the body influences one's quality of life.
MethodsA systematic review was conducted with a search of MEDLINE, EMBASE, and Web of Science databases. Only non-case report and non-review studies with explicitly stated body regions affected by psoriasis were included in the review.
FindingsPsoriatic patches and plaques in different areas of the body were not found to influence patients’ quality of life to differing extents.
ConclusionsWhile the body of evidence is limited and presents unstandardized results, the results of this review point to the fact that all psoriatic patches and plaques decrease patients’ quality of life, with neither one region doing so to a significantly greater extent than another.
La psoriasis vulgar es una enfermedad sistémica inflamatoria crónica, que estará mediada por el sistema inmunitario y que afecta al 1-3% de la población mundial.1 A menudo se asociará con la presencia de pápulas, parches y placas descamativas, las cuales pueden presentarse en cualquier parte del cuerpo2. Si bien se sabe que la psoriasis afecta de forma negativa a la calidad de vida de los pacientes, se conoce poco sobre la relación entre la región o las regiones del cuerpo afectadas) por la psoriasis y la calidad de vida3. El objetivo de la presente revisión sistemática fue determinar si la región del cuerpo afectada por la psoriasis estará relacionada con la calidad de vida de los pacientes. De acuerdo con la hipótesis planteada en el presente estudio, las áreas con psoriasis que son más visibles o sensibles (cara, cuello, genitales) se asociarán con una peor calidad de vida en comparación con aquellas localizaciones menos visibles, como, por ejemplo, los muslos o el tronco.
MétodosSe realizó una búsqueda bibliográfica en MEDLINE, EMBASE y la base de datos bibliográfica de la Web of Science utilizando los términos («psoriasis» AND (cara O facial O cuero cabelludo O oreja O mejilla* O labios O labio O lóbulo de la oreja* O frente O párpado* O nariz O barbilla O mandíbula O cuello O Hombro* O pecho O mama* O antebrazo* O axila O brazo O codo* O muñeca* O mano* O dedo* O uña* O abdomen O estómago O cadera O caderas O espalda O tronco O glúteos* O pierna O piernas O muslo* O rodilla* O rótula* O tobillo* O espinilla* O pantorrilla* O pantorrillas O dedo del pie O dedos de los pies O plantar O pie O pies O miembro* O Genital* O vulva * O labios genitales* O ingle O vagina* O ingle O pene O pene O escroto O pubis O «psoriasis inversa”) Y («Índice de calidad de vida en dermatología» O «DLQI» O «Skindex 29» O «Skindex 17» O «Escala de calidad de vida dermatológica» O «DQOLS» O «Índice de discapacidad por psoriasis» O «PDI» O «Cuestionario de impacto de la psoriasis» O «IPSO» O «Índice de psoriasis de calidad de vida» O «escala de calidad de vida» O «QOLS» O «PSORIQoL» O «SF36» O «EQ5D» O MQOL O «Escala de calidad de vida de McGill» O HRQOL O «Calidad de vida relacionada con la salud» O WHOQOL-BREF O «Escala de calidad de vida global» O GQOL) Y adulto).
Los artículos incluidos cumplieron con los siguientes criterios: haber mencionado la partes específicas del cuerpo afectadas por la psoriasis, haber descrito la calidad de vida de los pacientes con psoriasis y finalmente haber sido publicados antes del 14 de febrero del 2021. Aquellos estudios en los que las puntuaciones de la calidad de vida de los pacientes se relacionaban con más de una localización corporal de psoriasis fueron excluidos, por ejemplo, si los pacientes tenían múltiples áreas del cuerpo afectadas y si la puntuación de la calidad de vida hacía referencia a todas esas diferentes áreas. Además, se excluyeron los artículos si los estudios eran actas de congresos, si no mencionaban en qué parte del cuerpo los pacientes experimentaban psoriasis, si eran revisiones o metaanálisis y si eran informes de casos.
Escalas de calidad de vidaA pesar de que la estrategia de búsqueda incluía una amplia gama de diversas escalas de calidad de vida, la que se describió con mayor frecuencia en los estudios incluidos fue la del DLQI4-6.
El Dermatology Life Quality Index (DLQI) es un cuestionario de 10 elementos que se utiliza para evaluar el impacto en la calidad de vida y la discapacidad asociada con enfermedades cutáneas. Este cuestionario trata sobre los diversos aspectos de la vida de una persona, incluido el impacto de la enfermedad cutánea en los síntomas, en la autopercepción, en las actividades, en las relaciones y en el tratamiento. Los pacientes indican cuánto esta afectará su vida en cada sector, con las siguientes posibles respuestas: «muchísimo», «mucho», «poco» y «nada». La respuesta se puntúa en una escala de 0 a 3 y se suma para obtener una puntuación total de un máximo de 30 puntos. Así, una puntuación más alta de DLQI indica un mayor deterioro de la calidad de vida.
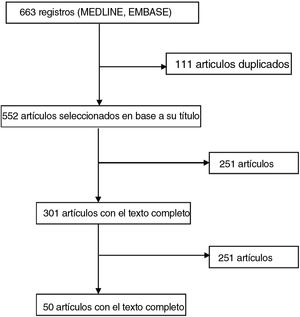
ResultadosSe identificaron un total de 663 citas relevantes a partir de la búsqueda bibliográfica (fig. 1)7. De estas, 251 se excluyeron en función del título y el resumen y 301 se seleccionaron para una evaluación más detallada. En esta revisión se incluyeron un total de 50 artículos8-57. Consulte el anexo 2 Apéndice B, tabla 1 (material complementario) para obtener un resumen de los estudios incluidos.
Dado que los estudios utilizaron diferentes escalas para cuantificar la calidad de vida de los pacientes, no fue posible recopilar y hacer un promedio de los resultados obtenidos en todos los estudios. Por lo tanto, se tomaron en cuenta los resultados de los estudios que utilizaron la misma escala de calidad de vida. Por ejemplo, los estudios cuyos resultados se basaron en el DLQI se analizaron con estudios similares, mientras que los estudios cuyos resultados se basaron en el EQ-5D se agruparon de manera similar.
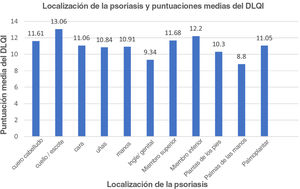
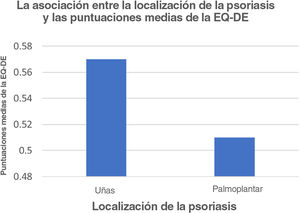
Para la representación gráfica y el análisis estadístico, cada localización corporal con psoriasis se tenía que corresponder con al menos 2estudios para poder ser incluida en el análisis y de esta manera evitar que los resultados de uno de los estudios sesgaran el análisis. Teniendo en cuenta esta metodología, la escala de calidad de vida utilizada con mayor frecuencia fue el DLQI, seguido del EQ-5D, como se muestra en las figuras 2 y 3.
En cuanto a las otras escalas de calidad de vida, como es el caso del cuestionario de Finlay-Kahn Modificado o el PDI, no se contó con suficientes estudios para la realización de un modelo gráfico y para el análisis estadístico. Sin embargo, los resultados de estos estudios se recogieron en el anexo 2 Apéndice B, tabla 1, material complementario.
Inicialmente, de manera visual, en la figura 2 se observa que las lesiones de psoriasis localizadas en la región del cuello/escote se asocian con puntuaciones del DLQI más elevadas (disminución de la calidad de vida) en comparación con aquellas lesiones de psoriasis localizadas en las palmas, por ejemplo. Para poder determinar si las diferencias observadas en cuanto a la calidad de vida entre las áreas corporales con lesiones de psoriasis son realmente significativas, se utilizó la prueba de ANOVA de una vía. Los resultados de la prueba de ANOVA demostraron que las puntuaciones medias del DLQI entre todas las regiones del cuerpo afectadas por la psoriasis no presentaron diferencias de manera significativa.
Para poder determinar si los resultados observados en la figura 3 presentaban diferencias de manera significativa, se utilizó la prueba de la t de Student. El resultado de esta prueba señaló que las puntuaciones medias del EQ-5D de las lesiones de psoriasis localizadas en el área ungueal y palmoplantar no fueron significativamente diferentes.
DiscusiónSi bien la hipótesis inicial del presente estudio sugería que las áreas con psoriasis más visibles o sensibles, como es el caso de la cara, el cuello y los genitales, se asociarían de manera significativa con una peor calidad de vida, sobre todo en comparación con aquellas zonas menos visibles o sensibles. Sin embargo, esta hipótesis no ha podido ser corroborada en el presente estudio. De hecho, no se ha evidenciado que ninguna localización específica del cuerpo se asocie con un empeoramiento significativo de la calidad de vida en comparación con otra localización. En esta revisión se analizaron de manera específica las puntuaciones iniciales de la calidad de vida de los pacientes según la localización corporal afectada con psoriasis, en lugar de evaluar la mejoría de la calidad de vida tras algún tratamiento. Esto se hizo para así evitar este factor de confusión.
Los resultados del presente estudio se han podido ver afectados por las limitaciones que suponen el haber realizado una revisión sistemática. Por un lado, en algunos de los estudios se describió la asociación entre la calidad de vida y la afectación ciertas áreas corporales, en lugar de describir la asociada con regiones corporales de forma aislada. Esto dificultó el poder determinar en qué medida el deterioro de la calidad de vida se debía a la afectación por psoriasis de una región específica únicamente. Además, los estudios incluidos en esta revisión utilizaron diferentes escalas de calidad de vida, lo que dificultó el comparar tanto los resultados de los estudios, así como la combinación de estos, lo que hubiera permitido realizar un análisis más profundo. Esto hizo con que el número de estudios incluidos en el análisis sea menor, lo que a su vez también puede haber sesgado los resultados. Por lo tanto, en los próximos estudios se recomienda que se utilicen únicamente las escalas que son usadas de manera cotidiana. Además, existe la limitación inherente de las escalas de calidad de vida, ya que suelen ser subjetivas. Una limitación metodológica de esta revisión es que un único revisor realizó la extracción y la revisión de los datos, lo que limita la confiabilidad entre los evaluadores de la selección del estudio. Finalmente, esta revisión está limitada por el hecho de que los estudios incluidos fueron estudios observacionales y ensayos controlados, lo que implica diversos grados de control de variables y de sesgos. Sin embargo, sin esta limitación metodológica, el tamaño de la evidencia sería insuficiente para realizar un análisis estadístico, por lo que se trata de una limitación necesaria.
Algunas de las fortalezas de este estudio incluyen el hecho de que se realizó una búsqueda amplia, con una revisión exhaustiva de los estudios, así como el uso de múltiples bases de datos para la búsqueda. Además, el análisis estadístico permitió llegar a conclusiones más sólidas.
Futuros estudios que incluyan un mayor tamaño muestral son necesarios; en estos además sería interesante que se incluyan pacientes con la afectación de una única localización (p. ej., psoriasis localizada únicamente en el cuero cabelludo); de esta forma, se podría determinar si realmente existe una relación directa entre la zona del cuerpo afectada y la calidad de vida de los pacientes. Por otro lado, los estudios deberían utilizar las escalas de calidad de vida que son utilizadas con mayor frecuencia, como es el caso del DLQI, y así permitir una mejor comparación entre los estudios incluidos. Finalmente, en próximos estudios, también se podría explorar en qué medida el tratamiento de aquellas zonas específicas podría mejora la calidad de vida, y si la calidad de vida asociada a ciertas localizaciones del cuerpo mejora de manera más significativa, si se compara con otras localizaciones afectadas por psoriasis. Por otro lado, en futuros estudios se podrían incluir más parámetros, como, por ejemplo, el área de la piel afectada por la psoriasis y los puntajes de calidad de vida correspondientes, para así determinar si las áreas más extensas de la piel también desempeñan un papel importante que pueda afectar la calidad de vida de los pacientes. Quizás el área de la piel afectada por la psoriasis sea otra variable de confusión en la relación que existe entre las localizaciones con psoriasis y la calidad de vida.
ConclusionesHasta donde sabemos, esta revisión sistemática es la primera en utilizar datos internacionales con la finalidad de determinar si afectación de una localización específica del cuerpo por psoriasis estará relacionada con el grado de deterioro de la calidad de vida de los pacientes. Los resultados de esta revisión demuestran que cualquier localización disminuirá la calidad de vida de los pacientes, sin que exista la evidencia de que una región corporal específica la afecte de manera significativamente mayor que otra localización.
A pesar de no haber podido confirmar la hipótesis planteada inicialmente, los resultados de esta revisión siguen siendo de gran utilidad, ya que permiten arrojar luz sobre el hecho de que los pacientes con psoriasis tienen una disminución de calidad de vida independientemente de la localización de las lesiones de psoriasis. Este hecho ayuda a resaltar la importancia de que los pacientes con psoriasis reciban una atención integral, lo cual permitirá anticiparse a una disminución de la calidad de vida, ya sea mediante un tratamiento más oportuno, el derivar al paciente a un especialista en psicoterapia o a grupos de apoyo para pacientes.
Esta revisión también ayuda a los pacientes a comprender que ninguna localización afectada por la psoriasis predice una calidad de vida significativamente «mejor» o «peor» que otra; todas las localizaciones con psoriasis se relacionaran con una disminución de la calidad de vida.
Para más información ver Anexo 1.
Conflicto de interesesDr. Vender ha recibido:
- –
Becas/apoyo a la investigación: Abbvie, Amgen, Bausch Health, Centocor, Dermira, Dermavant, Galderma, GSK, Leo, Lilly, Takeda, Novartis, Merck, Pfizer, Regeneron, UCB.
- –
Ha participado en Buró de oradores y ha recibido honorarios de: Abbvie, Amgen, Janssen, Galderma, GSK, Leo, Lilly, Merck, Novartis, Pfizer, Bausch-Health, Actelion, Celgene, Cipher, UCB.
- –
Ha recibido honorarios por consultoría: Abbvie, Amgen, BMS, Janssen, Galderma, GSK, Leo, Lilly, Merck, Novartis, Palladin, Pfizer, Bausch-Health, Actelion, Celgene, Cipher, UCB.