En los últimos años, el trasplante de progenitores hematopoyéticos (TPH) ha revolucionado el tratamiento de diversas enfermedades hematológicas y no hematológicas. Su realización no está exenta de riesgos y conlleva una tasa significativa de complicaciones, entre ellas mucocutáneas. Presentamos una revisión narrativa de las alteraciones mucocutáneas observadas tras TPH. Entre ellas, destacan la enfermedad de injerto contra receptor (EICR) aguda y crónica, cuyo diagnóstico y tratamiento pueden ser notoriamente complejos. Otras patologías frecuentes son las toxicodermias y las infecciones con afectación mucocutánea. Además, diversos estudios muestran que estos individuos pueden tener una mayor tasa de neoplasias mucocutáneas. La identificación y manejo temprano de estas complicaciones, junto con un enfoque multidisciplinar, son esenciales para mejorar la calidad de vida y los resultados a largo plazo de estos pacientes. Asimismo, es recomendable el cribado de cáncer cutáneo en estos individuos, especialmente si presentan otros factores de riesgo.
In recent years, hematopoietic stem cell transplantation (HSCT) has revolutionized the treatment of various hematological and non-hematological diseases. Its implementation is not stranger to risks and involves a significant rate of complications, including mucocutaneous adverse events. We present a narrative review of the mucocutaneous alterations observed after HSCT. Among these, acute and chronic graft-versus-host disease (GVHD) stand out, whose diagnosis and treatment can be challenging. Other common conditions include cutaneous adverse reactions and infections with mucocutaneous involvement. Additionally, various studies indicate that these individuals may have a higher rate of mucocutaneous neoplasms. Early identification and management of these complications, along with a multidisciplinary approach, are essential to improving these patients’ quality of life and long-term outcomes. Furthermore, it is advisable to screen for skin cancer in these individuals, especially if they have other associated risk factors.
El trasplante de progenitores hematopoyéticos (TPH), que incluye el trasplante de médula ósea, de sangre periférica y de sangre de cordón umbilical, implica la administración de células madre hematopoyéticas sanas a pacientes con médula ósea disfuncional secundaria a enfermedades hematológicas malignas, insuficiencias medulares e inmunodeficiencias graves. El TPH puede ser autólogo o alogénico, según las células hematopoyéticas procedan del propio paciente o de otra persona, respectivamente. En la actualidad, se ha consolidado como el tratamiento de elección en diversas enfermedades hematológicas malignas y no malignas graves1. Según datos de la Organización Nacional de Trasplantes (ONT), en España en el año 2022 se realizaron más de 3.500 TPH, número que duplica los realizados en el año 20022.
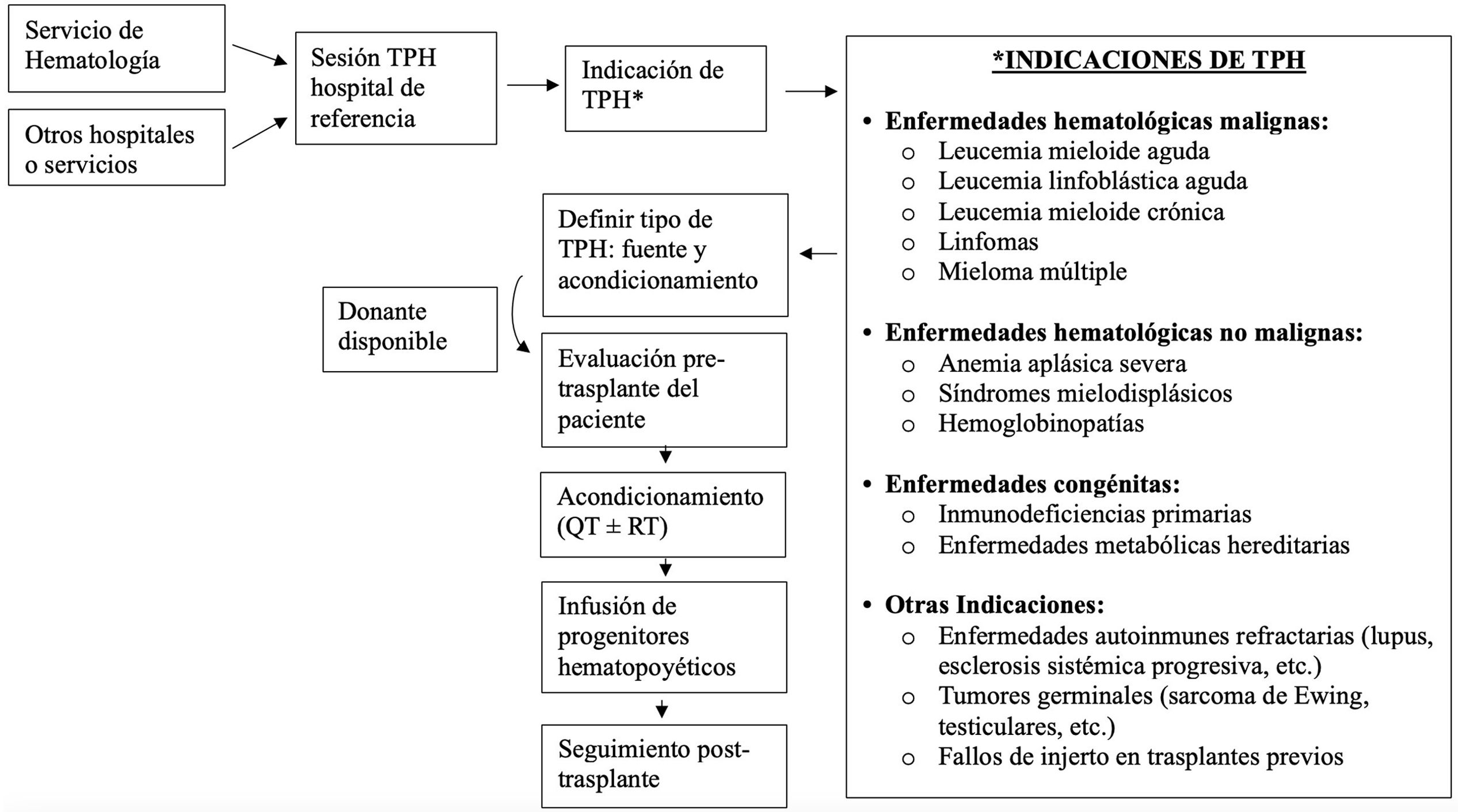
El TPH incluye una fase de acondicionamiento, donde se administra quimioterapia y/o radioterapia para preparar la médula ósea del receptor y eliminar las células neoplásicas (fig. 1). Uno o 2 días después, se realiza la fase de infusión. Posteriormente, el paciente entra en el periodo de aplasia, donde su inmunidad cae significativamente debido a la falta de producción de células sanguíneas por la médula ósea. Es una etapa crítica donde puede experimentar anemia severa, hemorragias e infecciones. Finalmente, ocurre la fase de injerto, que comienza cuando los progenitores empiezan a producir nuevas células en la médula. El tiempo de injerto varía según el tipo de trasplante y las condiciones del paciente, oscilando entre 11 y 40 días3.
Tras la realización del TPH, los individuos pueden presentar múltiples complicaciones mucocutáneas derivadas del propio trasplante, de la inmunosupresión recibida para el trasplante o del efecto de las células del injerto sobre el receptor. Un estudio reciente señaló que hasta el 45% de los individuos sometidos a TPH experimentaban algún tipo de erupción cutánea en el primer año post-TPH, porcentaje que se eleva hasta el 60-70% a largo plazo. Estas complicaciones pueden afectar considerablemente la calidad de vida de estos pacientes e, incluso, poner en riesgo su vida4. En este artículo revisaremos las alteraciones mucocutáneas observadas en pacientes sometidos a TPH, enfatizando en la enfermedad injerto contra receptor (EICR) aguda y crónica, las toxicodermias, las infecciones y las neoplasias mucocutáneas.
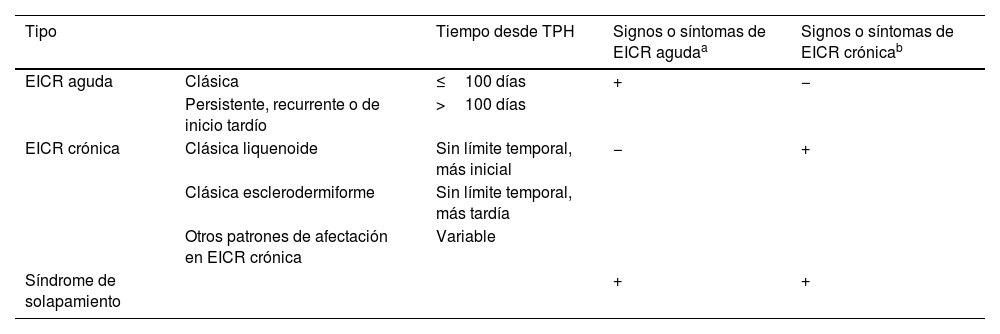
Enfermedad injerto contra receptor tras trasplante de progenitores hematopoyéticosEn la EICR, o enfermedad injerto contra huésped, las células inmunitarias del injerto (el trasplante) reconocen al receptor (el paciente) como extraño y atacan sus tejidos. La EICR se clasifica en aguda (EICR-A) y crónica (EICR-C). Clásicamente se distinguían por presentarse antes o después de los 100 días post-TPH, pero la clasificación actual las diferencia en función de sus distintos mecanismos fisiopatológicos y de su presentación clínica (tabla 1)5-7. La EICR puede afectar a cualquier órgano, aunque la piel y mucosas son los más frecuentemente afectados (20-70%), y su compromiso puede ayudar al diagnóstico. Es una complicación intrínseca al TPH alogénico (alo-TPH), al ser células diferentes al receptor, y contribuye significativamente a su morbimortalidad, siendo la causa de muerte más común después de la recidiva de la neoplasia hematológica que motivó el TPH6.
Clasificación de la EICR
| Tipo | Tiempo desde TPH | Signos o síntomas de EICR agudaa | Signos o síntomas de EICR crónicab | |
|---|---|---|---|---|
| EICR aguda | Clásica | ≤100 días | + | − |
| Persistente, recurrente o de inicio tardío | >100 días | |||
| EICR crónica | Clásica liquenoide | Sin límite temporal, más inicial | − | + |
| Clásica esclerodermiforme | Sin límite temporal, más tardía | |||
| Otros patrones de afectación en EICR crónica | Variable | |||
| Síndrome de solapamiento | + | + |
EICR: enfermedad injerto contra receptor; TPH: trasplante de progenitores hematopoyéticos.
Fuente: adaptado de Jagasia et al.5 y Ballester-Sánchez et al.7.
Signos o síntomas de EICR crónica: piel (patrón esclerodermiforme, liquenoide u otros), boca (síndrome seco, liquenoide, erosivo u otros), genital (síndrome seco, liquenoide, erosivo u otros), gastrointestinal (diarrea crónica, dolor abdominal, disfunción hepática), pulmonar (bronquiolitis obliterante), muscular, articular, nervioso (neuropatía periférica o central), etc.
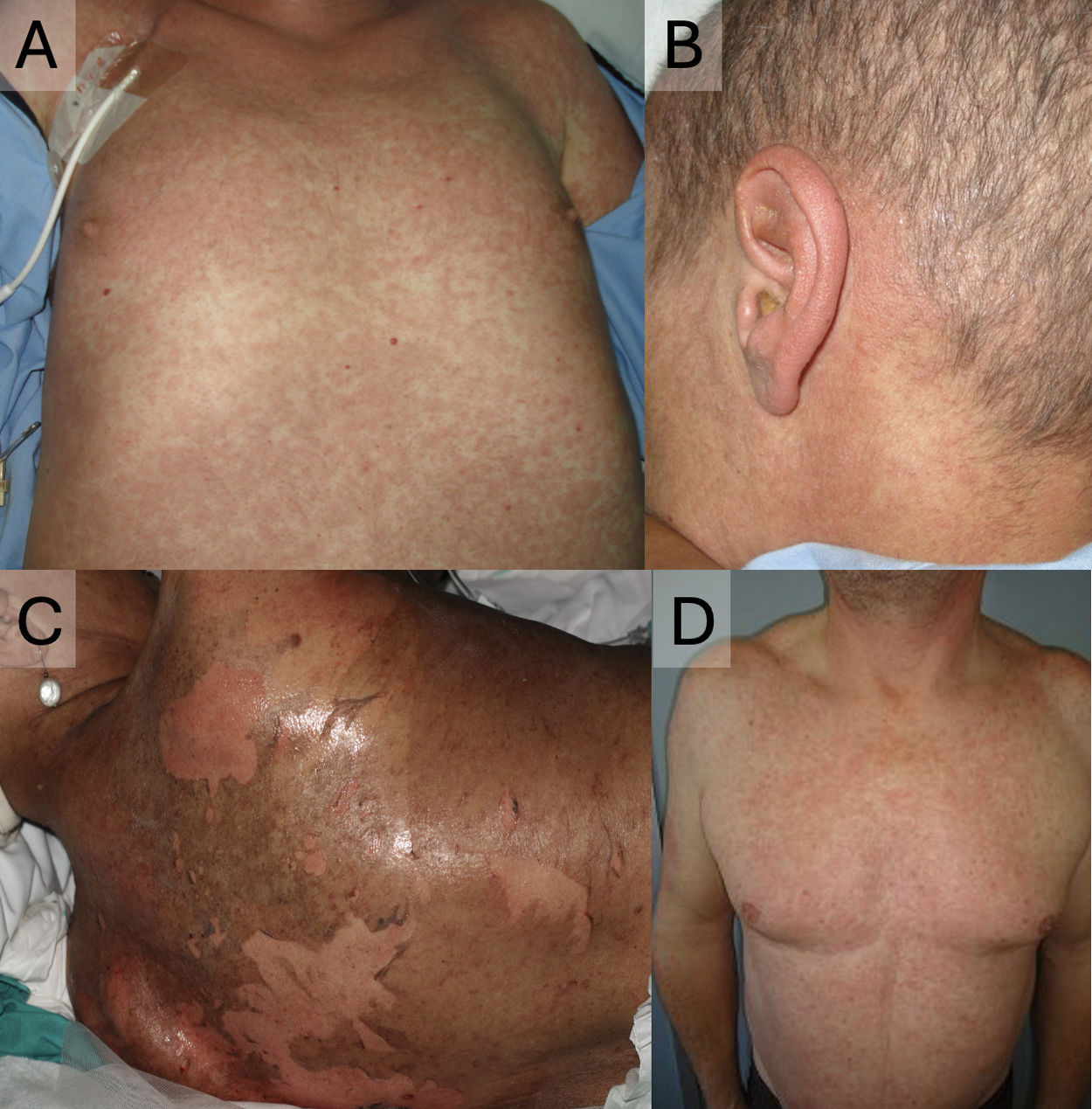
La EICR-A frecuentemente afecta primero a la piel y las mucosas. Los siguientes órganos comprometidos son el hígado y el intestino, y la tríada característica de la EICR-A incluye exantema cutáneo, hiperbilirrubinemia y diarrea. Clásicamente aparece y cede en los primeros 100 días post-TPH (se desarrolla frecuentemente 30 a 40 días post-TPH). Sin embargo, puede presentarse después de los 100 días (forma de inicio tardío), ser persistente (durar más de 100 días) o recurrente (desaparecer antes de los 100 días y reaparecer tras los 100 días)7. Se gradúa en 4 estadios: estadio 1 (+), con<25% de la superficie corporal total (SCT) afectada; estadio 2 (++): 25-50% de la SCT; estadio 3 (+++): 50-75% de la SCT; y estadio 4 (++++): >75% de la SCT7. La presentación cutánea (fig. 2) suele comenzar con disestesias, prurito, eritema o edema, que progresa a un exantema morbiliforme, muchas veces de apariencia foliculotropa y de predominio en el tronco, para de manera progresiva y confluente, comprometer de forma centrífuga al resto del cuerpo. Es típica la afectación de áreas palmo-plantares y retroauriculares. En casos graves, pueden formarse ampollas por despegamiento dermoepidérmico. Las mucosas oral, genital, nasal y ocular pueden estar afectadas, presentándose como mucositis8.
EICR cutánea aguda. A. Exantema maculopapular afectando a tronco, con predominio folicular. B. Afectación retroauricular, característica de la enfermedad. C. Despegamiento epidérmico en un paciente con EICR aguda grado 4. D. Exantema maculopapular afectando a tronco, con predominio folicular. Este paciente fue finalmente diagnosticado de toxicodermia a piperacilina-tazobactam. Nótese la dificultad en el diagnóstico diferencial con la EICR, siendo un caso muy similar al paciente de A.
La sospecha inicial de EICR-A se establece por la clínica: tríada de exantema, diarrea e hiperbilirrubinemia, si bien pueden no estar los 3 signos presentes o afectar a otros órganos. La biopsia cutánea no es patognomónica. Se puede clasificar histológicamente a la EICR-A en grado I, donde se aprecian cambios focales vacuolares a nivel de la membrana basal epidérmica, con infiltrado linfocitario escaso en dermis superficial. En el grado II, destaca la necrosis de queratinocitos con cambios vacuolares más evidentes. En el grado III, se observa apoptosis de queratinocitos, con borramiento de la unión dermoepidérmica y un infiltrado liquenoide en dermis papilar. En el grado IV, la necrosis epidérmica es total, con separación dermoepidérmica9.
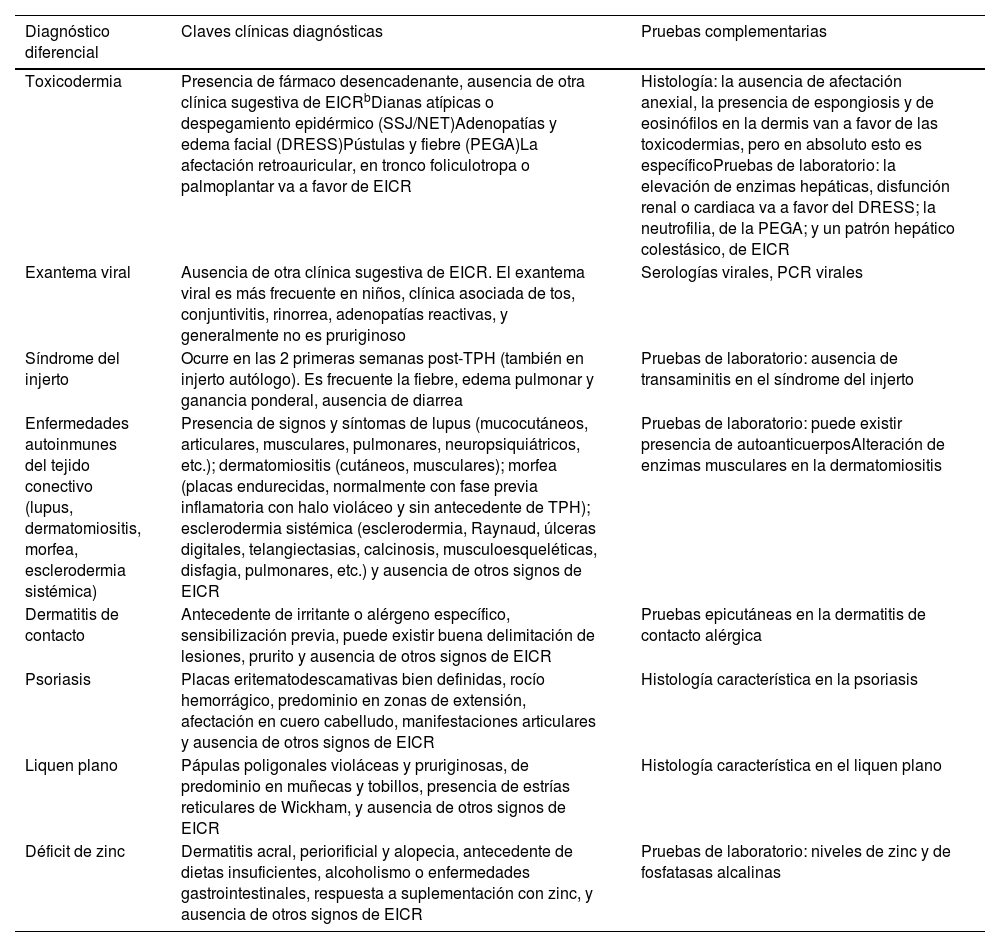
El diagnóstico diferencial de la EICR puede ser muy complejo (tabla 2, fig. 2). El exantema presente en las toxicodermias y en las infecciones virales puede ser idéntico al de la EICR-A. En este contexto, la asociación de diarrea e hiperbilirrubinemia apoya el diagnóstico de EICR-A; el antecedente de introducción de un nuevo fármaco el de toxicodermia; y la clínica a nivel respiratorio superior u otros signos/síntomas, así como la positividad de serologías o de la reacción de polimerasa en cadena (PCR) a las infecciones virales5,8,10. A nivel histológico, diversos autores han sugerido que un infiltrado escaso en eosinófilos y la ausencia de espongiosis en la EICR-A podría ayudar a diferenciarla de las toxicodermias11,12. Asimismo, se ha intentado encontrar marcadores específicos de EICR a nivel inmunohistoquímico, especialmente la expresión elafina13 o, más recientemente, la expresión de diversos microRNA14. Sin embargo, es necesario validar estos marcadores y, en ocasiones, pese a un estudio exhaustivo, no se alcanza un diagnóstico certero de EICR-A.
Diagnóstico diferencial de las manifestaciones mucocutáneas de la EICR agudaa
| Diagnóstico diferencial | Claves clínicas diagnósticas | Pruebas complementarias |
|---|---|---|
| Toxicodermia | Presencia de fármaco desencadenante, ausencia de otra clínica sugestiva de EICRbDianas atípicas o despegamiento epidérmico (SSJ/NET)Adenopatías y edema facial (DRESS)Pústulas y fiebre (PEGA)La afectación retroauricular, en tronco foliculotropa o palmoplantar va a favor de EICR | Histología: la ausencia de afectación anexial, la presencia de espongiosis y de eosinófilos en la dermis van a favor de las toxicodermias, pero en absoluto esto es específicoPruebas de laboratorio: la elevación de enzimas hepáticas, disfunción renal o cardiaca va a favor del DRESS; la neutrofilia, de la PEGA; y un patrón hepático colestásico, de EICR |
| Exantema viral | Ausencia de otra clínica sugestiva de EICR. El exantema viral es más frecuente en niños, clínica asociada de tos, conjuntivitis, rinorrea, adenopatías reactivas, y generalmente no es pruriginoso | Serologías virales, PCR virales |
| Síndrome del injerto | Ocurre en las 2 primeras semanas post-TPH (también en injerto autólogo). Es frecuente la fiebre, edema pulmonar y ganancia ponderal, ausencia de diarrea | Pruebas de laboratorio: ausencia de transaminitis en el síndrome del injerto |
| Enfermedades autoinmunes del tejido conectivo (lupus, dermatomiositis, morfea, esclerodermia sistémica) | Presencia de signos y síntomas de lupus (mucocutáneos, articulares, musculares, pulmonares, neuropsiquiátricos, etc.); dermatomiositis (cutáneos, musculares); morfea (placas endurecidas, normalmente con fase previa inflamatoria con halo violáceo y sin antecedente de TPH); esclerodermia sistémica (esclerodermia, Raynaud, úlceras digitales, telangiectasias, calcinosis, musculoesqueléticas, disfagia, pulmonares, etc.) y ausencia de otros signos de EICR | Pruebas de laboratorio: puede existir presencia de autoanticuerposAlteración de enzimas musculares en la dermatomiositis |
| Dermatitis de contacto | Antecedente de irritante o alérgeno específico, sensibilización previa, puede existir buena delimitación de lesiones, prurito y ausencia de otros signos de EICR | Pruebas epicutáneas en la dermatitis de contacto alérgica |
| Psoriasis | Placas eritematodescamativas bien definidas, rocío hemorrágico, predominio en zonas de extensión, afectación en cuero cabelludo, manifestaciones articulares y ausencia de otros signos de EICR | Histología característica en la psoriasis |
| Liquen plano | Pápulas poligonales violáceas y pruriginosas, de predominio en muñecas y tobillos, presencia de estrías reticulares de Wickham, y ausencia de otros signos de EICR | Histología característica en el liquen plano |
| Déficit de zinc | Dermatitis acral, periorificial y alopecia, antecedente de dietas insuficientes, alcoholismo o enfermedades gastrointestinales, respuesta a suplementación con zinc, y ausencia de otros signos de EICR | Pruebas de laboratorio: niveles de zinc y de fosfatasas alcalinas |
DRESS: drug reaction with eosinophilia and systemic symptoms; EICR: enfermedad injerto contra huésped; PEGA: pustulosis exantemática generalizada aguda; SSJ/NET: síndrome de Stevens-Johnson/necrólisis epidérmica tóxica; TPH: trasplante de progenitores hematopoyéticos; VHC: virus de la hepatitis C.
Fuente: elaboración propia.
El tratamiento de la EICR-A depende del grado y la localización de la enfermedad. Para formas localizadas de EICR-A cutánea de grado I, se pueden utilizar corticoides tópicos. En la EICR-A de grado II, se requiere tratamiento sistémico con corticosteroides como la prednisona (1-2mg/kg/día, aunque dosis menores pueden ser suficientes). Para la EICR-A cutánea refractaria a corticoides, una opción terapéutica es la fotoaféresis extracorpórea, con tasas de respuesta completa mayores del 80%, mejorando la supervivencia y reduciendo la mortalidad, especialmente si se inicia dentro de los primeros 35 días. La fototerapia UVA-1 y UVB también pueden ser beneficiosas en manifestaciones cutáneas localizadas. Otra alternativa en casos refractarios es el uso de globulina antitimocítica (ATG). Dentro de los fármacos, destacan el tacrólimus, el micofenolato de mofetilo, el sirolimus o los inhibidores de la janus kinasa (I-JAK), especialmente ruxolitinib15,16. Este último ha sido recientemente aprobado para la EICR-A refractaria a corticoides sistémicos17.
Enfermedad injerto contra receptor crónicaLa EICR-crónica (EICR-C) es una enfermedad multisistémica que puede afectar a cualquier órgano, siendo nuevamente la afectación de la piel y la mucosa oral la más frecuente, hasta en el 80% de los pacientes. Otros órganos afectados en orden decreciente de frecuencia son el hígado, los ojos (síndrome del ojo seco), el intestino y los pulmones. Igualmente, puede afectar a nivel musculoesquelético y psicológico, dado el carácter crónico de la enfermedad5,10,18,19.
A nivel mucocutáneo, la EICR-C es una enfermedad polimórfica, tanto a nivel de la piel como de la mucosa oral y genital (tabla 3, fig. 3). En 2014, el Proyecto de Consenso NIH propuso una clasificación de la EICR-C utilizando criterios órgano-específicos5,7.
Manifestaciones clínicas de las manifestaciones mucocutáneas de la EICR crónica
| Piel | Pelo | Uñas | Mucosa oral | Mucosa genital |
|---|---|---|---|---|
| Liquen plano-likeLiquen escleroso-likeMorfea-likeFascitis-likePoiquilodermiaPsoriasiformeEccematoso/dishidróticoLECS-likePitiriasis rosada-likeIctiosiforme/queratosis pilar-likeHipopigmentaciónHiperpigmentaciónVitíligoNódulos angiomatososCalcinosis cutis | Alopecia de nuevo desarrollo (especialmente parcheada >difusa). Puede ser cicatricial o no cicatricialColoración grisácea prematura del pelo | RugosidadAdelgazamientoRoturaFragilidadOnicólisisPterigión dorsalAnoniquia | Placas queratósicasLiquen plano-likeMicrostomía por esclerosisGingivitisMucositisPseudomembranasÚlcerasXerostomíaAtrofia mucosaMucocele | Liquen plano-likeEstenosis o cicatrices a nivel vulvovaginalFisurasErosionesÚlcerasBalanitisFimosis |
EICR: enfermedad injerto contra receptor; LECS: lupus eritematoso cutáneo subagudo.
Fuente: elaboración propia.
Se resaltan en negrita los criterios «diagnósticos» del Proyecto de Consenso del NIH. Estos criterios son aquellas manifestaciones cutáneas suficientes para hacer un diagnóstico clínico de EICR crónica. Los criterios restantes se denominaron criterios «distintivos» de la EICR crónica, ya que requieren la exclusión de otras posibles etiologías.
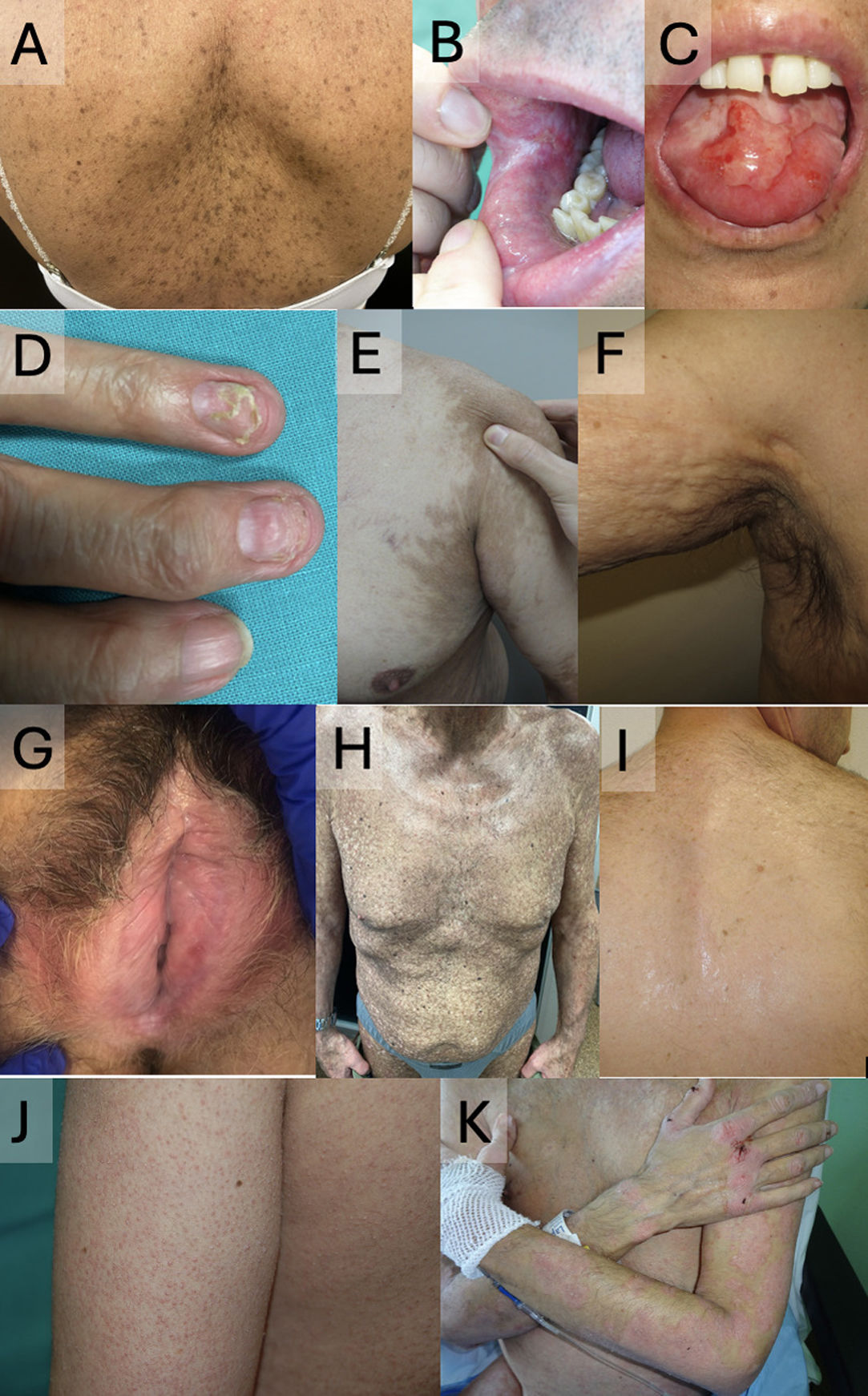
EICR crónica mucocutánea. A-C. Patrón liquen plano-like, afectando a la espalda (A), la mucosa labial y yugal (B) y la lengua (C). D. Afectación ungueal con onicólisis y pterigión. E. Patrón esclerodermia-like, con hiperpigmentación secundaria. F. Patrón fascitis-like. G. Afectación de mucosa genital, con cambios esclerodermiformes liquen escleroatrófico-like. H. Patrón poiquilodermia-like. I. Patrón liquen escleroatrófico-like, con afectación extragenital en espalda. J. Patrón queratosis pilaris-like. K. Patrón psoriasiforme.
El diagnóstico de la EICR-C es clínico. Puede apoyarse de pruebas complementarias, destacando la biopsia cutánea. A nivel histológico, la EICR-C se manifiesta principalmente con dos patrones: liquenoide o esclerodermiforme. La forma liquenoide presenta acantosis, hiperqueratosis ortoqueratósica y paraqueratósica con un infiltrado linfocítico en banda, vacuolización de la capa basal y queratinocitos apoptóticos, similar al liquen plano, pero con necrosis de células satélite como clave distintiva. La forma esclerodermiforme se caracteriza por esclerosis dérmica y pérdida de grasa perianexial, similar a una biopsia de morfea o liquen escleroso. Otras formas menos frecuentes en la biopsia son las similares a la fascitis o la psoriasiforme9,20. Sin embargo, estos hallazgos son inespecíficos y deben ser evaluados en el contexto clínico del paciente. Actualmente, se están evaluando biomarcadores específicos para el diagnóstico de la EICR-C, tanto a nivel histológico como genético, pero todavía en fase de desarrollo21. El diagnóstico diferencial incluye la EICR-A, las toxicodermias e infecciones virales, además del liquen plano, la psoriasis, la morfea y la esclerodermia sistémica, entre otras5,7.
Respecto al tratamiento de la EICR-C mucocutánea, carecemos de guías terapéuticas estandarizadas, ya que la mayoría de los ensayos excluyen resultados dermatológicos. Es esencial el cuidado adecuado de la piel, con medidas generales y emolientes. El tratamiento de primera línea en formas leves consiste en corticoides tópicos. Como ahorrador de corticoides, pueden emplearse inhibidores de la calcineurina tópicos. En casos más graves, generalmente se emplea la fototerapia (UVB o UVA1), la fotoaféresis extracorpórea, el rituximab, el imatinib (estos últimos especialmente en formas esclerodermiformes) y, más recientemente, ibrutinib y ruxolitinib10,15,16. A nivel oral y genital, el tratamiento es similar, destacando especialmente la utilidad de tacrólimus en enjuagues para las lesiones liquenoides orales22. Es esencial un seguimiento multidisciplinar (hematología, dermatología, reumatología y ginecología, entre otras), dada la cronicidad de esta patología y sus potenciales complicaciones.
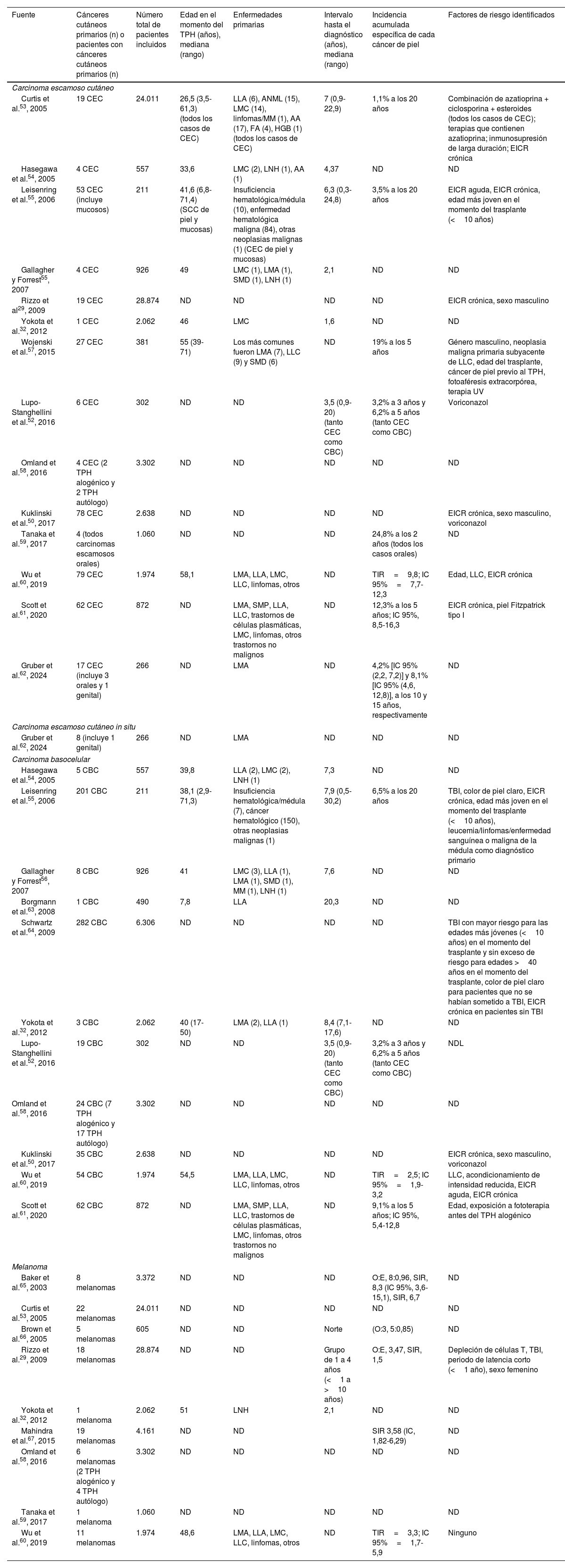
Cáncer cutáneo tras trasplante de progenitores hematopoyéticosExiste una clara asociación entre la inmunosupresión crónica en pacientes sometidos a trasplante de órganos sólidos (TOS) y el desarrollo de cáncer cutáneo23–27. Sin embargo, la relación entre TPH y cáncer cutáneo no ha sido tan bien documentada. Se ha descrito que los individuos sometidos a TPH tienen un mayor riesgo de neoplasias secundarias en comparación con la población general28–30. Concretamente, las neoplasias malignas sólidas aparecen hasta en el 15% de los pacientes 15 años después del TPH con acondicionamiento mieloablativo y son responsables del 5-10% de las muertes tardías tras el TPH30. En cuanto al cáncer cutáneo (tabla 4)29,32,50,52–61,65–67, los estudios publicados revelan una incidencia aproximada de entre el 1% y el 2% a los 5 años de seguimiento, de entre el 1% y el 7% a los 10 años, y de entre el 6% y el 10% a los 20 años de seguimiento33. Se han señalado varios factores de riesgo, como el sexo masculino, la edad en el momento del TPH, los antecedentes de cáncer cutáneo, el tipo de acondicionamiento, la irradiación corporal total, el uso de voriconazol como profilaxis antifúngica o la presencia de ICRD, entre otros29–33. Una reciente revisión sistemática y metaanálisis señaló que la razón de incidencia estandarizada (SIR) para cáncer cutáneo post-TPH fue de 7,21 (IC 95%: 3,98-13,08), con SIR de 2,25 (IC 95%: 1,7-3,68) para TPH autólogo y 10,18 (IC 95%: 5,07-20,43) para TPH alogénico. Los factores de riesgo para el cáncer de piel incluyeron la EICR-C, específicamente para el carcinoma basocelular y el carcinoma escamoso cutáneo (CEC), así como el género masculino y la exposición a voriconazol para el CEC34. La EICR, especialmente la EICR-C y con afectación mucocutánea, podría asociarse a mayor riesgo de cáncer cutáneo por varios motivos, entre ellos la inflamación crónica de la piel y las mucosas en pacientes con EICR-C, así como la mayor necesidad de inmunosupresión para el tratamiento de la EICR. Ya se ha demostrado previamente que la inflamación crónica es un factor de riesgo independiente de cáncer de piel, en particular del CEC49. Por otra parte, el voriconazol es un conocido fármaco fototóxico y asociado a carcinogénesis, derivado de la producción de radicales con su metabolismo. Su empleo como profilaxis antifúngica en pacientes sometidos a TPH se ha relacionado con cáncer cutáneo, especialmente en el espectro de queratosis actínica-carcinoma escamoso cutáneo50–52.
Principales estudios que evalúan el riesgo de queratosis actínicas y cáncer cutáneo posteriores a la realización de TPH
| Fuente | Cánceres cutáneos primarios (n) o pacientes con cánceres cutáneos primarios (n) | Número total de pacientes incluidos | Edad en el momento del TPH (años), mediana (rango) | Enfermedades primarias | Intervalo hasta el diagnóstico (años), mediana (rango) | Incidencia acumulada específica de cada cáncer de piel | Factores de riesgo identificados |
|---|---|---|---|---|---|---|---|
| Carcinoma escamoso cutáneo | |||||||
| Curtis et al.53, 2005 | 19 CEC | 24.011 | 26,5 (3,5-61,3) (todos los casos de CEC) | LLA (6), ANML (15), LMC (14), linfomas/MM (1), AA (17), FA (4), HGB (1) (todos los casos de CEC) | 7 (0,9-22,9) | 1,1% a los 20 años | Combinación de azatioprina + ciclosporina + esteroides (todos los casos de CEC); terapias que contienen azatioprina; inmunosupresión de larga duración; EICR crónica |
| Hasegawa et al.54, 2005 | 4 CEC | 557 | 33,6 | LMC (2), LNH (1), AA (1) | 4,37 | ND | ND |
| Leisenring et al.55, 2006 | 53 CEC (incluye mucosos) | 211 | 41,6 (6,8-71,4) (SCC de piel y mucosas) | Insuficiencia hematológica/médula (10), enfermedad hematológica maligna (84), otras neoplasias malignas (1) (CEC de piel y mucosas) | 6,3 (0,3-24,8) | 3,5% a los 20 años | EICR aguda, EICR crónica, edad más joven en el momento del trasplante (<10 años) |
| Gallagher y Forrest55, 2007 | 4 CEC | 926 | 49 | LMC (1), LMA (1), SMD (1), LNH (1) | 2,1 | ND | ND |
| Rizzo et al29, 2009 | 19 CEC | 28.874 | ND | ND | ND | ND | EICR crónica, sexo masculino |
| Yokota et al.32, 2012 | 1 CEC | 2.062 | 46 | LMC | 1,6 | ND | ND |
| Wojenski et al.57, 2015 | 27 CEC | 381 | 55 (39-71) | Los más comunes fueron LMA (7), LLC (9) y SMD (6) | ND | 19% a los 5 años | Género masculino, neoplasia maligna primaria subyacente de LLC, edad del trasplante, cáncer de piel previo al TPH, fotoaféresis extracorpórea, terapia UV |
| Lupo-Stanghellini et al.52, 2016 | 6 CEC | 302 | ND | ND | 3,5 (0,9-20) (tanto CEC como CBC) | 3,2% a 3 años y 6,2% a 5 años (tanto CEC como CBC) | Voriconazol |
| Omland et al.58, 2016 | 4 CEC (2 TPH alogénico y 2 TPH autólogo) | 3.302 | ND | ND | ND | ND | ND |
| Kuklinski et al.50, 2017 | 78 CEC | 2.638 | ND | ND | ND | ND | EICR crónica, sexo masculino, voriconazol |
| Tanaka et al.59, 2017 | 4 (todos carcinomas escamosos orales) | 1.060 | ND | ND | ND | 24,8% a los 2 años (todos los casos orales) | ND |
| Wu et al.60, 2019 | 79 CEC | 1.974 | 58,1 | LMA, LLA, LMC, LLC, linfomas, otros | ND | TIR=9,8; IC 95%=7,7-12,3 | Edad, LLC, EICR crónica |
| Scott et al.61, 2020 | 62 CEC | 872 | ND | LMA, SMP, LLA, LLC, trastornos de células plasmáticas, LMC, linfomas, otros trastornos no malignos | ND | 12,3% a los 5 años; IC 95%, 8,5-16,3 | EICR crónica, piel Fitzpatrick tipo I |
| Gruber et al.62, 2024 | 17 CEC (incluye 3 orales y 1 genital) | 266 | ND | LMA | ND | 4,2% [IC 95% (2,2, 7,2)] y 8,1% [IC 95% (4,6, 12,8)], a los 10 y 15 años, respectivamente | ND |
| Carcinoma escamoso cutáneo in situ | |||||||
| Gruber et al.62, 2024 | 8 (incluye 1 genital) | 266 | ND | LMA | ND | ND | ND |
| Carcinoma basocelular | |||||||
| Hasegawa et al.54, 2005 | 5 CBC | 557 | 39,8 | LLA (2), LMC (2), LNH (1) | 7,3 | ND | ND |
| Leisenring et al.55, 2006 | 201 CBC | 211 | 38,1 (2,9-71,3) | Insuficiencia hematológica/médula (7), cáncer hematológico (150), otras neoplasias malignas (1) | 7,9 (0,5-30,2) | 6,5% a los 20 años | TBI, color de piel claro, EICR crónica, edad más joven en el momento del trasplante (<10 años), leucemia/linfomas/enfermedad sanguínea o maligna de la médula como diagnóstico primario |
| Gallagher y Forrest56, 2007 | 8 CBC | 926 | 41 | LMC (3), LLA (1), LMA (1), SMD (1), MM (1), LNH (1) | 7,6 | ND | ND |
| Borgmann et al.63, 2008 | 1 CBC | 490 | 7,8 | LLA | 20,3 | ND | ND |
| Schwartz et al.64, 2009 | 282 CBC | 6.306 | ND | ND | ND | ND | TBI con mayor riesgo para las edades más jóvenes (<10 años) en el momento del trasplante y sin exceso de riesgo para edades >40 años en el momento del trasplante, color de piel claro para pacientes que no se habían sometido a TBI, EICR crónica en pacientes sin TBI |
| Yokota et al.32, 2012 | 3 CBC | 2.062 | 40 (17-50) | LMA (2), LLA (1) | 8,4 (7,1-17,6) | ND | ND |
| Lupo-Stanghellini et al.52, 2016 | 19 CBC | 302 | ND | ND | 3,5 (0,9-20) (tanto CEC como CBC) | 3,2% a 3 años y 6,2% a 5 años (tanto CEC como CBC) | NDL |
| Omland et al.58, 2016 | 24 CBC (7 TPH alogénico y 17 TPH autólogo) | 3.302 | ND | ND | ND | ND | ND |
| Kuklinski et al.50, 2017 | 35 CBC | 2.638 | ND | ND | ND | ND | EICR crónica, sexo masculino, voriconazol |
| Wu et al.60, 2019 | 54 CBC | 1.974 | 54,5 | LMA, LLA, LMC, LLC, linfomas, otros | ND | TIR=2,5; IC 95%=1,9-3,2 | LLC, acondicionamiento de intensidad reducida, EICR aguda, EICR crónica |
| Scott et al.61, 2020 | 62 CBC | 872 | ND | LMA, SMP, LLA, LLC, trastornos de células plasmáticas, LMC, linfomas, otros trastornos no malignos | ND | 9,1% a los 5 años; IC 95%, 5,4-12,8 | Edad, exposición a fototerapia antes del TPH alogénico |
| Melanoma | |||||||
| Baker et al.65, 2003 | 8 melanomas | 3.372 | ND | ND | ND | O:E, 8:0,96, SIR, 8,3 (IC 95%, 3,6-15,1), SIR, 6,7 | ND |
| Curtis et al.53, 2005 | 22 melanomas | 24.011 | ND | ND | ND | ND | ND |
| Brown et al.66, 2005 | 5 melanomas | 605 | ND | ND | Norte | (O:3, 5:0,85) | ND |
| Rizzo et al.29, 2009 | 18 melanomas | 28.874 | ND | ND | Grupo de 1 a 4 años (<1 a >10 años) | O:E, 3,47, SIR, 1,5 | Depleción de células T, TBI, periodo de latencia corto (<1 año), sexo femenino |
| Yokota et al.32, 2012 | 1 melanoma | 2.062 | 51 | LNH | 2,1 | ND | ND |
| Mahindra et al.67, 2015 | 19 melanomas | 4.161 | ND | ND | SIR 3,58 (IC, 1,82-6,29) | ND | |
| Omland et al.58, 2016 | 6 melanomas (2 TPH alogénico y 4 TPH autólogo) | 3.302 | ND | ND | ND | ND | ND |
| Tanaka et al.59, 2017 | 1 melanoma | 1.060 | ND | ND | ND | ND | ND |
| Wu et al.60, 2019 | 11 melanomas | 1.974 | 48,6 | LMA, LLA, LMC, LLC, linfomas, otros | ND | TIR=3,3; IC 95%=1,7-5,9 | Ninguno |
AA: anemia aplásica; AF: anemia de Fanconi; CBC: carcinoma basocelular; EICR: enfermedad de injerto contra receptor; HGB: hemoglobinopatías; LLA: leucemia linfoblástica aguda; LMA: leucemia mieloide aguda; LMC: leucemia mieloide crónica; LNH: linfomas no Hodgkin; MM: mieloma múltiple; ND: no descrito; CEC: carcinoma de células escamosas; SIR: razón de incidencia estandarizada; IC: intervalo de confianza; SMD: síndrome mielodisplásico; TBI: irradiación corporal total; TIR: razón de tasas de incidencia; TPH: trasplante de progenitores hematopoyéticos.
Fuente: elaboración propia.
Debido al riesgo incrementado de cáncer cutáneo, diversos autores han recomendado la realización de un cribado selectivo y seguimiento de cáncer cutáneo en estos pacientes34–36.
Otras alteraciones mucocutáneas tras trasplante de progenitores hematopoyéticos(tabla 5)37,41-44,45,47,50,70Los individuos sometidos a TPH pueden presentar numerosas alteraciones mucocutáneas. Además de las comentadas EICR, infecciones virales, toxicodermias y segundas neoplasias mucocutáneas nos centraremos en otras infecciones, así como en otras entidades menos frecuentes. Las infecciones mucocutáneas más frecuentes tras TPH son las producidas por el virus varicela-zóster, las infecciones del túnel o del orificio de salida relacionadas con catéteres y las manifestaciones cutáneas de infecciones bacterianas o fúngicas diseminadas. Son frecuentes las áreas focales de celulitis bacteriana en las extremidades inferiores en el contexto de edema por insuficiencia cardiaca, linfedema y alteración del retorno venoso37,38. Igualmente, son relativamente frecuentes las infecciones por molusco contagioso y citomegalovirus. Es importante resaltar que su presentación puede ser atípica y más agresiva, dado el contexto de inmunosupresión y de administración de múltiples fármacos en los pacientes sometidos a TPH39, así como la posibilidad de linfoma post-trasplante asociado al virus de Ebstein-Barr, aunque la presentación con lesiones cutáneas aisladas es rara40.
Principales estudios que evalúan alteraciones mucocutáneas (distintas a EICR) posteriores a TPH
| Autor/año | Tamaño muestral | Tipo de estudio y enfermedades evaluadas | Resultados |
|---|---|---|---|
| Canninga-van Dijk et al.37, 2003 | NE | - Revisión narrativa- Todo tipo de indicaciones | - Los pacientes sometidos a TPH, además de exantemas virales, están sometidos a mayor riesgo de infecciones bacterianas (especialmente piodermitis por Staphylococcus aureus), infecciones por herpes simple y virus varicela-zóster, reactivación de citomegalovirus, molusco contagioso o infecciones fúngicas- Su presentación puede ser atípica y más agresiva, dado su contexto- Es importante reseñar la posibilidad de linfoma post-trasplante asociado al VEB, aunque la presentación con lesiones cutáneas aisladas es rara |
| Mabuchi et al.41, 2012 | 1 | - Caso clínico aislado- Unicéntrico- LNH | La psoriasis puede desarrollarse de novo tras un TPH de donante sin psoriasisa. En este caso, a los 10 años después del TPH alogénico en un paciente con LNH |
| Khalil et al.68, 2014 | 92 | - Estudio de cohortes retrospectivo- Unicéntrico- Enfermedades no malignas | - Seis pacientes (6,5%) fueron diagnosticados de vitíligo sin relación con EICR crónica, 6 (6,5%) de anemia hemolítica autoinmune, 6 (6,5%) de trombocitopenia idiopática, 3 (3,3%) de leucopenia leve, 2 (2,2%) de anemia aplásica y uno (1,1%) de enfermedad tiroidea autoinmune- Las complicaciones autoinmunes fueron más frecuentes en pacientes con TPH secundario a trastornos metabólicos |
| Kato et al.47, 2015 | 1 | - Caso clínico aislado- Unicéntrico- Leucemia linfoblástica T | - El TPH podría constituir un factor de riesgo para penfigoide ampolloso en pacientes sometidos a TPH, por lo que, ante clínica sospechosa, debe ser descartado con clínica, biopsia y serología con anticuerpos anti-membrana basal epidérmica |
| Bae et al.42, 2016 | 2.457 receptores de TPH vs. 8.241 controles | - Estudio de cohortes retrospectivo- Multicéntrico- Todos los diagnósticos | - Se encontró una asociación a vitíligo en pacientes sometidos a TPH, de forma independiente a la presencia de EICR y superior al grupo control- Los factores de riesgo más asociados a la aparición de vitíligo fueron el TPH alogénico y la fuente médula ósea |
| Song et al.44, 2017 | 85 receptores de TPH vs. 85 controles | - Estudio de cohortes prospectivo- Unicéntrico- Todos los diagnósticos | - Los niños sometidos a TPH tenían significativamente más nevus que los controles (mediana [intervalo]: 44 (0-150) frente a 11 (0-94), p=0,0001)- Los niños con TPH tenían significativamente más nevus >5mm de diámetro y más nevus atípicos que los controles- Entre los factores asociados a un mayor número de nevus se incluían la indicación maligna del TPH, la QT previa al trasplante, la exposición a TBI y el acondicionamiento mieloablativo |
| Bresters et al.43, 2017 | 263 | - Estudio de cohortes retrospectivo- Unicéntrico- Todos los diagnósticos | - El porcentaje de alopecia permanente fue del 15,6% (41/263 pacientes)- Un régimen de acondicionamiento con busulfán y busulfán más fludarabina (OD 5,7 [IC: 2,5-12,7] y OR 7,4 [IC: 3,3-16,2], respectivamente, fue el principal factor de riesgo, y se asoció a alopecia independientemente de la EICR aguda/crónica |
| Huang et al.48, 2018 | 85 | - Estudio de cohortes retrospectivo- Unicéntrico- Todos los diagnósticos | - Un 14% (n=12) de los pacientes desarrollaron vitíligo; un 16% (n=14), psoriasis/sebopsoriasis; un 25% (n=21), alopecia; y un 6% (n=5), alteraciones ungueales- Entre los factores significativamente asociados con el vitíligo independientes de la EICR se encontraban la indicación de inmunodeficiencia primaria y la menor edad en el momento del trasplante (<10 años)- Los factores significativamente asociados con la alopecia independientes de la EICR fueron el acondicionamiento con busulfán y los antecedentes familiares de alopecia androgénica precoz- El único factor de riesgo identificado para alteraciones ungueales fue el antecedente de EICR crónica |
| Miyagi et al.45, 2023 | 2 | - Dos casos clínicos y revisión de la literatura- Unicéntrico | - La dermatomiositis puede ser una complicación tardía del TPH, y es esencial descartarla ante clínica cutánea y muscular compatible en pacientes sometidos a TPH |
EICR: enfermedad injerto contra receptor; IC: intervalo de confianza; LNH: linfoma no Hodking; NE: no especificado; OR: odds ratio; QT: quimioterapia; TBI: irradiación corporal total; TPH: trasplante de progenitores hematopoyéticos.
Otras dermatosis incluyen el desarrollo de novo de psoriasis41, de vitíligo en pacientes sin otros síntomas de EICR-C42, de alopecia en pacientes sin otros síntomas de EICR-C43, o aparición de nevus melanocíticos en niños44. Recientemente, se han descrito varios casos de dermatomiositis en pacientes sometidos previamente a TPH, algunas de ellas con afectación pulmonar severa45,46, así como un caso de penfigoide ampolloso post-TPH47. Un estudio reciente describió las alteraciones cutáneas tardías en niños sometidos a TPH, destacando la elevada incidencia de vitíligo, de psoriasis/sebopsoriasis, de alopecia y los cambios ungueales, especialmente en niños con EICR-C, edad <10 años al TPH e inmunodeficiencia primaria como enfermedad basal al TPH48.
DiscusiónEn esta revisión, se han presentado los principales cambios mucocutáneos en pacientes sometidos a TPH. Entre ellos, destaca por su frecuencia y potencial gravedad la EICR. En su variante aguda, plantea un diagnóstico diferencial muy complejo, especialmente con toxicodermias e infecciones víricas. Es esencial una adecuada historia clínica para su correcto diagnóstico, dada la inespecificidad de sus lesiones5,8,10. En su tratamiento, además de los corticoides tópicos o sistémicos, cabe resaltar la reciente aprobación de ruxolitinib como tratamiento de segunda línea15–17. Por su parte, en referencia a la EICR-C, quizá su aspecto más destacado sea su polimorfismo, pudiendo presentarse de más de 10 formas diferentes a nivel cutáneo, destacando las variantes liquenoide y esclerodermiforme; al igual que a nivel oral, genital, capilar o ungueal5,7. Este hecho pone de manifiesto la necesidad de realizar revisiones dermatológicas para un adecuado diagnóstico y seguimiento. Igualmente, es esencial la realización de sesiones multidisciplinares, dada su potencial afectación multiorgánica.
ConclusionesEl TPH ha revolucionado el tratamiento de diversas enfermedades hematológicas y no hematológicas, pero con un riesgo significativo de complicaciones mucocutáneas. Entre ellas, destacan la EICR, aguda y crónica, cuyo diagnóstico y tratamiento pueden ser notoriamente complejos. Otras patologías frecuentes son las infecciones con manifestaciones cutáneas y las toxicodermias. La identificación y manejo temprano de estas complicaciones, junto con un enfoque multidisciplinar, son esenciales para mejorar la calidad de vida y los resultados a largo plazo de estos pacientes. Asimismo, es recomendable el cribado de cáncer cutáneo en estos individuos, especialmente si presentan factores de riesgo, y entregar recomendaciones de fotoprotección.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.