El dupilumab es un anticuerpo IgG4 monoclonal recombinante humano que inhibe las interleucinas (IL)-4 y IL-13 mediante su unión específica a la subunidad IL-4Rα de sus complejos receptores1. Se ha detectado IL-4 en biopsias de urticaria crónica espontánea (UCE)2 y se ha descrito la eficacia de dupilumab en UCE1,3-5 y en urticaria crónica inducible (UCInd) (p. ej., urticaria por frío6, colinérgica7 o solar8). Se describen a continuación 2casos, con una UCE y UCInd tipo urticaria por presión retardada (UPR), refractarias al omalizumab con una respuesta excelente posterior al dupilimab.
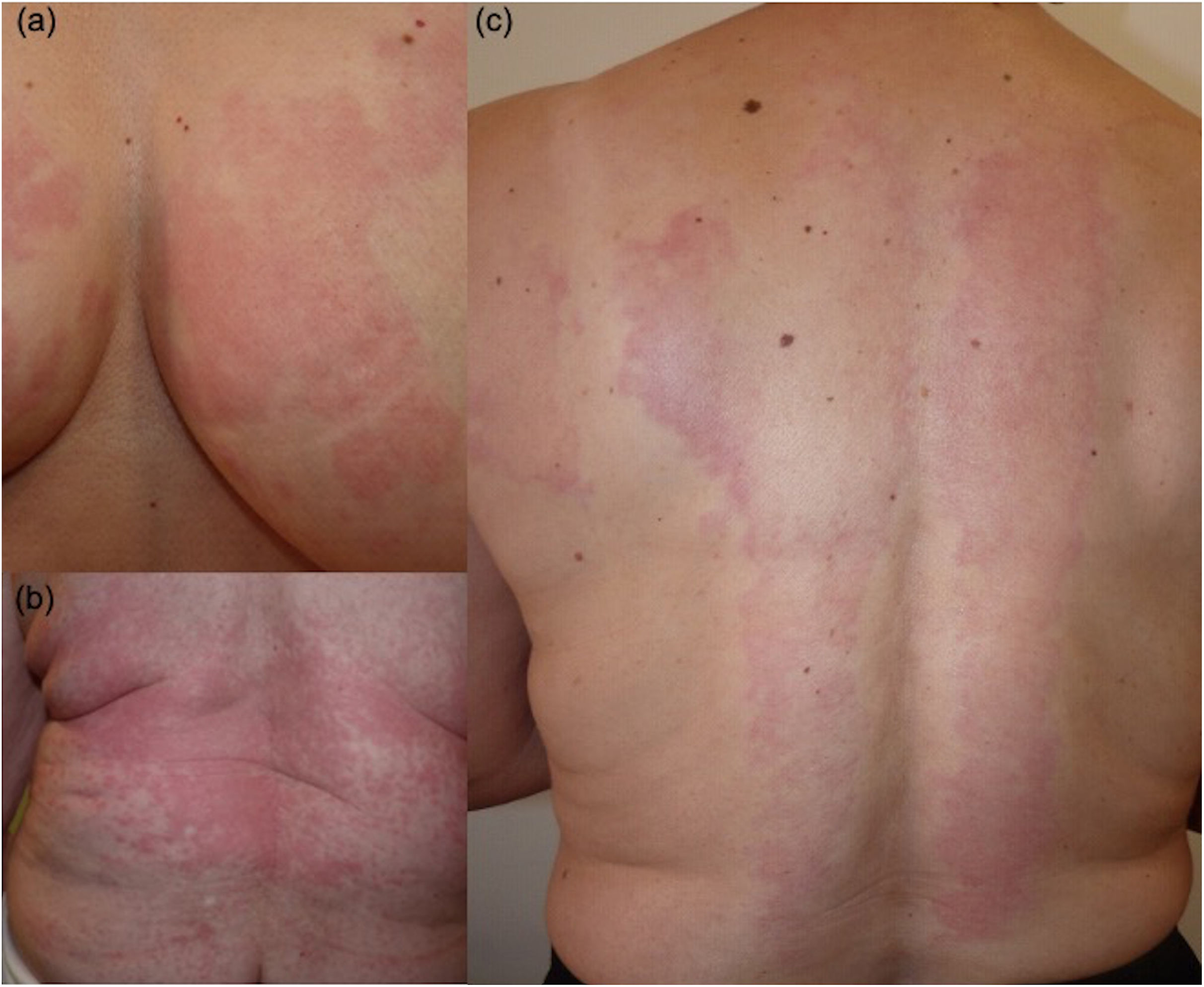
Caso 1. En 2012, una mujer de 67 años de edad con antecedentes de diabetes, hipertensión, dislipidemia y tiroiditis autoinmune, con UCE y UCInd tipo UPR (fig. 1 a-c) refractarias a antihistamínicos y ciclosporina, fue tratada con omalizumab (300mg cada 15 días) con una rápida resolución del cuadro. En 2018, tras permanecer asintomática varios años, se suspendió el omalizumab desarrollándose al poco tiempo una recaída relacionada con acontecimientos estresantes. Al no responder al tratamiento intensificado (omalizumab 600mg cada 3-4 semanas) combinado con antihistamínicos (×4), se pautaron sucesivamente otros fármacos sistémicos (ciclosporina, dapsona, metotrexato, montelukast y azatioprina y minipulsos semanales de dexametasona) sin mejoría. El estudio histopatológico mostró unos infiltrados dérmicos intersticiales de neutrófilos y eosinófilos, sin daño vascular. El test del peso suspendido fue positivo.
En febrero del 2022, la paciente presentaba un Urticaria Activity Score (UAS)7>20 con un impacto grave en la calidad de vida, precisando diariamente corticoides orales. En ese momento, se inició el tratamiento con dupilumab (600mg en el día 0 seguidos de 300mg bisemanal) percibiéndose una mejoría inicial del prurito, si bien, siguió precisando corticoides orales. A los 2meses presentó una exacerbación que atribuyó al COVID-19 (con una UPR por reposo prolongado en cama). La paciente comenzó a responder a partir del tercer mes y fue posible reducir progresivamente la dosis de corticoide hasta suspenderlo completamente en el quino mes. Los valores de IgE descendieron de 6 KU/l a 4 KU/l a los 3 meses de iniciar el tratamiento. Posteriormente, se ha mantenido asintomática sin corticoide durante los siguientes 11 meses (16 meses desde el inicio del tratamiento).
Caso 2. Una mujer de 59 años de edad, médico, con antecedentes de polinosis y tiroiditis autoinmune, desarrolló 2episodios de UCE entre 2011 y 2014 de varios meses de duración. En enero del 2020, presentó nuevamente UCE con angioedema y UPR. El estudio histopatológico mostró una inflamación dérmica intersticial con eosinófilos sin vasculitis.
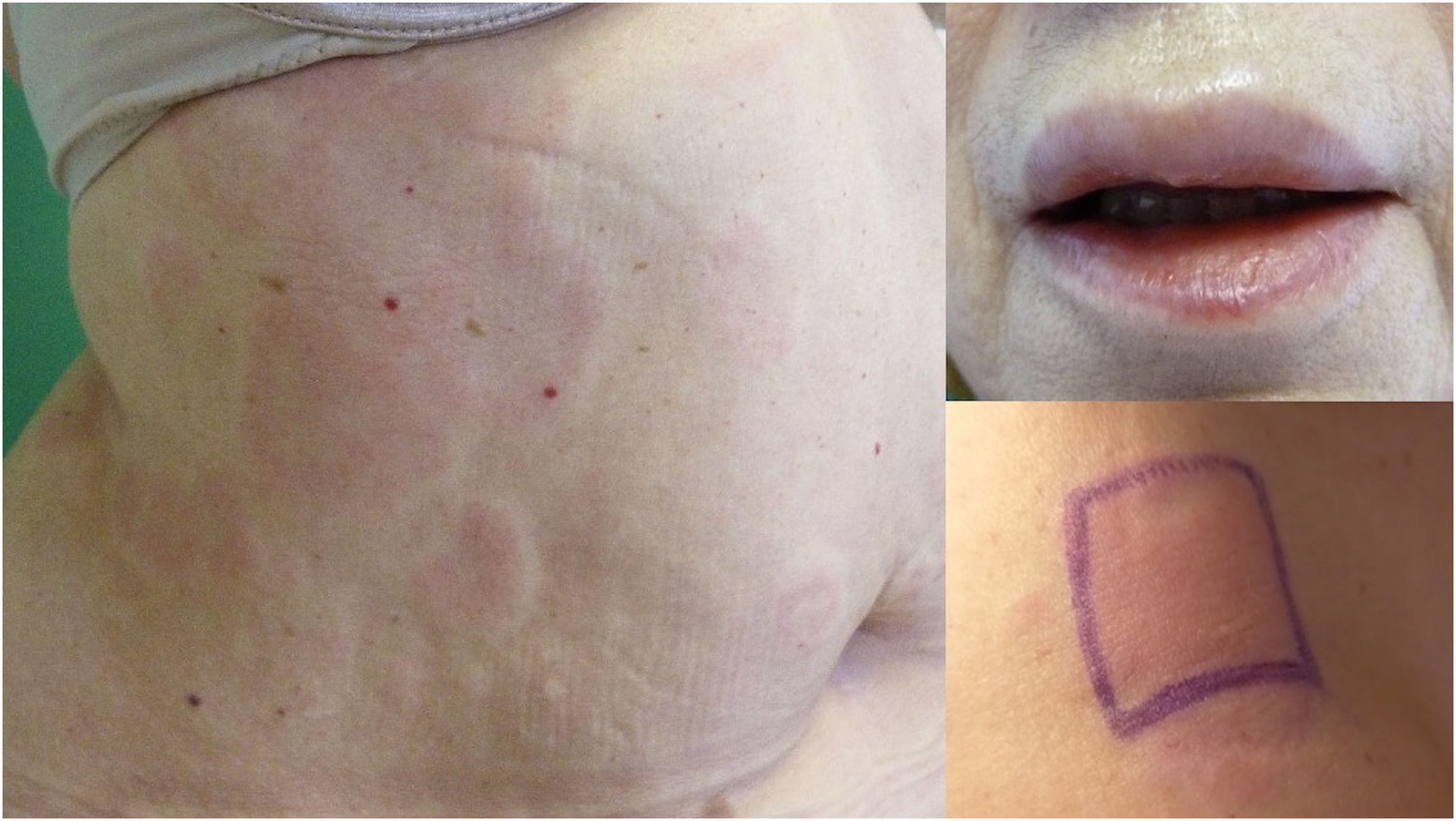
Se trató con antihistamínicos (×4) y prednisona, sin mejoría, por lo que precisó una baja laboral por una privación del sueño. A continuación, se introdujo el omalizumab (300mg cada 4 semanas), con un buen control inicial (incrementándose la IgE de 19,9 KU/l a 65,7 KU/l al mes del inicio), pero debido al estrés por la pandemia (COVID-19), en marzo del 2020, se deterioró el control de la enfermedad y precisó incrementar la dosis del omalizumab (600mg mensuales) y asociar prednisona (5-10mg) durante 2años por la presencia de habones persistentes (UAS: 24-42) (fig. 2 a), angioedema (fig. 2 b) y un deterioro de la calidad de vida (DLQI=30). El test del peso suspendido fue repetidamente positivo (fig. 2c).
Se descartó la ciclosporina porque la paciente atendía regularmente a enfermos de COVID-19. Por ello, se trató con dupilumab (600mg en D0 y 300mg cada 2semanas) pese a lo que continuó presentando lesiones los primeros 4meses. Sin embargo, a partir del quinto mes, experimentó una mejoría progresiva con una resolución completa de los habones y del angioedema en el séptimo mes. Los valores de IgE se elevaron discretamente de 42,4 KU/l (antes de la primera dosis de dupilumab) a 46,5 KU/l (al mes del inicio). Posteriormente, se mantuvo asintomática sin corticoides durante 12 meses de seguimiento (19 meses desde el inicio del tratamiento).
Tras suspender el omalizumab por un buen control, en caso de recaída, más del 90% de los pacientes responden al retratamiento9. Posiblemente, la asociación con una enfermedad autoinmune (diabetes mellitus o tiroiditis autoinmune), unos niveles bajos de IgE (especialmente en el primer caso), la presencia de angioedema (en el segundo caso), la propia UPR (variante de UCInd especialmente rebelde al tratamiento) y el estrés han podido contribuir a una respuesta desfavorable al omalizumab (con una refractariedad al reintroducirlo en el primer caso y una pérdida de eficacia en el segundo). No se puede precisar si una pauta intensificada de dupilimab habría acortado en estos casos el tiempo de respuesta porque no existen precedentes de casos de UPR tratados con este fármaco.
El dupilumab emerge como una alternativa potencial para tratar UCE y UCInd refractarias al omalizumab. En nuestra experiencia, la respuesta puede no acontecer inmediatamente, sino al cabo de unos 3-4 meses del inicio.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.