El abordaje terapéutico de pacientes de edad avanzada con psoriasis en placas moderada-grave es complejo debido, entre otros factores, a las comorbilidades asociadas, la polimedicación y la inmunosenescencia propias de este grupo de edad. En el presente documento se recogen 17 recomendaciones para el manejo de la psoriasis moderada-grave en pacientes de edad avanzada (>65 años). Estas recomendaciones han sido propuestas por un comité científico de 6 dermatólogos a partir de una revisión de la literatura científica y consensuadas entre 51 miembros del Grupo de Psoriasis de la Academia Española de Dermatología y Venereología mediante dos rondas de consulta Delphi. En los pacientes con psoriasis moderada-grave de edad avanzada, estas recomendaciones pueden mejorar su manejo, resultados y pronóstico.
Managing moderate to severe psoriasis in older adults is complex due to factors characteristic of the later years of life, such as associated comorbidity, polypharmacy, and immunosenescence. This consensus statement discusses 17 recommendations for managing treatment for moderate to severe psoriasis in patients older than 65 years. The recommendations were proposed by a committee of 6 dermatologists who reviewed the literature. Fifty-one members of the Psoriasis Working Group of the Spanish Academy of Dermatology and Venereology (AEDV) then applied the Delphi process in 2 rounds to reach consensus on which principles to adopt. The recommendations can help to improve management, outcomes, and prognosis for older adults with moderate to severe psoriasis.
El curso crónico de la psoriasis y el aumento de la esperanza de vida han hecho que los pacientes de edad avanzada constituyan un grupo importante1. Se estima que hasta el 13% de los pacientes con psoriasis inician la enfermedad a partir de los 60 años, siendo moderada-grave en aproximadamente el 15% de ellos2.
Sin embargo, los pacientes de edad avanzada suelen ser excluidos de los estudios clínicos, por lo que la evidencia en términos de eficacia y seguridad en este grupo es limitada3. La mayor prevalencia de comorbilidades, la polimedicación, la inmunosenescencia y el mayor riesgo de efectos adversos (EA) en esta población hacen su abordaje terapéutico más complejo4. Tanto es así que las terapias biológicas se inician con mayor frecuencia en pacientes jóvenes1,2, pudiendo existir un infratratamiento injustificado en pacientes de mayor edad5.
Por tanto, es necesario un posicionamiento terapéutico que dote de mayor confianza y seguridad al dermatólogo en el manejo de la psoriasis en este subgrupo de edad. El presente estudio tiene como objetivo desarrollar recomendaciones basadas en la evidencia sobre el manejo del paciente mayor de 65 años con psoriasis en placas moderada-grave.
Materiales y métodosSe realizó una consulta Delphi dirigida a los miembros del Grupo de Psoriasis (GPS) de la Academia Española de Dermatología y Venereología (AEDV). El cuestionario para la primera ronda se desarrolló en base a una revisión de la literatura y el asesoramiento de un comité científico constituido por 6 dermatólogos expertos (JM, JCRC, IB, LG, SMC, PC) e incluía un total de 34 afirmaciones. Para cada afirmación, los panelistas expresaron su grado de acuerdo a través de una escala Likert de 9 puntos. Se estableció consenso si al menos el 75% de los panelistas se situaban en el rango de acuerdo (7-9) y desacuerdo (1-3). Las afirmaciones que no alcanzaron consenso en primera ronda fueron replanteadas en una segunda.
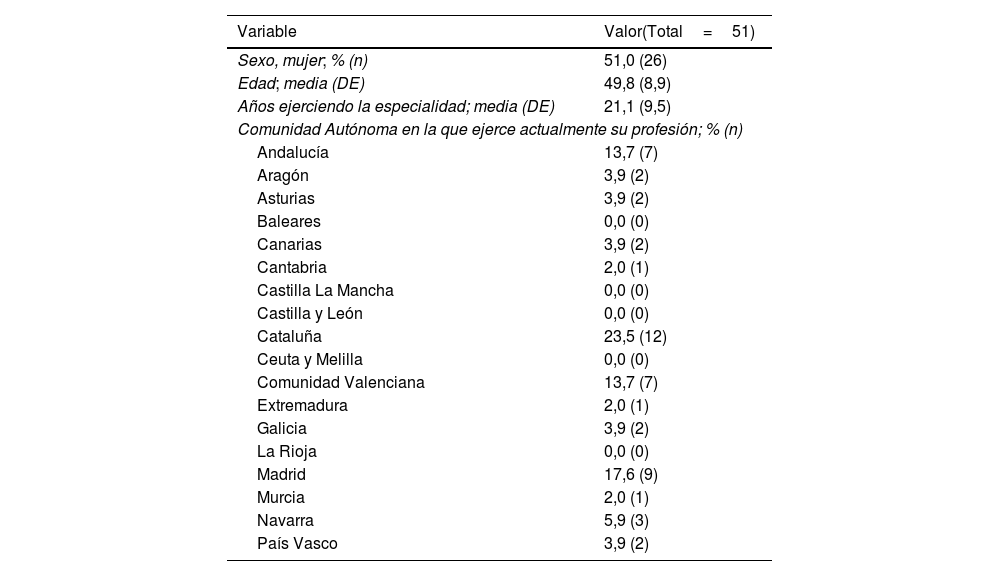
ResultadosEl cuestionario fue enviado a los miembros del GPS (n=151), participando 51 dermatólogos en primera (tasa de respuesta 33,8%) y 38 en segunda ronda (74,5%) (tabla 1).
Variables sociodemográficas y profesionales
| Variable | Valor(Total=51) |
|---|---|
| Sexo, mujer; % (n) | 51,0 (26) |
| Edad; media (DE) | 49,8 (8,9) |
| Años ejerciendo la especialidad; media (DE) | 21,1 (9,5) |
| Comunidad Autónoma en la que ejerce actualmente su profesión; % (n) | |
| Andalucía | 13,7 (7) |
| Aragón | 3,9 (2) |
| Asturias | 3,9 (2) |
| Baleares | 0,0 (0) |
| Canarias | 3,9 (2) |
| Cantabria | 2,0 (1) |
| Castilla La Mancha | 0,0 (0) |
| Castilla y León | 0,0 (0) |
| Cataluña | 23,5 (12) |
| Ceuta y Melilla | 0,0 (0) |
| Comunidad Valenciana | 13,7 (7) |
| Extremadura | 2,0 (1) |
| Galicia | 3,9 (2) |
| La Rioja | 0,0 (0) |
| Madrid | 17,6 (9) |
| Murcia | 2,0 (1) |
| Navarra | 5,9 (3) |
| País Vasco | 3,9 (2) |
DE: desviación estándar.
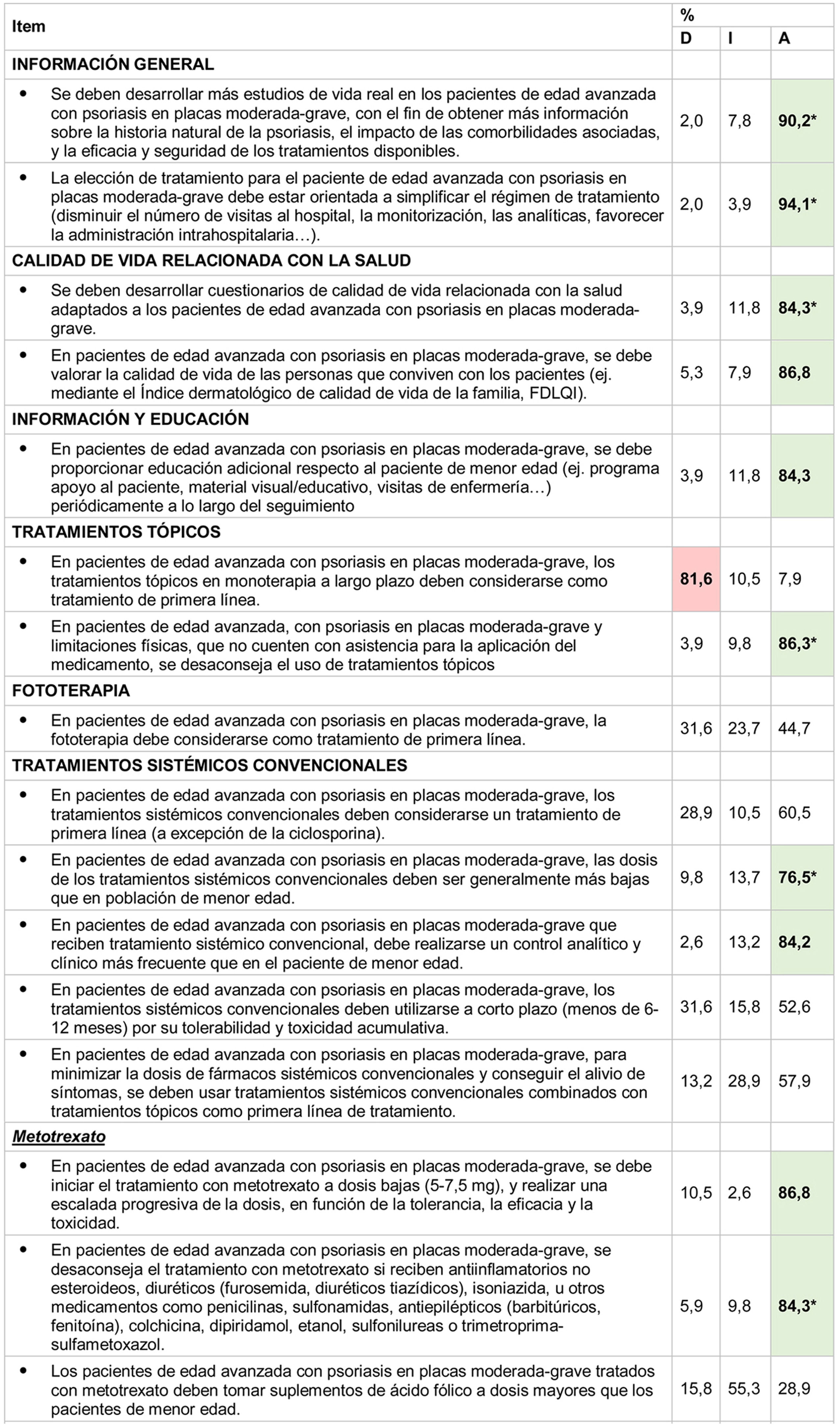
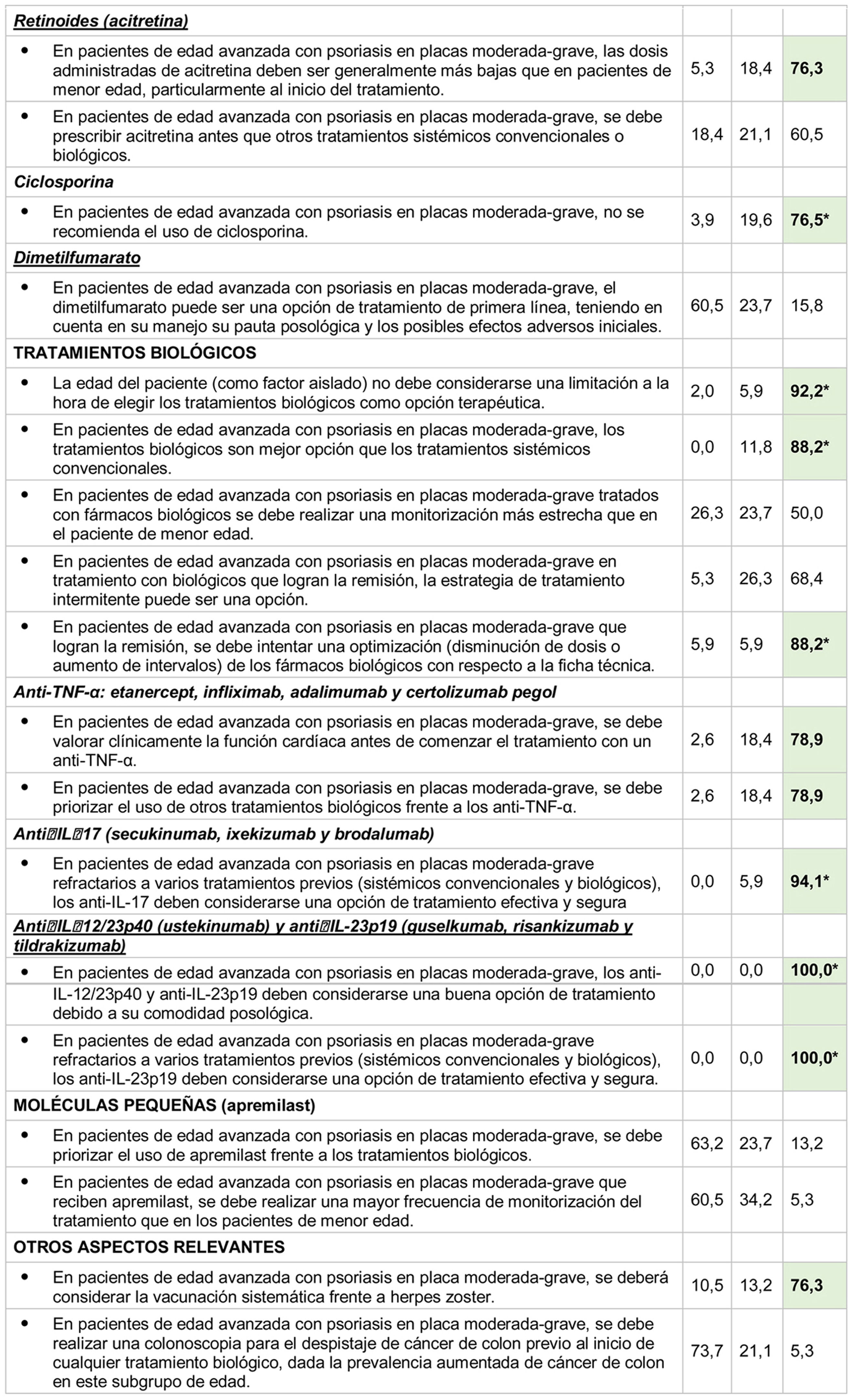
De las 34 afirmaciones planteadas, 22 alcanzaron consenso (13 en primera y 9 en segunda ronda) (tabla 2). De acuerdo con estos resultados, el comité científico propuso 17 recomendaciones, agrupadas en 5 bloques (tabla 3).
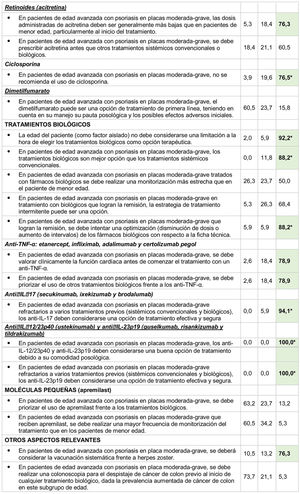
Resultados de la consulta Delphi
A: acuerdo (7, moderadamente de acuerdo; 8, bastante de acuerdo; 9, totalmente de acuerdo); D: desacuerdo o rechazo (1, totalmente en desacuerdo; 2, bastante en desacuerdo; 3, moderadamente en desacuerdo); I: indeterminación (4, algo en desacuerdo; 5, ni de acuerdo ni en desacuerdo; 6, algo de acuerdo).
* Acuerdo alcanzado en primera ronda de consulta Delphi.
Valores en negrita indican consenso (> 75% participantes de acuerdo o en desacuerdo).
Recomendaciones consensuadas
| Evaluación de calidad de vida |
| Recomendación 1. Desarrollar cuestionarios de calidad de vida relacionada con la salud (CVRS) adaptados a los pacientes de edad avanzada con psoriasis en placas moderada-grave |
| Recomendación 2. Evaluar la CVRS de las personas que conviven con los pacientes de edad avanzada con psoriasis en placas moderada-grave |
| Educación adicional |
| Recomendación 3. Proporcionar, a lo largo del seguimiento y de forma periódica, educación adicional respecto al paciente de menor edad (Ej. Programa apoyo al paciente, material visual/educativo, visitas enfermería, …) |
| Vacunación |
| Recomendación 4. Considerar la vacunación sistemática frente a herpes zóster en pacientes de edad avanzada con psoriasis en placas moderada-grave |
| Generación de la evidencia |
| Recomendación 5. Promover el desarrollo de estudios en práctica clínica real que incluyan población anciana con psoriasis moderada-grave |
| Tratamiento |
| Recomendación 6. Orientar la elección del tratamiento a simplificar el régimen terapéutico |
| Recomendación 7. Los tratamientos tópicos en monoterapia a largo plazo no deben considerarse como una opción de tratamiento de primera línea, especialmente en ancianos con limitaciones físicas que no cuenten con asistencia para la aplicación del medicamento |
| Recomendación 8. En los pacientes que reciben tratamiento sistémico convencional, las dosis deben ser generalmente más bajas y debe realizarse un control analítico y clínico más frecuente que en población de menor edad |
| Recomendación 9. Iniciar el tratamiento con metotrexato a dosis bajas (5-7,5 mg), y realizar una escalada progresiva de la dosis, en función de la tolerancia, la eficacia y la toxicidad; y se desaconseja su uso en pacientes que reciben antiinflamatorios no esteroideos, diuréticos, isoniazida, u otros medicamentos como penicilinas, sulfonamidas, antiepilépticos, colchicina, dipiridamol, etanol, sulfonilureas o trimetroprima-sulfametoxazol |
| Recomendación 10. Las dosis administradas de acitretina deben ser generalmente más bajas que en pacientes de menor edad, particularmente al inicio del tratamiento |
| Recomendación 11. No se recomienda el uso de ciclosporina en el paciente de edad avanzada con psoriasis moderada-grave |
| Recomendación 12. La edad del paciente como factor aislado no debe considerarse una limitación a la hora de elegir los tratamientos biológicos como opción terapéutica |
| Recomendación 13. Los tratamientos biológicos son, en su conjunto, más eficaces y mejor tolerados que los tratamientos sistémicos convencionales |
| Recomendación 14. Los fármacos anti-IL-12/23p40 y anti-IL-23p19 son una buena opción de tratamiento debido a su comodidad posológica tanto en primera como en sucesivas líneas terapéuticas |
| Recomendación 15. En pacientes refractarios a varios tratamientos previos (sistémicos convencionales y biológicos), los anti-IL-17 y los anti-IL-23p19 deben considerarse una opción de tratamiento efectiva y segura |
| Recomendación 16. Usar otros tratamientos biológicos frente a los anti-TNF-α en presencia de enfermedad desmielinizante, insuficiencia cardiaca, ITL en ausencia de quimioprofilaxis, VHB anti-HBc(+)/HBAg(-) y lupus eritematoso u otras enfermedades autoinmunes. En el caso de iniciar el tratamiento con anti-TNF-α, se recomienda valorar clínicamente la función cardíaca antes de comenzar dicho tratamiento en esta subpoblación de pacientes |
| Recomendación 17. Intentar una optimización (disminución de dosis o aumento de intervalos) de los fármacos biológicos con respecto a la ficha técnica en los pacientes que logran la remisión |
Recomendación 1. Desarrollar cuestionarios de calidad de vida relacionada con la salud (CVRS) adaptados a los pacientes de edad avanzada con psoriasis en placas moderada-grave.
Dado que la CVRS de los pacientes ancianos con psoriasis se encuentra afectada tanto física como social y emocionalmente6, su tratamiento debe orientarse a mejorar todas las esferas de la enfermedad7,8. Por tanto, es adecuado evaluar su CVRS durante el seguimiento. Actualmente, existen distintos instrumentos para medir la CVRS de estos pacientes9,10, siendo el Dermatology Life Quality Index (DLQI) el más utilizado11. Sin embargo, muchos de estos pacientes no son capaces de cumplimentar autónomamente estos cuestionarios por problemas de comprensión o visión y dependen de un familiar/cuidador para realizarlos, limitándose en cierto modo su utilidad y/o validez. Además, algunos de los ítems incluidos (por ejemplo, la actividad sexual, laboral, o deportiva) pueden ser poco relevantes y distorsionar los resultados.
Recomendación 2. Evaluar la CVRS de las personas que conviven con los pacientes de edad avanzada con psoriasis en placas moderada-grave.
El impacto de la psoriasis no se limita al paciente, pudiendo afectar a familiares y convivientes que desempeñan un papel fundamental en su cuidado12. Por ello, también es recomendable evaluar la CVRS de las personas convivientes; siendo el DLQI familiar12 un instrumento adecuado para ello.
Bloque 2: educación adicionalRecomendación 3. Proporcionar, a lo largo del seguimiento y de forma periódica, educación adicional respecto al paciente de menor edad.
Las características propias del paciente anciano hacen que sus necesidades sean distintas a las de un paciente más joven13, siendo necesario fomentar el desarrollo de programas de apoyo y material visual educativo adaptado a este subgrupo de pacientes.
Bloque 3: vacunaciónRecomendación 4. Considerar la vacunación sistemática frente a herpes zóster (HZ) en pacientes de edad avanzada con psoriasis en placas moderada-grave.
El Ministerio de Sanidad recomienda incorporar la vacunación con la nueva vacuna recombinante y adyuvada frente al HZ (HZ/su) en mayores de 65 años independientemente de su patología de base o tratamientos pautados14,15 (tabla 4), ya que la prevalencia de la infección por HZ aumenta con la edad16. Además, enfermedades inmunomediadas como la psoriasis16 y ciertos fármacos sistémicos, como los anti-TNF-α, pueden estar asociados a un mayor riesgo de reactivación17–21.
Vacunación sistemática recomendada en pacientes ≥65 años
| Vacuna | Recomendación |
|---|---|
| Vacuna tétanos y difteria | Verificar el estado de vacunación previo antes de iniciar o completar una pauta de primovacunación con vacuna frente a tétanos y difteria (Td) en personas adultas. Se aprovechará el contacto con los servicios sanitarios para revisar el estado de vacunación y, en caso necesario, se vacunará con Td hasta completar 5 dosis. Se administrará una dosis de Td en torno a los 65 años a las personas que recibieron 5 dosis durante la infancia y la adolescencia |
| Vacuna neumococo | Se recomienda la vacunación frente a neumococo a partir de los 65 años con una dosis de vacuna polisacárida neumocócica de 23 serotipos (VPN23)* |
| Vacuna herpes zóster | Se recomienda la vacunación con HZ/su de la población a los 65 años (nacidos en 1958). Se administrarán 2 dosis separadas por un intervalo mínimo de 8 semanas. Además, se podrán captar progresivamente cohortes entre 66 y 80 años comenzando por la población que cumple 80 años** |
| Vacuna gripe anual | Se recomienda la vacunación con una dosis durante la campaña anual a las personas mayores, preferentemente a partir de los 65 años de edad |
Ya está disponible la nueva vacuna neumocócica conjugada de 20 serotipos (VNC20) que irá sustituyendo progresivamente a la VPN23.
Los casos infrecuentes de personas adultas ≥50 años sin evidencia de inmunidad frente a varicela, deben vacunarse frente a varicela con dos dosis. Los estudios clínicos con el uso de la vacuna de varicela en mayores de 65 años no incluyen un suficiente número de casos para determinar si la respuesta inmune es similar a la observada en personas jóvenes, aunque en las infrecuentes ocasiones en las que una persona de 50 o más años es seronegativa a varicela, debería, en ausencia de contraindicaciones, recibir dos dosis de vacuna.
Fuente: Ministerio de Sanidad56.
Recomendación 5. Promover el desarrollo de estudios en práctica clínica real que incluyan población anciana con psoriasis moderada-grave.
La evidencia científica sobre el curso natural de la enfermedad y las comorbilidades asociadas en pacientes de edad avanzada es muy limitada22, siendo necesaria la realización de estudios en práctica clínica real que incluyan a esta subpoblación y permitan generar evidencia sobre la historia natural de la enfermedad y la efectividad y seguridad de los tratamientos disponibles.
Bloque 5: tratamientoRecomendación 6. Orientar la elección del tratamiento a simplificar el régimen terapéutico.
Los pacientes de edad avanzada tienen necesidades terapéuticas concretas. Es necesario priorizar aspectos como la seguridad y la simplicidad posológica en la elección del tratamiento23,24. Por ello, los tratamientos con mejor perfil de seguridad, y con posologías más sencillas son los más recomendables en estos pacientes25.
Recomendación 7. Los tratamientos tópicos en monoterapia a largo plazo no deben considerarse una opción de tratamiento de primera línea, especialmente en ancianos con limitaciones físicas que no cuenten con asistencia para la aplicación del medicamento.
Los agentes tópicos presentan menos EA e interacciones farmacológicas que las terapias sistémicas, aspecto relevante en pacientes polimedicados26. Sin embargo, esta subpoblación tiene un mayor riesgo de atrofia cutánea con el uso de esteroides tópicos7,26. Asimismo, la adherencia a estos tipos de tratamiento suele ser baja a largo plazo27 y su uso puede ser inadecuado si existen limitaciones físicas y no se cuenta con asistencia para su aplicación26.
Recomendación 8. En los pacientes que reciben tratamiento sistémico convencional, las dosis deben ser generalmente más bajas y debe realizarse un control analítico y clínico más frecuente que en población de menor edad.
Existe cierta controversia en relación con el empleo del tratamiento sistémico convencional como primera línea en pacientes de edad avanzada. Dada su mala tolerabilidad y toxicidad acumulada órgano-específica27, junto con la posible mielosupresión asociada a la inmunosenescencia7, debe tenerse especial cuidado con su uso en este rango de edad11.
Recomendación 9. Iniciar el tratamiento con metotrexato a dosis bajas (5-7,5mg), y realizar una escalada progresiva de la dosis, en función de la tolerancia, la eficacia y la toxicidad. Se desaconseja su uso en pacientes que reciben antiinflamatorios no esteroideos, diuréticos, isoniazida, u otros medicamentos como penicilinas, sulfonamidas, antiepilépticos, colchicina, dipiridamol, etanol, sulfonilureas o trimetroprim-sulfametoxazol.
La edad avanzada se asocia a una mayor prevalencia de comorbilidades como dislipemia, diabetes, insuficiencia renal u obesidad que incrementan el riesgo de toxicidad asociada al metotrexato21,28. Por tanto, se ha sugerido iniciar el tratamiento con metotrexato a dosis bajas con escaladas progresivas si fuera necesario11,26. Asimismo, y de acuerdo con las indicaciones del producto, se desaconseja el tratamiento con metotrexato si se está recibiendo alguno de los tratamientos arriba indicados de manera concomitante.
Recomendación 10. Las dosis administradas de acitretina deben ser generalmente más bajas que en pacientes de menor edad, particularmente al inicio del tratamiento.
Aunque la eficacia de la acitretina21 es inferior a la de otros fármacos29, al no tratarse de un agente inmunosupresor tiene una posición única dentro de la estrategia terapéutica de la psoriasis30. Sin embargo, es necesario tener en cuenta algunos EA que pueden afectar particularmente a esta subpoblación, como son: 1) la sequedad cutáneo-mucosa, que puede agravar la xerosis propia de esta edad30; 2) la hipertrigliceridemia que aumenta el riesgo cardiovascular31; y 3) su contraindicación en pacientes con insuficiencia hepática o renal21, patologías que se hacen más prevalentes con la edad. Además, aunque las pautas posológicas para su administración no son diferentes en ancianos, las dosis bajas en pacientes de edad avanzada son más eficaces que en pacientes jóvenes21.
Recomendación 11. No se recomienda el uso de ciclosporina en el paciente de edad avanzada con psoriasis moderada-grave.
El riesgo de desarrollar toxicidad renal, infecciones graves o carcinogénesis aumenta con la edad11,25. Los pacientes ancianos también presentan mayor riesgo de hipertensión y de otros EA asociados a este fármaco7,29. Algunos medicamentos comúnmente administrados en este subgrupo de pacientes pueden afectar la farmacocinética y/o farmacodinámica de ciclosporina, recomendándose extremar la precaución al prescribirla en esta población21.
Recomendación 12. La edad del paciente como factor aislado no debe considerarse una limitación a la hora de elegir los tratamientos biológicos como opción terapéutica.
La eficacia del tratamiento para la psoriasis moderada-grave es similar independientemente de la edad32,33. A pesar de ello, en la práctica clínica, se prescriben menos fármacos biológicos a los pacientes de edad avanzada32.
Recomendación 13. Los tratamientos biológicos son, en su conjunto, más eficaces y mejor tolerados que los tratamientos sistémicos convencionales.
Los Informes de Posicionamiento Terapéutico (IPT)34–39 consideran los fármacos biológicos como una alternativa terapéutica en segunda línea para pacientes con psoriasis moderada-grave tras respuesta inadecuada, contraindicación o intolerancia a tratamientos sistémicos convencionales o PUVA. Sin embargo, la terapia biológica se asocia a mayor eficacia, menor probabilidad de toxicidad órgano-específica y mayor comodidad posológica en comparación con los agentes sistémicos convencionales7,21,25,40.
En cuanto a la seguridad de las terapias biológicas en pacientes de edad avanzada se han descrito pocos EA1,29,33,41–43. Por ello, su uso a largo plazo es más adecuado que el de los tratamientos sistémicos convencionales44, debido a su mejor tolerabilidad y seguridad21,27,40,41,45.
En cualquier caso, estos pacientes deben monitorizarse de forma estrecha por el mayor riesgo de infección7, y porque los EA graves tienden a ser más comunes a estas edades, independientemente de la modalidad terapéutica seleccionada32. No obstante, siempre que se tomen las medidas profilácticas adecuadas, los agentes biológicos son una opción segura y eficaz.
Recomendación 14. Los fármacos anti-IL-12/23p40 y anti-IL-23p19 son una buena opción de tratamiento debido a su comodidad posológica tanto en primera como en sucesivas líneas terapéuticas.
Los fármacos anti-IL23 en pacientes de edad avanzada con psoriasis moderada-grave son opciones seguras y efectivas33 que mejoran la CVRS de los pacientes21,32,44–49. Además, es probable que exista un menor riesgo de infección con los fármacos anti-IL-12/23p40 y anti-IL-23p19, en comparación con los agentes biológicos de primera generación y la terapia sistémica convencional7, presentando adicionalmente mayor comodidad posológica.
Recomendación 15. En pacientes refractarios a varios tratamientos previos (sistémicos convencionales y biológicos), los anti-IL-17 y los anti-IL-23p19 deben considerarse una opción de tratamiento efectiva y segura.
Los anti-IL-17 han demostrado ser tratamientos eficaces y seguros en la población de edad avanzada25. Los principales EA desarrollados con estos agentes no parecen diferir de los reportados en poblaciones más jóvenes a pesar de la mayor prevalencia de comorbilidades en pacientes de mayor edad46. Las candidiasis mucocutáneas serían la única consideración relevante asociada al uso de anti-IL-17 que podría aumentar su incidencia en esta población27.
Recomendación 16. Usar otros tratamientos biológicos frente a los anti-TNF-α en presencia de enfermedad desmielinizante, insuficiencia cardiaca (IC), infección tuberculosa latente (ITL) en ausencia de quimioprofilaxis, infección por virus de la hepatitis B (VHB) y lupus eritematoso u otras enfermedades autoinmunes. En el caso de iniciar el tratamiento con anti-TNF-α, se recomienda valorar clínicamente la función cardíaca antes de comenzar dicho tratamiento en esta subpoblación de pacientes.
Los anti-TNF-α deben prescribirse con precaución en pacientes con infecciones crónicas o estados portadores27,50 del VHB, ITL o episodios previos de HZ ya que están asociados a un pequeño, pero significativo, mayor riesgo de reactivación21, especialmente en pacientes con sistemas inmunes debilitados.
De igual forma, debe usarse con cautela en pacientes con lupus eritematoso u otras enfermedades autoinmunes27,50,51 y en pacientes con IC grado I-II NYHA7. Por último, la IC moderada-grave (NYHA III-IV) y la presencia de enfermedad desmielinizante contraindican de manera absoluta su uso.
Recomendación 17. Intentar una optimización (disminución de dosis o aumento de intervalos) de los fármacos biológicos con respecto a la ficha técnica en los pacientes que logran la remisión.
Las directrices actuales del GPS recomiendan priorizar la seguridad y consideran oportunas las estrategias de optimización respecto a la ficha técnica en aquellos pacientes que logran la remisión51.
DiscusiónEn el presente documento promovido por el GPS de la AEDV, se establecen una serie de recomendaciones prácticas para el manejo del paciente de edad avanzada con psoriasis en placas moderada-grave, sustentadas en una revisión de la literatura y consensuadas por un grupo de expertos, siguiendo la metodología Delphi.
El objetivo de estas recomendaciones es el de servir de soporte en la toma de decisiones a los clínicos y a otros actores implicados en el proceso asistencial (farmacéuticos y/o gestores), con el fin último de mejorar los resultados en salud de pacientes de edad avanzada con psoriasis en placas moderada-grave. En este rango de edad, el panel de expertos resalta la importancia de: 1) evaluar la CVRS de pacientes y familiares, 2) potenciar las medidas de apoyo y acompañamiento terapéutico, 3) simplificar el régimen terapéutico y 4) plantear la terapia biológica como opción más segura y eficaz que las terapias sistémicas clásicas.
Cabe señalar que algunos aspectos explorados en el Delphi no han alcanzado consenso. Así, a pesar de que existe evidencia sobre la eficacia y seguridad de la fototerapia en pacientes de edad avanzada21,52, no se alcanza consenso sobre su uso como primera línea de tratamiento. Del mismo modo, aunque existe evidencia sobre la eficacia y tolerabilidad de dimetilfumarato en estos pacientes53, la compleja posología inicial, así como la elevada frecuencia de EA gastrointestinales y la necesidad de monitorización analítica periódica54, dificulta considerarlo como opción ideal en esta subpoblación. Finalmente, si bien el perfil de seguridad de apremilast puede parecer interesante en esta subpoblación33, la compleja posología inicial, la mayor frecuencia de EA gastrointestinales y sus tasas de eficacia relativa respecto a la terapia biológica55, limita la priorización frente a otras alternativas.
El presente proyecto presenta algunas limitaciones inherentes a su metodología, donde el consenso se basa en la experiencia de los participantes. Las recomendaciones proceden del procedimiento metodológico descrito, y su aplicación debe contextualizarse dentro del sistema sanitario español.
ConclusionesEl consenso alcanzado ha permitido establecer recomendaciones específicas para el manejo del paciente de edad avanzada con psoriasis en placas moderada-grave. Estas recomendaciones pueden ayudar al dermatólogo prescriptor a tomar decisiones con mayor seguridad y a otros actores implicados en el cuidado de estos pacientes a conocer la evidencia científica disponible.
FinanciaciónEl proyecto ha sido impulsado y financiado por la Academia Española de Dermatología y Venereología con una beca sin restricciones de Almirall. Ninguna persona relacionada con Almirall ha participado en la elaboración de propuestas ni en la redacción de este manuscrito.
Los autores quieren agradecer a los miembros del GPS sus contribuciones al documento y a Outcomes’10 por el apoyo y coordinación metodológica del proyecto.