El comienzo de la psoriasis en la edad pediátrica, aunque generalmente leve, puede requerir tratamiento sistémico en las formas moderadas o graves de la enfermedad. El objetivo de este trabajo es analizar la frecuencia relativa, las características de los pacientes, el tratamiento empleado y los eventos adversos (EA) observados a partir del registro BIOBADADERM en niños y jóvenes con psoriasis moderada-grave. Del total de 3.946 pacientes del registro, se incluyen 24 pacientes menores de 21 años, con una edad media al inicio del tratamiento en BIOBADADERM de 16,1 años y un PASI medio de 9,4. El 67% de los pacientes estaba en tratamiento sistémico clásico al inicio del registro. Catorce pacientes (58%) suspendieron el tratamiento por pérdida o falta de eficacia o por EA. En conclusión, los datos del registro BIOBADADERM muestran que los menores representan un grupo muy pequeño dentro de los pacientes con psoriasis que reciben tratamiento sistémico y son manejados más frecuentemente con tratamientos clásicos.
Childhood-onset psoriasis generally follows an indolent course but patients with moderate or severe disease may require systemic treatment. The aim of this study was to determine the relative proportion of children and young people aged up to 21 years with moderate to severe psoriasis in the BIOBADADERM registry and to analyze the characteristics of these patients, treatments used, and adverse events. Of the 3946 patients in the registry, 24 were aged 21 years or younger. They had mean age of 16.1 years on starting treatment. When the registry was started, they had a Psoriasis Area and Severity Index of 9.4 and 67% were being treated with a conventional systemic drug. Treatment was discontinued in 14 patients (58%) due to adverse events or a loss or lack of effectiveness. In conclusion, the BIOBADADERM registry shows that young people account for a small proportion of psoriasis patients receiving systemic treatment, and they are more likely to be treated using conventional systemic drugs.
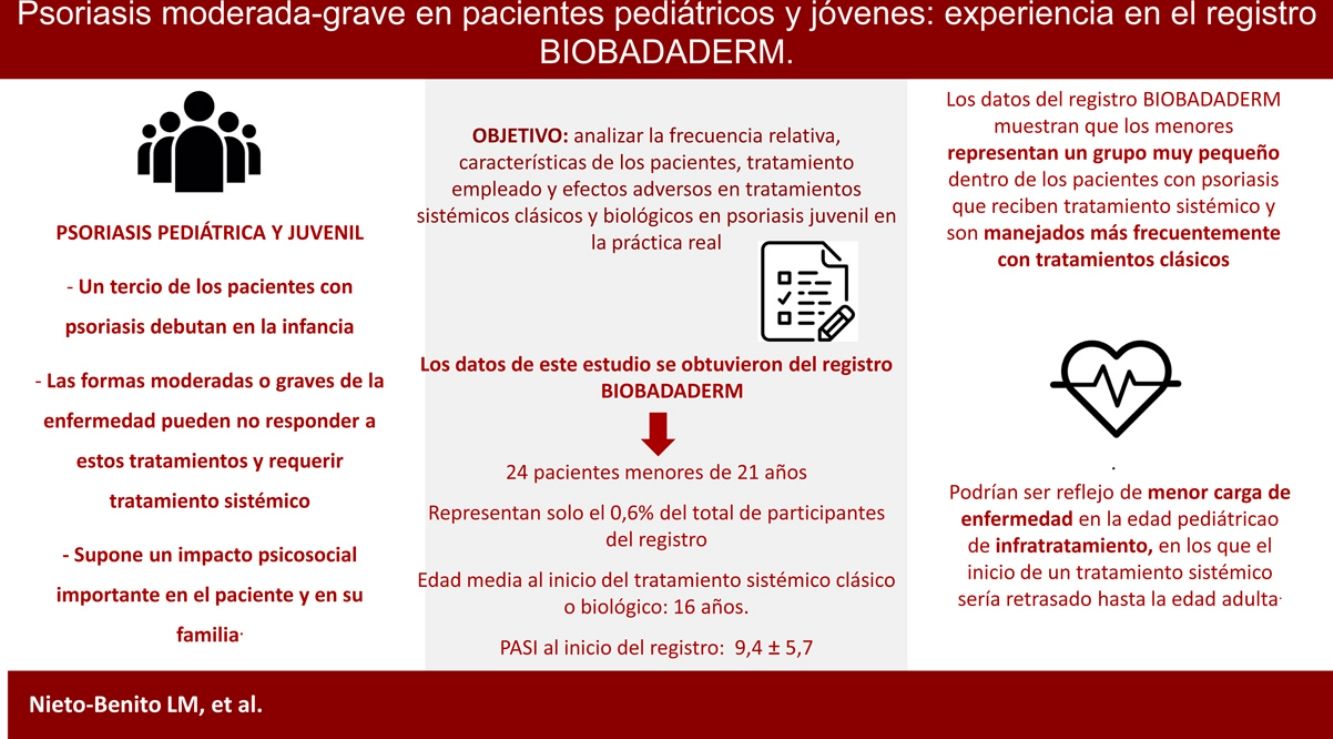
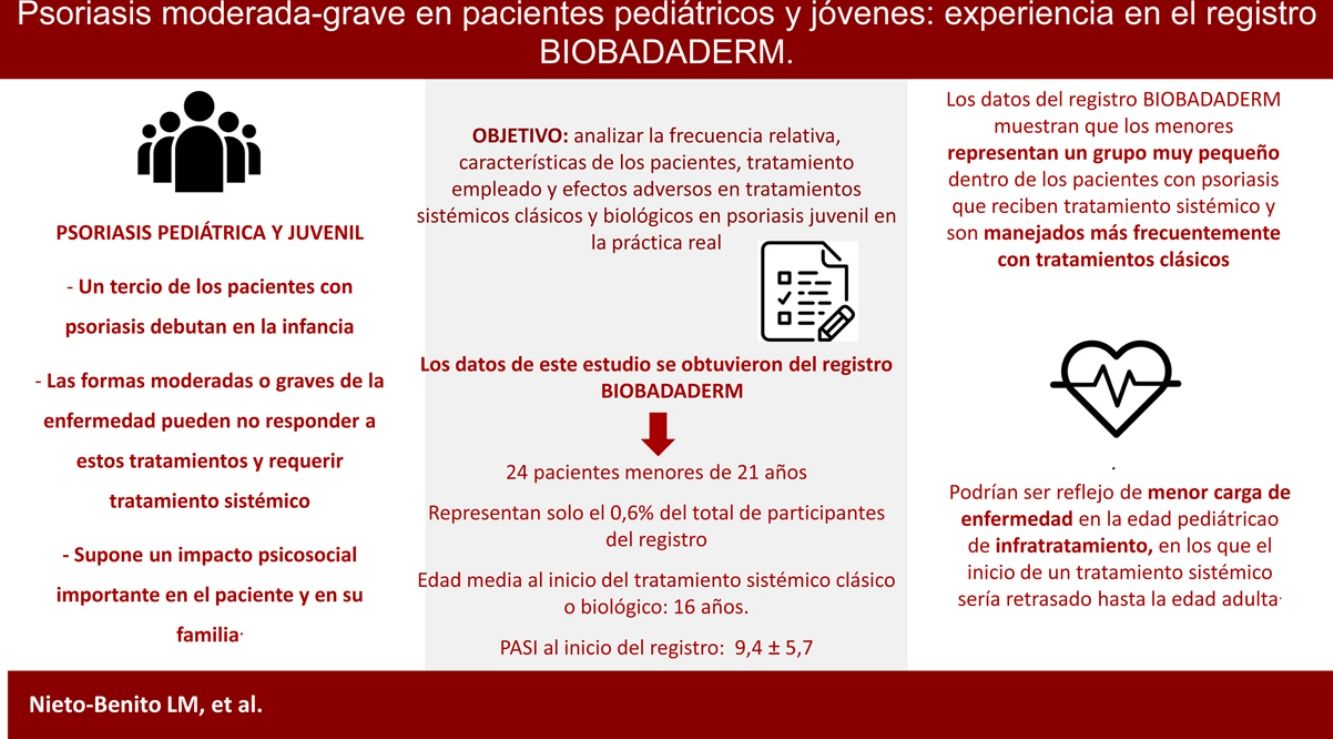
Un tercio de los pacientes con psoriasis comienzan en la infancia1, con una edad media al diagnóstico de 9 años. En la infancia y en la adolescencia, la psoriasis suele tener un curso leve y habitualmente suele controlarse con tratamientos tópicos y/o fototerapia2. Sin embargo, las formas moderadas o graves de la enfermedad pueden no responder a estos tratamientos y requerir tratamiento sistémico1,2.
El comienzo de la enfermedad en la edad pediátrica supone un impacto psicosocial importante en el paciente y en su familia2. Además, se relaciona con mayor comorbilidad cardiovascular y metabólica, por lo que, especialmente en casos graves, es necesaria una intervención precoz que pudiera contribuir a cambiar el curso inflamatorio de la enfermedad, y evitar complicaciones y secuelas posteriores3,4. Al ser un grupo etario vulnerable, es fundamental disponer de estudios que ofrezcan datos de seguridad a largo plazo e, idealmente, que avalen el ajuste de dosis por peso en estos pacientes2,4.
El objetivo de este trabajo es analizar la frecuencia relativa, las características de los pacientes y el tratamiento empleado en pacientes pediátricos, y conocer los efectos adversos (EA) de los tratamientos sistémicos en psoriasis juvenil en la práctica real.
Material y métodosLos datos de este estudio se obtuvieron del registro BIOBADADERM. Es un estudio impulsado por el Grupo de Psoriasis de la Academia Española de Dermatología y Venereología (AEDV), cuyo objetivo es analizar la seguridad de los tratamientos sistémicos en psoriasis. La descripción del estudio ha sido publicada previamente5,6.
Se recogieron las características demográficas y clínicas —incluyendo la forma clínica, así como la gravedad, Psoriasis Area Severity Index (PASI)— las comorbilidades, los tratamientos previos, el número de tratamientos realizados, los eventos adversos y la evolución de los pacientes incluidos en BIOBADADERM menores de 18 años incluidos en el registro hasta noviembre 2020. De forma análoga, se describieron también las características de los pacientes con edades comprendidas entre los 19 y 21 años.
BIOBADADERM fue aprobado por el Comité Ético de Investigación Clínica del Hospital Doce de Octubre (216/07, Madrid) y se realizó en conformidad con la Declaración de Helsinki. Todos los pacientes incluidos dieron su consentimiento por escrito y, en el caso de los menores de edad, lo hicieron sus padres y/o tutores legales.
Se realizó un análisis descriptivo. Las variables continuas se mostraron como medias con desviaciones estándar o medianas y rangos intercuartílicos. Las variables cualitativas se expresaron con porcentajes y valores absolutos. El análisis estadístico se realizó con Stata® (StataCorp. 2019. Stata Statistical Software: Release 16. College Station, TX: StataCorp LLC).
ResultadosDel total de 3.946 pacientes incluidos en el registro, 9 pacientes eran menores de 18 años y 15 de edades entre 19 y 21 años. Globalmente, presentaban una edad media al diagnóstico de la enfermedad de 16 (DE: 3,1) años y predominio del sexo masculino (71%). La duración media de enfermedad desde el diagnóstico hasta el inicio del tratamiento era de unos 5,5 (DE: 4,8) años y presentaban un PASI medio de 9,4 (DE: 5,7) al inicio del registro. A excepción de dos pacientes en el grupo de 19-21 años (hipertensión arterial e infección por VIH), el resto de los pacientes no presentaba comorbilidades.
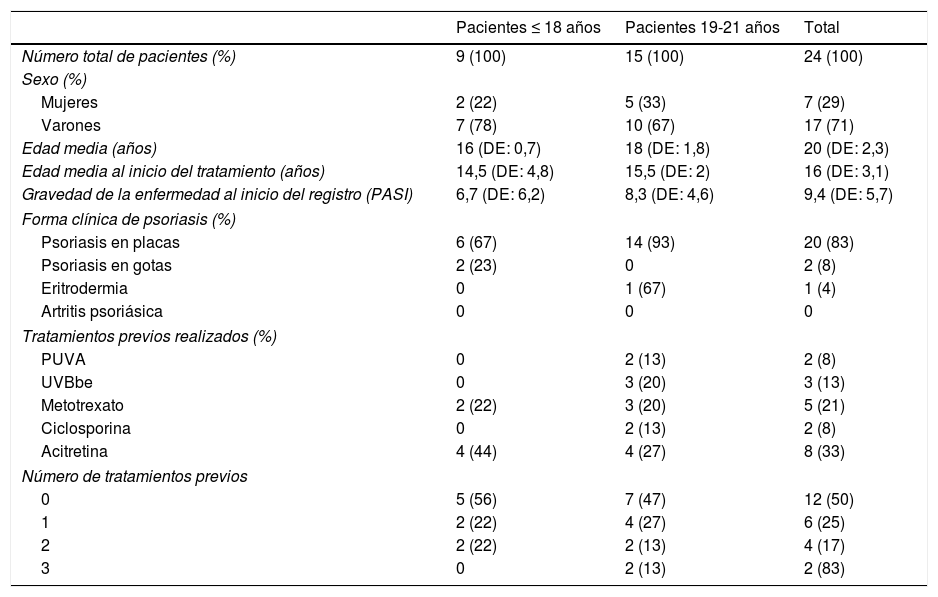
La forma clínica de psoriasis y los tratamientos previos realizados por ambos grupos se recogen en la tabla 1.
Descripción de las características epidemiológicas, clínicas y tratamientos previos realizados por los pacientes incluidos en el estudio
| Pacientes ≤ 18 años | Pacientes 19-21 años | Total | |
|---|---|---|---|
| Número total de pacientes (%) | 9 (100) | 15 (100) | 24 (100) |
| Sexo (%) | |||
| Mujeres | 2 (22) | 5 (33) | 7 (29) |
| Varones | 7 (78) | 10 (67) | 17 (71) |
| Edad media (años) | 16 (DE: 0,7) | 18 (DE: 1,8) | 20 (DE: 2,3) |
| Edad media al inicio del tratamiento (años) | 14,5 (DE: 4,8) | 15,5 (DE: 2) | 16 (DE: 3,1) |
| Gravedad de la enfermedad al inicio del registro (PASI) | 6,7 (DE: 6,2) | 8,3 (DE: 4,6) | 9,4 (DE: 5,7) |
| Forma clínica de psoriasis (%) | |||
| Psoriasis en placas | 6 (67) | 14 (93) | 20 (83) |
| Psoriasis en gotas | 2 (23) | 0 | 2 (8) |
| Eritrodermia | 0 | 1 (67) | 1 (4) |
| Artritis psoriásica | 0 | 0 | 0 |
| Tratamientos previos realizados (%) | |||
| PUVA | 0 | 2 (13) | 2 (8) |
| UVBbe | 0 | 3 (20) | 3 (13) |
| Metotrexato | 2 (22) | 3 (20) | 5 (21) |
| Ciclosporina | 0 | 2 (13) | 2 (8) |
| Acitretina | 4 (44) | 4 (27) | 8 (33) |
| Número de tratamientos previos | |||
| 0 | 5 (56) | 7 (47) | 12 (50) |
| 1 | 2 (22) | 4 (27) | 6 (25) |
| 2 | 2 (22) | 2 (13) | 4 (17) |
| 3 | 0 | 2 (13) | 2 (83) |
EPOC: enfermedad pulmonar obstructiva crónica; N: número; PASI: Psoriasis Área Severity Index; PUVA: fototerapia con luz ultravioleta A y psoraleno; UVBbe: luz ultravioleta de banda estrecha; VIH: virus de la inmunodeficiencia humana; %: porcentaje.
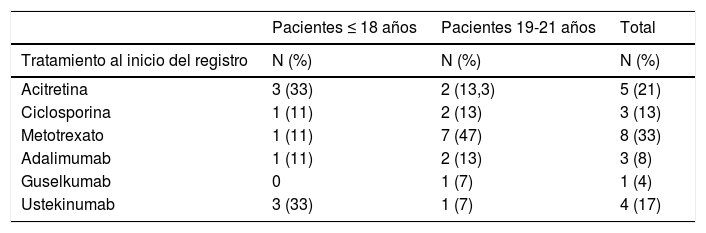
La mayoría de los pacientes incluidos en este estudio recibieron como primer tratamiento dentro del registro, un fármaco sistémico no biológico (67%): 5 recibieron tratamiento con acitretina, 3 con ciclosporina y 8 con metotrexato (tabla 2). En el grupo de pacientes que comenzaron con tratamiento biológico, ustekinumab fue el más frecuente, seguido de adalimumab y guselkumab. En el grupo de pacientes menores de 18 años, el tratamiento sistémico más frecuentemente prescrito a lo largo del seguimiento fue acitretina, a diferencia de los pacientes de 19-21 años, en los que fue metotrexato. El tiempo global de seguimiento para todos los pacientes fue de 38 personas/año.
Tratamientos realizados y efectos adversos notificados durante el registro BIOBADADERM
| Pacientes ≤ 18 años | Pacientes 19-21 años | Total | |
|---|---|---|---|
| Tratamiento al inicio del registro | N (%) | N (%) | N (%) |
| Acitretina | 3 (33) | 2 (13,3) | 5 (21) |
| Ciclosporina | 1 (11) | 2 (13) | 3 (13) |
| Metotrexato | 1 (11) | 7 (47) | 8 (33) |
| Adalimumab | 1 (11) | 2 (13) | 3 (8) |
| Guselkumab | 0 | 1 (7) | 1 (4) |
| Ustekinumab | 3 (33) | 1 (7) | 4 (17) |
| Ciclos de tratamiento | N (%) | N (%) | N (%) |
|---|---|---|---|
| Acitretina | 3 (23) | 3 (9) | 6 (13) |
| Ciclosporina | 1 (8) | 5 (15) | 6 (13) |
| Metotrexato | 1 (8) | 14 (42) | 15 (33) |
| Fumarato de dimetilo | 0 | 1 (3) | 1 (2) |
| Adalimumab | 2 (15) | 5 (3) | 7 (15) |
| Guselkumab | 0 | 1 (3) | 1 (2) |
| Risankizumab | 0 | 1 (3) | 1 (2) |
| Secukinumab | 1 (8) | 1 (3) | 2 (4) |
| Ustekinumab | 5 (39) | 2 (6) | 7 (15) |
| Total | 13 | 33 | 46 |
| Motivos de suspensión | N (% sobre total de pacientes) | N (% sobre total de pacientes) | N (% sobre total de pacientes) |
|---|---|---|---|
| Ineficacia o pérdida de eficacia | 2 (15) | 10 (30) | 12 (26) |
| Acontecimiento adverso | 2 (15) | 0 | 2 (4) |
| Remisión | 1 (8) | 8 (24) | 9 (20) |
| Suspensión preventiva por COVID-19 | 0 | 1 (3) | 1 (2) |
| Otros | 0 | 4 (12) | 4 (9) |
COVID-19: coronavirus disease-19; N: número; %: porcentaje.
De los 46 ciclos de tratamiento administrados, 28 (61%) fueron suspendidos, 14 (28%) de los cuales fueron por pérdida o falta de eficacia o por EA, perteneciendo cuatro de estos pacientes al grupo de menores de 18 años. Los EA que motivaron la suspensión fueron diarrea y náuseas asociadas a cefalea.
Del total de los 27 EA registrados, 5 fueron en menores de 18 años (ninguno de ellos considerado como grave) y 22 en pacientes de 19-21 años. En este grupo, se registraron dos EA infecciosos en pacientes diferentes que no condicionaron la suspensión del tratamiento: una otitis media aguda, en un paciente en tratamiento con acitretina y una apendicitis aguda, en otro paciente con risankizumab.
DiscusiónEn este estudio se recogieron los datos de los 24 pacientes menores de 21 años con diagnóstico de psoriasis incluidos en el registro BIOBADADERM, los cuales representaban solo el 0,6% del total de participantes. La edad media al inicio del tratamiento sistémico clásico o biológico entre los menores de 18 años fue de 14,5 años.
Estos datos podrían ser reflejo de la menor carga de enfermedad en la edad pediátrica, en la que la mayoría de los casos se controlaría con tratamiento tópico1,2 o de infratratamiento, en los que el inicio de un tratamiento sistémico sería retrasado hasta la edad adulta4,7.
La mayoría de la evidencia disponible en el tratamiento de la psoriasis moderada-grave en la edad pediátrica con tratamientos sistémicos clásicos y biológicos está basada en la experiencia descrita en adultos4. Aun así, los datos en seguridad y eficacia de los diferentes biológicos en la edad pediátrica está aumentando de forma considerable en los últimos años8–17. A día de hoy, existen 5 fármacos sistémicos biológicos aprobados por la European Medicines Agency (EMA) para el tratamiento de la psoriasis pediátrica: etanercept, ustekinumab, secukinumab, ixekizumab y adalimumab. Los 4 primeros tienen indicación para el tratamiento de psoriasis moderada-grave en placas en pacientes pediátricos mayores de 6 años, tras fallo o contraindicación a tratamientos sistémicos clásicos y/o fototerapia y, en el caso de adalimumab, en pacientes mayores de 4 años y como primera línea de tratamiento en psoriasis grave16.
Existen varios estudios retrospectivos que analizan las características y el tratamiento de pacientes menores de 18 años, con diagnóstico de psoriasis moderada-severa. Charbit et al.18 realizaron un estudio retrospectivo multicéntrico en el que se recogieron 154 pacientes. Presentaban una edad media al diagnóstico de 7,7 años y una edad media de inicio de tratamiento sistémico de 10,3 años. Acitretina fue el tratamiento más usado (55,2%) y prescrito como primera línea de tratamiento (76,6%); 34 pacientes de la serie precisaron tratamiento biológico. De los 261 ciclos de tratamiento, 15 tuvieron que ser suspendidos por EA. Ciclosporina fue el fármaco que más se asoció a EA graves, condicionando la suspensión del tratamiento (mialgias, trastornos gastrointestinales, hipertricosis).
Otro estudio19 recogió las características de 51 pacientes. Analizan los pacientes que reciben tratamiento sistémico clásico y biológico en monoterapia y/o en combinación. Metotrexato es el tratamiento no biológico más utilizado (27,5%) en monoterapia y combinado con fármaco biológico; solo un paciente recibió tratamiento con acitretina. El tratamiento biológico más usado fue etanercept (23 pacientes), seguido de adalimumab y ustekinumab. Se reportaron 29 EA del total de 80 ciclos de tratamiento. Los esquemas de tratamiento combinado no presentaron mayor número de EA, aunque el poder estadístico para detectar diferencias es bajo. El EA más frecuente en los pacientes en tratamiento con metotrexato fue la intolerancia gastrointestinal; solo un paciente recibía el tratamiento de forma subcutánea.
En nuestro medio, un estudio20 recogió un grupo de 40 pacientes menores de edad que presentaban una edad media al diagnóstico de psoriasis de 10,2 años y de inicio de tratamiento sistémico de 13,4 años. De los 63 ciclos de tratamiento y excluyendo 36 de los mismos (tratamiento con fototerapia), el tratamiento más usado en primera línea fue acitretina, pero, globalmente, fue metotrexato. Etanercept y acitretina fueron los tratamientos más prolongados. Describen un 11% de EA, ninguno de los cuales condicionó la suspensión del fármaco.
Con respecto al uso de tratamientos biológicos, Bronckers et al.8 realizaron un estudio retrospectivo de 390 pacientes, con una edad media de 11 años y 482 ciclos de tratamiento incluidos. El tratamiento biológico más usado fue etanercept, seguido de adalimumab, ustekinumab e infliximab. De los 270 pacientes que fueron tratados con metotrexato, el 48,1% experimentó algún EA, siendo 3 de ellos considerados como graves y condicionando la suspensión del tratamiento. Tres pacientes en tratamiento con fumaratos y 2 con adalimumab tuvieron que suspender el tratamiento por EA grave. No se observó ningún EA en los 2 pacientes tratados con infliximab.
Ollech et al.4 recogieron una serie de 10 pacientes con psoriasis grave; etanercept también fue el tratamiento biológico más prescrito. La edad media de inicio de tratamiento biológico fue de 12,6 años. Fue preciso el uso de una segunda línea en 6 casos y de una tercera, en 3. En cuanto a los EA, los dos casos que habían recibido tratamiento con infliximab tuvieron que ser suspendidos por reacción de hipersensibilidad al fármaco.
En conclusión, los datos del registro BIOBADADERM muestran que los menores representan un grupo muy pequeño dentro de los pacientes con psoriasis que reciben tratamiento sistémico y son manejados más frecuentemente con tratamientos clásicos, sin poder establecer si el motivo es por la menor gravedad o un posible infratratamiento.
FinanciaciónEl proyecto BIOBADADERM está promovido por la Fundación Piel Sana, Academia Española de Dermatología y Venereología, que cuenta con el apoyo económico de la Agencia Española de Medicamentos y Productos Sanitarios y de empresas farmacéuticas (Abbott/AbbVie, Amgen, Almirall, Janssen, Novartis y UCB). Las siguientes empresas también han colaborado en el pasado (Leo Pharma, Lilly, MSD y Pfizer). Las empresas farmacéuticas colaboradoras no han participado en el diseño y la realización del estudio; recopilación, gestión, análisis e interpretación de datos; preparación, revisión o aprobación del manuscrito; decisión de enviar el manuscrito para su publicación.
Conflicto de interesesLa Dra. Baniandrés-Rodríguez ha actuado como consultora y/o ponente para Janssen-Cilag, AbbVie, Pfizer, Novartis, Lilly, Celgene, Leo Pharma y Almirall.
El Dr. Carretero ha sido reembolsado por Janssen, AbbVie, Novartis, Pfizer, MSD y Celgene por servicios de asesoramiento y conferencias.
El Dr. Vilar-Alejo participó como AB de Janssen, Novartis, AbbVie, Almirall y Celgene.
La Dra. Rivera actuó como consultora y/o ponente y/o participó en ensayos clínicos como IP para AbbVie, Almirall, Celgene, Janssen, Leo Pharma, Lilly, Novartis, MSD y Pfizer-Wyeth.
El Dr. Carrascosa ha participado como ponente y/o asesor de Celgene, Janssen, Lilly, Novartis, Leo Pharma, Pfizer, MSD, AbbVie, Biogen Amgen.
El Dr. Dauden actuó como consultor para Abbott, Amgen, Astellas, Centocor Ortho Biotech Inc, Galderma, Glaxo, Jansenn-Cilag, Leo Pharma, Novartis, Pfizer, MSD y Celgene, recibió honorarios de Abbott, Amgen, Janssen-Cilag, Leo Pharma, Novartis, Pfizer, MSD, Celgene, participó en speakers bureau para Abbott, Pfizer, MSD y Janssen y recibió subvenciones de Pfizer, Abbott, Janssen y MSD.
El Dr. Herrera-Acosta ha desempeñado como consultor y/o ponente en Leo Pharma, Novartis, Janssen, Lilly, Celgene y AbbVie.
El Dr. Sahuquillo ha desempeñado como consultor y/o orador pagado y/o participado en ensayos clínicos patrocinados por compañías que fabrican medicamentos utilizados para el tratamiento de la psoriasis, incluidas AbbVie, Celgene, Janssen-Cilag, LEO Pharma, Lilly, Novartis y Pfizer.
El Dr. de la Cueva actuó como consultor y/o ponente para Janssen-Cilag, AbbVie, MSD, Pfizer, Novartis, Lilly, Almirall, UCB, Biogen, Celgene, Amgen, Sandoz, Sanofi y Leo-Pharma.
El Dr. López-Estebaranz participó como AB y recibió becas de Janssen, AbbVie, MSD, Lilly, Novartis, Leo Pharma, Pfizer.
La Dra. Belinchón actuó como consultora y/o ponente para y/o participó en ensayos clínicos patrocinados por empresas que fabrican medicamentos utilizados para el tratamiento de la psoriasis, incluidas Janssen Pharmaceuticals Inc, Almirall SA, Lilly, AbbVie, Novartis, Celgene, Biogen Amgen, Leo-Pharma, UCB, Pfizer-Wyeth y MSD.
La Dra. Ferran-Farrés ha participado como ponente o asesor de Janssen, Lilly, Novartis, Pfizer, MSD, Abbvie Celgene y Almirall.
La Dra. Rodríguez Fernández-Freire actuó como consultor y ponente para Janssen-Cilag, AbbVie, MSD, Pfizer, Novartis, Lilly, Almirall, Celgene y Leo-Pharma.
La Dra. García-Donoso participó como AB de AbbVie, Almirall y ponente de Janssen, Lilly y Celgene.
La Dra. Llamas-Velasco actuó como consultor y ponente y participó en ensayos clínicos para Janssen-Cilag, AbbVie, Celgene, Pfizer, Novartis, Lilly, Almirall y Leo-Pharma.
La Dra. Herrera-Ceballos se ha desempeñado como consultora y/o ponente para y/o participado en ensayos clínicos como IP y patrocinada por empresas que fabrican medicamentos utilizados para el tratamiento de la psoriasis, incluidas AbbVie, Janssen-Cilag, LEO Pharma, Lilly, Novartis y Pfizer.
El Dr. Botella-Estrada se ha desempeñado como consultor y/o orador pagado y/o participado en ensayos clínicos patrocinados por empresas que fabrican medicamentos utilizados para el tratamiento de la psoriasis, incluidas AbbVie, Celgene, Janssen-Cilag, LEO Pharma, Lilly, Novartis y Pfizer.
La Dra. Ruiz-Genao ha sido reembolsada por Pfizer, Janssen, Celgene, AbbVie, Novartis y LEO Pharma por servicios de asesoramiento y conferencias.
El Dr. Riera-Monroig recibió becas de viaje para congresos de AbbVie, Almirall, Janssen, LEO-Pharma y Novartis.
El Dr. García-Doval recibió becas de viaje para congresos de AbbVie, MSD y Pfizer.
Ninguno de los otros autores tiene intereses en conflicto que declarar.
A todos los participantes, tanto profesionales como pacientes, que participan en el registro BIOBADADERM.