La vasculopatía livedoide es una enfermedad trombo oclusiva crónica con una importante afectación cutánea1. Por ello, y debido a su carácter crónico, supone un reto terapéutico. Existen distintas alternativas de tratamiento que han demostrado su papel beneficioso en múltiples trabajos2,3. No obstante, en ocasiones hay cuadros refractarios de difícil control, por lo que la búsqueda de nuevas modalidades de terapia resulta relevante para el control de la enfermedad y el alivio sintomático de los pacientes.
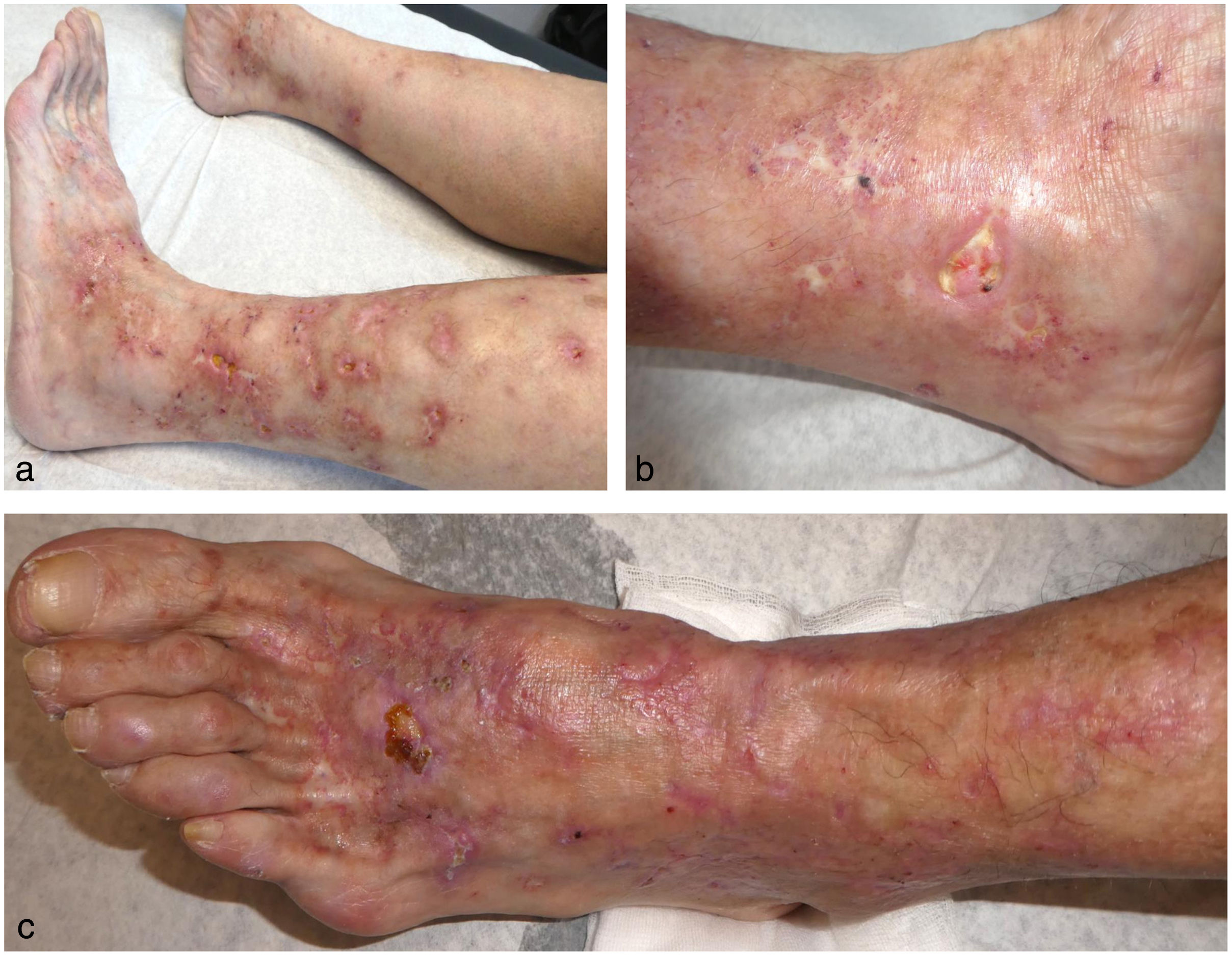
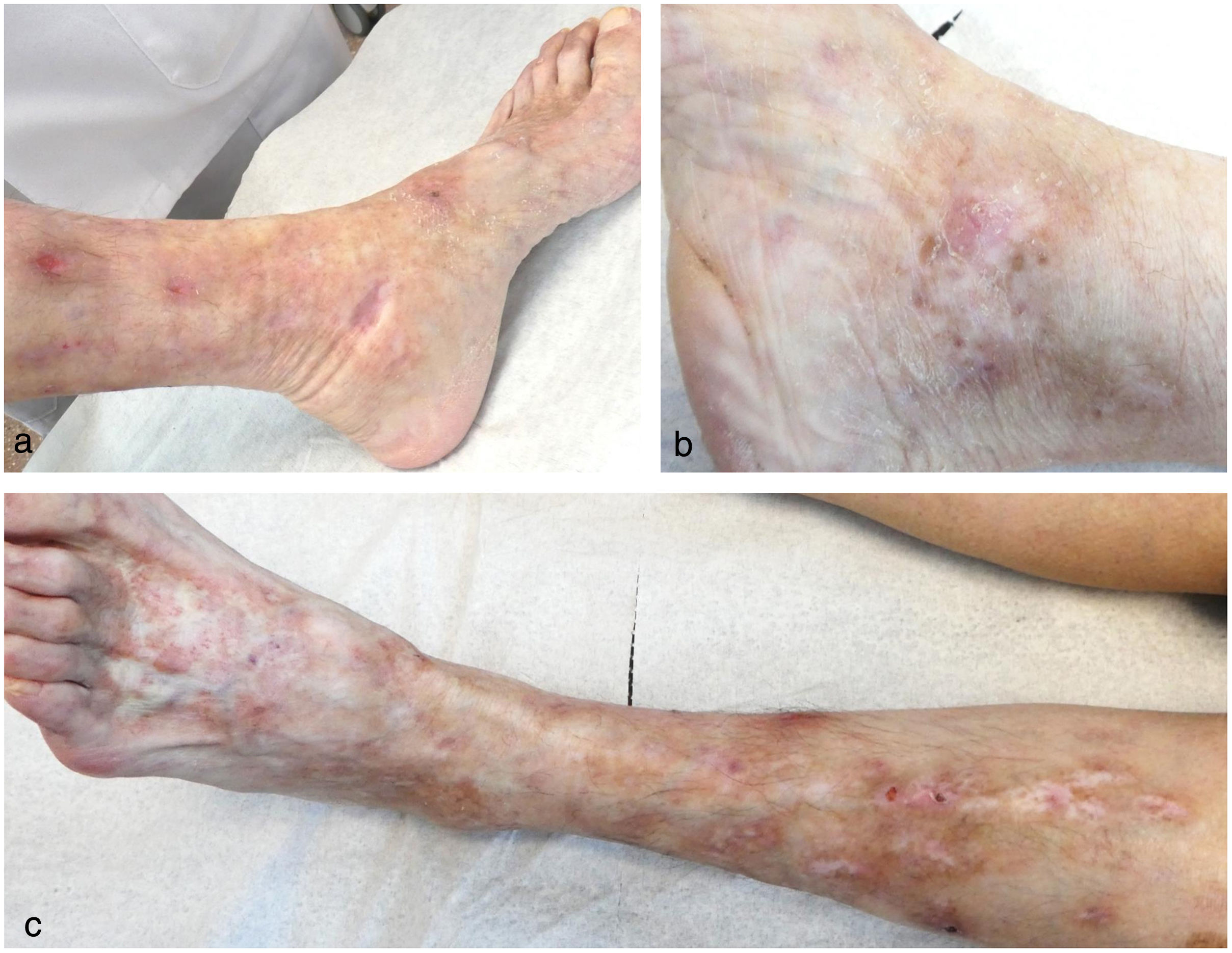
Una mujer de 68 años estaba en control dermatológico por padecer unos brotes de lesiones en piernas que, clínica e histológicamente, correspondían a vasculopatía livedoide de seis años de evolución (fig. 1). Los estudios para descartar alguna patología asociada (síndrome antifosfolípido, paraproteinemias, trastornos genéticos protrombóticos, enfermedades reumatológicas y autoinmunes) habían sido negativos. La paciente recibió tratamiento con múltiples fármacos tópicos, orales y parenterales (pentoxifilina, ácido acetilsalicílico, colchicina, nifedipino, bosentán, rivaroxabán, sildenafilo, nitroglicerina, inmunoglobulinas, rituximab y sevoflurano) suspendidos por falta de respuesta o intolerancia. Además, presentaba una mala tolerancia a diferentes analgésicos. Ante el curso tórpido y agresivo del cuadro, el mal control del dolor y de la afectación cutánea se derivó a la Unidad del Dolor, donde se le colocó un implante de estimulación de los cordones posteriores de la médula espinal. La mujer mostró una mejoría evidente del dolor y una resolución prácticamente completa de las úlceras cutáneas, con una respuesta mantenida durante los meses siguientes (fig. 2).
La vasculopatía livedoide es un trastorno cutáneo crónico infrecuente, con un importante impacto en la calidad de vida. La clínica se caracteriza por la presencia de úlceras persistentes, muy dolorosas, que afectan fundamentalmente a las piernas de manera bilateral. Además, los pacientes muestran una livedo racemosa y áreas de atrofia blanca1. El diagnóstico se confirma con la histología característica que consiste en la presencia de trombosis intraluminal, proliferación endotelial y degeneración hialina subíntima de la vasculatura dérmica4. Tras la confirmación histopatológica, debemos descartar que hayan enfermedades sistémicas asociadas, tales como el síndrome antifosfolípido primario, el lupus eritematoso sistémico, la artritis reumatoide, la esclerosis sistémica o la enfermedad mixta del tejido conectivo5.
Las distintas modalidades de tratamiento suelen ofrecer resultados desiguales, por lo que generalmente son precisos los procedimientos combinados o secuenciales, aunque con un nivel de evidencia bajo2,3. Por un lado, es importante llevar a cabo medidas generales, tales como el control del dolor, la cura de las heridas y la terapia compresiva3,4. Por otro lado, se utilizan medidas terapéuticas dirigidas a disminuir el riesgo de trombosis, por ejemplo, antiagregantes, anticoagulantes y agentes fibrinolíticos; así como agentes inmunomoduladores y vasodilatadores3.
El implante de electrodos sobre los cordones posteriores medulares actúa mediante dos vías: una inhibición centrípeta, impidiendo el impulso nervioso desde las terminaciones nerviosas periféricas hasta el sistema nervioso central, lo que evita que se haga consciente la sensación de dolor; y una inhibición centrífuga, la cual imposibilita que se genere un impulso nervioso simpático, favoreciendo la vasodilatación periférica, la perfusión de territorios distales y disminuye el dolor6,7. Esto en nuestra paciente se tradujo en una mejoría satisfactoria de las úlceras y de la intensidad del malestar. Su uso en otras vasculopatías se ha recogido en la literatura, pero hasta la fecha no hay publicado ningún caso de vasculopatía livedoide tratada satisfactoriamente con dicha modalidad8. Esta técnica es bastante segura con una incidencia de complicaciones de 5,3-40%9. Entre ellas encontramos la infección quirúrgica7,9 (2,5-10%9) y las complicaciones mecánicas como migración (2,1-27%9) o rotura (0-9,1%) del cable, molestias producidas por el generador de impulsos (0,9-12%7,9) y mal funcionamiento del dispositivo (0-10,2%9). La complicación más grave es el daño neurológico (0,4-2,1%10) que puede consistir en el desarrollo de un hematoma epidural (0,3%), déficit neurológico mayor (0,25%), déficit motor limitado (0,1%), cambios autonómicos (0,013%) o déficit sensorial (0,1%)9. No obstante, estos porcentajes han ido disminuyendo en incidencia gracias a la mejora tecnológica y el perfeccionamiento de las técnicas de implantación9.
La formación de un hematoma epidural es rara, se ha observado principalmente tras la inserción quirúrgica del dispositivo y puede derivar en daño neurológico permanente. Este riesgo está incrementado en los pacientes antiagregados o anticuagulados, por lo que existen guías para prevenirlo. La incidencia de aparición de hematomas epidurales en aquellos bajo tratamiento con anticoagulantes o antiagregantes es desconocida y el manejo debe ser individualizado10.
La estimulación de cordones posteriores puede considerarse una alternativa en el tratamiento de pacientes con vasculopatía livedoide que no respondan a otras opciones clásicas.