En España se carece de evidencia sobre psoriasis (PsO) pediátrica en el mundo real. El objetivo de este estudio fue identificar la carga de la enfermedad reportada por el facultativo y los patrones actuales de tratamiento en una cohorte de pacientes psoriásicos pediátricos en el mundo real. Ello ampliará nuestra comprensión de la enfermedad y contribuirá al desarrollo de directrices regionales.
Material y métodoEste análisis retrospectivo transversal de una encuesta de investigación mercado evaluó las necesidades clínicas no satisfechas y los patrones de tratamiento en pacientes con PsO pediátrica en España, según lo reportado por sus médicos de atención primaria y especialistas, utilizando datos recopilados como parte del Disease-Specific Program (DSP™) de Adelphi para PsO pediátrica en el mundo real, entre los meses de febrero y octubre de 2020.
ResultadosSe incluyeron los datos de la encuesta realizada a 57 facultativos médicos tratantes (71,9% [n = 41] de dermatólogos, 17,6% [n = 10] de médicos generales de atención primaria y 10,5% [n = 6] de pediatras); el análisis final incluyó 378 pacientes. En la muestra, 84,1% (318/378) de los pacientes padeció enfermedad leve, 15,3% (58/378) enfermedad moderada y 0,5% (2/378) enfermedad severa. De acuerdo con el reporte retrospectivo, la gravedad juzgada por el facultativo en el momento de diagnosticarse la PsO pediátrica registró 41,8% (158/378) de pacientes con enfermedad leve, 51,3% (194/378) con enfermedad moderada y 6,9% (26/378) con enfermedad severa. En general, 89,3% (335/375) de los pacientes recibía en la actualidad terapia tópica para PsO pediátrica, mientras que 8,8% (33/375), 10,4% (39/375) y 14,9% (56/375) de los pacientes recibían en la actualidad fototerapia, sistémicos y biológicos convencionales, respectivamente.
ConclusionesEstos datos del mundo real reflejan la carga actual y el panorama de la PsO pediátrica en España. El manejo de los pacientes pediátricos podría mejorar, formando aún más a los profesionales sanitarios y desarrollando directrices regionales.
Real-world evidence of paediatric psoriasis (PsO) is lacking in Spain. The purpose of this study was to identify physician-reported disease burden and current treatment patterns in a real-world paediatric PsO patient cohort in Spain. This will enhance our understanding of the disease and contribute to the development of regional guidelines.
Material and methodThis retrospective analysis of a cross-sectional market research survey assessed the clinical unmet needs and treatment patterns in patients with paediatric PsO in Spain, as reported by their primary care and specialist physicians, using data collected as part of the Adelphi Real World Paediatric PsO Disease-Specific Program (DSP™) between February and October 2020.
ResultsSurvey data from 57 treating physicians were included (71.9% [N = 41] dermatologists, 17.6% [N = 10] general practitioners/primary care physicians, and 10.5% [N = 6] paediatricians); the final analysis included 378 patients. At sampling, 84.1% (318/378) of patients had mild disease, 15.3% (58/378) had moderate disease and 0.5% (2/378) had severe disease. Retrospectively reported physician-judged severity at the time of PsO diagnosis recorded 41.8% (158/378) of patients with mild disease, 51.3% (194/378) with moderate disease and 6.9% (26/378) with severe disease. Overall, 89.3% (335/375) of patients were currently receiving topical PsO therapy, while 8.8% (33/375), 10.4% (39/375) and 14.9% (56/375) of patients were currently receiving phototherapy, conventional systemics and biologics, respectively.
ConclusionsThese real-world data reflect the current burden and treatment landscape of paediatric PsO in Spain. The management of patients with paediatric PsO could be improved by further educating healthcare professionals and developing regional guidelines.
La psoriasis (PsO) es una enfermedad sistémica crónica de la piel con una implicación tanto física como psicológica1. Aproximadamente un tercio de los pacientes desarrollarán la enfermedad antes de los 16 años, con una edad media de 8 a 11 años. La PsO en niños y adolescentes afecta aproximadamente a 0,5-1,2% de la población, y la prevalencia aumenta de forma lineal, siendo de 0,1% en niños de un año, llegando a ser de 1,2% a los 18 años2–4. La PsO tiene un profundo impacto en la calidad de vida (CdV) de los niños5.
Las guías europeas y americanas (EE. UU.) de PsO6,7 recomiendan múltiples formas para poder evaluar la gravedad de la enfermedad, incluida el área de superficie corporal (BSA), la Evaluación global del médico (PGA), el Índice de gravedad y área de psoriasis (PASI) y el Índice de gravedad en los niños, «Dermatology Life Quality Index» infantil (DLQI) (CDLQI)6,7. A pesar de que existen guías generales para el manejo de la PsO en Europa y EE. UU., se carece de guías regionales para la PsO pediátrica en España.
La mayoría de los pacientes pediátricos con PsO leve se manejan de manera satisfactoria utilizando solo terapias tópicas, sin embargo, la fototerapia y las terapias sistémicas pueden ser necesarias para tratar la PsO moderada y grave8. Los tratamientos sistémicos convencionales no biológicos a menudo se usan sin indicación en Europa y EE. UU.3 En Galicia, España, la fototerapia, seguida del metotrexato, son los tratamientos más comunes para la PsO de moderada a grave en niños menores de 18 años9.
Actualmente, existen cinco agentes biológicos aprobados por la Agencia Europea de Medicamentos (EMA) para el tratamiento de la PsO pediátrica de moderada a grave: adalimumab (≥ 4 años), etanercept (≥ 6 años), secukinumab (≥ 6 años), ustekinumab (≥ 6 años) e ixekizumab (≥ 6 años con un peso > 25 kg)10–13. Los resultados del registro BIOBADADERM14 demuestran que los pacientes pediátricos (hasta 21 años) representan solo un pequeño número de pacientes con PsO tratados con biológicos. Los pacientes pediátricos fueron tratados más comúnmente con tratamientos sistémicos convencionales15. Sin embargo, no fue posible establecer si esto se debió a un tratamiento insuficiente o a una menor carga de enfermedad grave en este grupo15.
Seyger et al. informaron que, a pesar de recibir tratamiento para la PsO, los pacientes pediátricos presentaron puntajes altos de BSA, PASI y PGA, así como muchos síntomas y áreas afectadas. Si bien esto fue más llamativo en los pacientes con PsO moderada o grave, se observó que los pacientes con una PsO leve, presentaban una carga de enfermedad persistente16. Un estudio realizado en Europa concluyó que los niños de mayor edad y con mayor peso que fueron tratado con productos biológicos, presentaban predominantemente una psoriasis más severa, y las prescripciones de tratamientos biológicos solo se indicaban después de la ausencia de respuesta a otros tratamientos17. El presente estudio es la continuación del estudio de Seyger et al., e incluye datos recopilados de la población pediátrica con psoriasis en España16.
Material y métodosDiseño del estudioEn este estudio se realizó un análisis de tipo retrospectivo, utilizando una encuesta tranversal de estudio de mercado, utilizando datos recopilados como parte del Disease-Specific Program (DSP™) Adelphi de PsO pediátrica. Los métodos y el diseño del estudio fueron descritos previamente por Seyger et al.16 Los datos se recopilaron entre febrero y octubre de 2020.
El estudio reclutó a dermatólogos, médicos generales o de atención primaria (GP/PCP) y pediatras que manejaban activamente a los pacientes pediátricos con PsO. Los pacientes tenían entre cuatro y 17 años y habían recibido algún tratamiento para la PsO. Por dermatólogo se incluyeron al menos dos pacientes que utilizaban en la actualidad o habían utilizado terapia biológica previamente. Asimismo, se incluyeron pacientes que habían recibido múltiples clases de tratamiento en tándem (por ejemplo, terapia sistémica convencional y tópica, o terapia biológica y sistémica convencional).
Objetivos del estudioEl objetivo principal de este estudio fue describir las necesidades clínicas insatisfechas notificadas por los médicos entre la población pediátrica con PsO en España. El objetivo secundario fue describir los patrones de tratamiento actuales entre la población pediátrica con PsO en España16.
Gravedad de la enfermedadComo se observó anteriormente16, la gravedad de la enfermedad fue determinada según el criterio del médico, sin que se definieran criterios clínicos previamente. Los médicos pueden haber considerado utilizar diversos factores para definir de manera subjetiva la gravedad de la enfermedad de un paciente (por ejemplo, BSA, PASI, síntomas actuales y áreas afectadas). Si bien este estudio se basa en una encuesta transversal, con datos relacionados con el momento del muestreo (o «en la actualidad»), las clasificaciones de gravedad determinadas por los médicos también se recopilaron de modo retrospectivo en el momento del diagnóstico.
Los datos se han presentado con el grado de la gravedad agrupada en los siguientes puntos (fig. 1A): En el momento del muestreo («actualmente»; Análisis 1), en el momento del primer diagnóstico de PsO (Análisis 2) y en el momento del inicio del tratamiento actual (Análisis 3). Los resultados de BSA, PASI y gravedad a juicio del médico también se registraron retrospectivamente (Análisis 2/3) y en el muestreo (Análisis 1); todos los demás resultados se registraron solo en el momento del muestreo. Para los análisis específicos con respecto a los patrones de tratamiento, los pacientes con enfermedad moderada o grave se agruparon (denominados «enfermedad moderada a grave»), ya que ambas categorías son elegibles para el tratamiento escalonado con agentes sistémicos.
Cambio en la gravedad de la enfermedad del paciente y recopilación de datos. A) Esquema que ilustra la recopilación de los datos acerca de la gravedad recogido de manera retrospectiva (en el momento del diagnóstico, en el momento del inicio del tratamiento utilizado en la «actualidad» y en el momento del muestreo [actualmente]). B) Esquema que muestra la frecuencia de pacientes con PsO leve, moderada y grave, según la categorización en el momento del primer diagnóstico de PsO (retrospectivo) frente al momento del muestreo (actualmente).
n: número de pacientes con resultado; N: número total de pacientes en el grupo; Pso: psoriasis.
Los datos también se filtraron para determinar con precisión las necesidades clínicas insatisfechas en la población de estudio. Se utilizaron los siguientes filtros:
- •
Excluir pacientes con una duración de tratamiento < 4 semanas para terapia tópica y/o < 12 semanas para terapia convencional sistémica y/o biológica.
- •
Un análisis adicional del subconjunto de pacientes que actualmente no experimentaban brotes de PsO.
Los datos continuos se informan como media ± desviación estándar (DE) a menos que se indique lo contrario, y los datos categóricos se presentan como porcentaje y como n/N (donde n = número de pacientes con resultado y N = número de pacientes con los datos disponibles).
Consideraciones regulatorias y éticasLa encuesta se llevó a cabo de conformidad con la Asociación Europea de Investigación del Mercado Farmacéutico y en plena conformidad con la Ley de Portabilidad y Responsabilidad de Seguros Médicos de EE. UU. de 1996. La Junta de Revisión Institucional del grupo Western Copernicus otorgó la aprobación ética.
ResultadosPoblaciónEn el estudio se incluyeron datos de 57 médicos de España que pautaban tratamientos (71,9% [n = 41] dermatólogos, 17,6% [n = 10] médicos de cabecera y 10,5% [n = 6] pediatras), completando un total de 477 registros de pacientes. Cada registro de paciente representaba un solo paciente con PsO pediátrica. Para garantizar un tiempo de respuesta al tratamiento suficiente, los pacientes con un tiempo de tratamiento < 4 semanas para la terapia tópica y/o < 12 semanas para la terapia sistémica y/o biológica convencional se eliminaron de la población global para todos los análisis posteriores, dejando una población total de 378 pacientes (tabla 1).
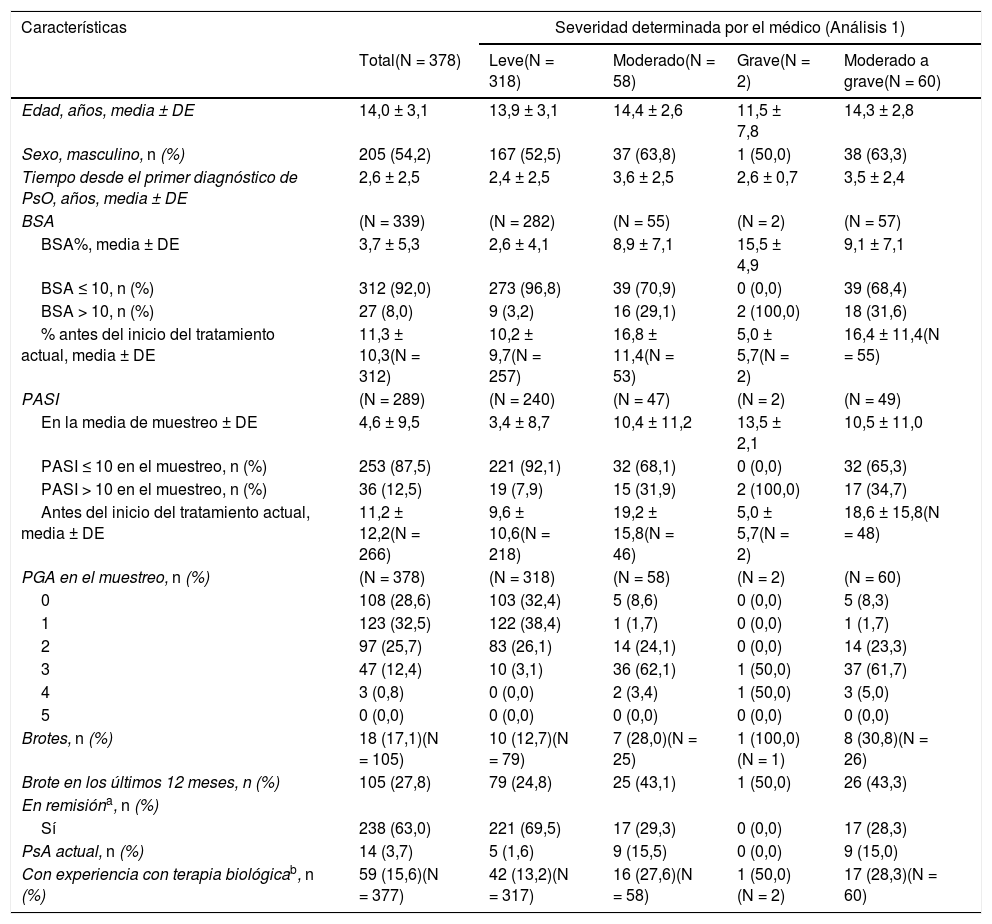
Características de la enfermedad, en general y según la gravedad de la enfermedad determinada por el médico en el momento del muestreo (Análisis 1)
| Características | Severidad determinada por el médico (Análisis 1) | ||||
|---|---|---|---|---|---|
| Total(N = 378) | Leve(N = 318) | Moderado(N = 58) | Grave(N = 2) | Moderado a grave(N = 60) | |
| Edad, años, media ± DE | 14,0 ± 3,1 | 13,9 ± 3,1 | 14,4 ± 2,6 | 11,5 ± 7,8 | 14,3 ± 2,8 |
| Sexo, masculino, n (%) | 205 (54,2) | 167 (52,5) | 37 (63,8) | 1 (50,0) | 38 (63,3) |
| Tiempo desde el primer diagnóstico de PsO, años, media ± DE | 2,6 ± 2,5 | 2,4 ± 2,5 | 3,6 ± 2,5 | 2,6 ± 0,7 | 3,5 ± 2,4 |
| BSA | (N = 339) | (N = 282) | (N = 55) | (N = 2) | (N = 57) |
| BSA%, media ± DE | 3,7 ± 5,3 | 2,6 ± 4,1 | 8,9 ± 7,1 | 15,5 ± 4,9 | 9,1 ± 7,1 |
| BSA ≤ 10, n (%) | 312 (92,0) | 273 (96,8) | 39 (70,9) | 0 (0,0) | 39 (68,4) |
| BSA > 10, n (%) | 27 (8,0) | 9 (3,2) | 16 (29,1) | 2 (100,0) | 18 (31,6) |
| % antes del inicio del tratamiento actual, media ± DE | 11,3 ± 10,3(N = 312) | 10,2 ± 9,7(N = 257) | 16,8 ± 11,4(N = 53) | 5,0 ± 5,7(N = 2) | 16,4 ± 11,4(N = 55) |
| PASI | (N = 289) | (N = 240) | (N = 47) | (N = 2) | (N = 49) |
| En la media de muestreo ± DE | 4,6 ± 9,5 | 3,4 ± 8,7 | 10,4 ± 11,2 | 13,5 ± 2,1 | 10,5 ± 11,0 |
| PASI ≤ 10 en el muestreo, n (%) | 253 (87,5) | 221 (92,1) | 32 (68,1) | 0 (0,0) | 32 (65,3) |
| PASI > 10 en el muestreo, n (%) | 36 (12,5) | 19 (7,9) | 15 (31,9) | 2 (100,0) | 17 (34,7) |
| Antes del inicio del tratamiento actual, media ± DE | 11,2 ± 12,2(N = 266) | 9,6 ± 10,6(N = 218) | 19,2 ± 15,8(N = 46) | 5,0 ± 5,7(N = 2) | 18,6 ± 15,8(N = 48) |
| PGA en el muestreo, n (%) | (N = 378) | (N = 318) | (N = 58) | (N = 2) | (N = 60) |
| 0 | 108 (28,6) | 103 (32,4) | 5 (8,6) | 0 (0,0) | 5 (8,3) |
| 1 | 123 (32,5) | 122 (38,4) | 1 (1,7) | 0 (0,0) | 1 (1,7) |
| 2 | 97 (25,7) | 83 (26,1) | 14 (24,1) | 0 (0,0) | 14 (23,3) |
| 3 | 47 (12,4) | 10 (3,1) | 36 (62,1) | 1 (50,0) | 37 (61,7) |
| 4 | 3 (0,8) | 0 (0,0) | 2 (3,4) | 1 (50,0) | 3 (5,0) |
| 5 | 0 (0,0) | 0 (0,0) | 0 (0,0) | 0 (0,0) | 0 (0,0) |
| Brotes, n (%) | 18 (17,1)(N = 105) | 10 (12,7)(N = 79) | 7 (28,0)(N = 25) | 1 (100,0)(N = 1) | 8 (30,8)(N = 26) |
| Brote en los últimos 12 meses, n (%) | 105 (27,8) | 79 (24,8) | 25 (43,1) | 1 (50,0) | 26 (43,3) |
| En remisióna, n (%) | |||||
| Sí | 238 (63,0) | 221 (69,5) | 17 (29,3) | 0 (0,0) | 17 (28,3) |
| PsA actual, n (%) | 14 (3,7) | 5 (1,6) | 9 (15,5) | 0 (0,0) | 9 (15,0) |
| Con experiencia con terapia biológicab, n (%) | 59 (15,6)(N = 377) | 42 (13,2)(N = 317) | 16 (27,6)(N = 58) | 1 (50,0)(N = 2) | 17 (28,3)(N = 60) |
Cuando el número total de pacientes no estaba disponible, el número de pacientes por grupo se indica en la tabla (n). Debido al redondeo, es posible que algunos porcentajes no sumen 100%.
BSA: área de superficie corporal; N: número total de pacientes por grupo; n: número de pacientes con resultado; PASI: área de psoriasis e índice de severidad; PGA: Evaluación global del médico; PsA: artritis psoriásica; PsO: psoriasis; DE: desviación estándar.
La tabla 1 detalla las características clínicas generales de los pacientes con PsO pediátrica en el momento del muestreo (Análisis 1). En el momento del muestreo, el 84,1% (318/378) de los pacientes tenía enfermedad leve y el 15,9% (60/378) tenía enfermedad de moderada a grave. La evaluación de la gravedad por el médico en el momento del diagnóstico de la PsO (Análisis 2) registró un 41,8% (158/378) de pacientes con enfermedad leve y un 58,2% (220/378) con enfermedad de moderada a grave (fig. 2B).
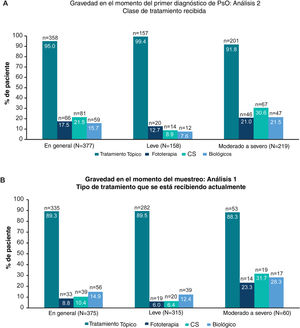
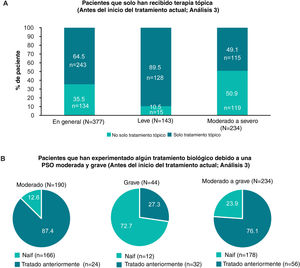
Clases de tratamiento recibidas alguna vez según la gravedad del primer diagnóstico (Análisis 2) y clases de tratamiento que se pautan actualmente, según la gravedad en el momento del muestreo (Análisis 1). Debido al redondeo, es posible que los datos no sumen 100%. A) Gráficos de barras que muestran la proporción de pacientes que alguna vez recibieron terapia tópica, fototerapia, CS y terapia biológica (incluidos los biosimilares) en general y en pacientes con enfermedad leve y moderada a grave a juicio del médico en el momento del primer diagnóstico (Análisis 2). B) Gráficos de barras que muestran la proporción de pacientes que actualmente reciben terapia tópica, fototerapia, CS y terapia biológica (incluidos los biosimilares) en general y en pacientes con enfermedad leve y moderada a grave a juicio del médico en el momento del muestreo (Análisis 1).
CS: tratamiento sistémico convencional; n: número de pacientes con resultado; N: número total de pacientes en el grupo; Pso: psoriasis.
Utilizando los datos de gravedad entre el momento del diagnóstico y el momento de la toma de muestras (fig. 1A), se pudieron determinar las necesidades insatisfechas de los pacientes (fig. 1B [Análisis 2 vs. Análisis 1]). De los pacientes con enfermedad leve en el momento del diagnóstico (41,8% [158/378]), 7,6% (12/158) progresó a enfermedad moderada en el momento del muestreo. De los pacientes con enfermedad moderada en el momento del diagnóstico (51,3% [194/378]), 18,6% (36/194) todavía tenía enfermedad moderada y 0,5% (1/194) progresó a enfermedad grave. De los pacientes con enfermedad grave en el momento del diagnóstico (6,9% [26/378]), 38,5% (10/26) tenía enfermedad moderada en el momento del muestreo, mientras que 3,8% (1/26) todavía tenía enfermedad grave en el momento del muestreo.
Características de la psoriasis, síntomas y áreas afectadasEn el momento del muestreo, las puntuaciones medias ± DE del BSA y del PASI en general fueron 3,7 ± 5,3% y 4,6 ± 9,5, respectivamente. En general, 38,9% (147/378) de los pacientes tenía una puntuación PGA ≥ 2, lo que indica ausencia de aclaramiento cutáneo o casi aclaramiento, 17,1% (18/105) experimentaba en la actualidad un brote, 27,8% (105/378) había notificado un brote en los 12 meses previos, y 63% (238/378) estaba en remisión (tabla 1). De los pacientes con enfermedad de moderada a grave, 31,6% (18/57) tenía un BSA > 10%, 34,7% (17/49) tenía un PASI > 10 y 30,8% (8/26) experimentaba un brote. El Apéndice B, tabla SI (ver material suplementario) muestra otros síntomas y áreas afectadas por PsO en el muestreo.
Se llevó a cabo un análisis en el subconjunto de pacientes que actualmente no experimentaban un brote (Apéndice B, tabla SII; ver material suplementario). En el muestreo, los pacientes con enfermedad leve reportaron un BSA media de 2,6 ± 4,1%, un PASI medio de 3,4 ± 8,8; 28,2% (87/308) de los pacientes con enfermedad leve tenían una puntuación PGA de dos a cuatro. De los pacientes con enfermedad de moderada a grave que actualmente no experimentan un brote, los pacientes tenían un BSA media de 7,9 ± 6,2%, una puntuación PASI media de 9,1 ± 7,8 y 88,5% (46/52) tenían una puntuación PGA2–4.
Gravedad según el tipo de médico que indicó el tratamientoUna mayor proporción de pacientes acudió al dermatólogo (leve, 84% [200/238]; moderado a grave, 16% [38/238]), que al pediatra (leve, 79,4% [27/34]; moderado a grave, 20,6% [7/34]) o al MG (leve, 92,0% [81/88], moderado a grave, 8,0% [7/88]) (Análisis 1, Apéndice B, tabla SIII; ver material suplementario). Los dermatólogos informaron un puntaje PASI promedio más bajo en pacientes con enfermedad de moderada a grave en comparación con los médicos de cabecera y los pediatras; sin embargo, los médicos de cabecera informaron el porcentaje de BSA promedio más bajo con enfermedad de moderada a grave.
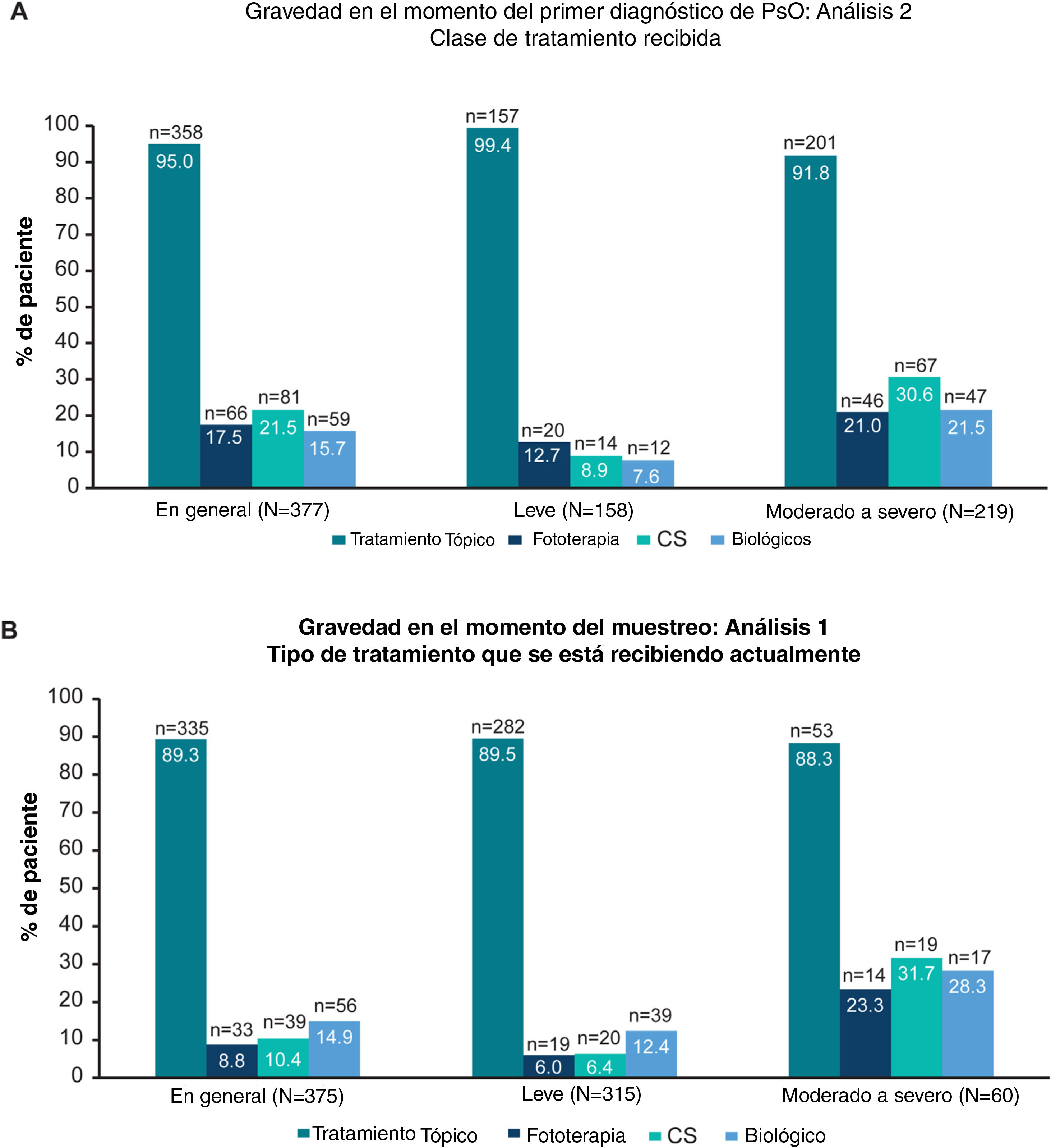
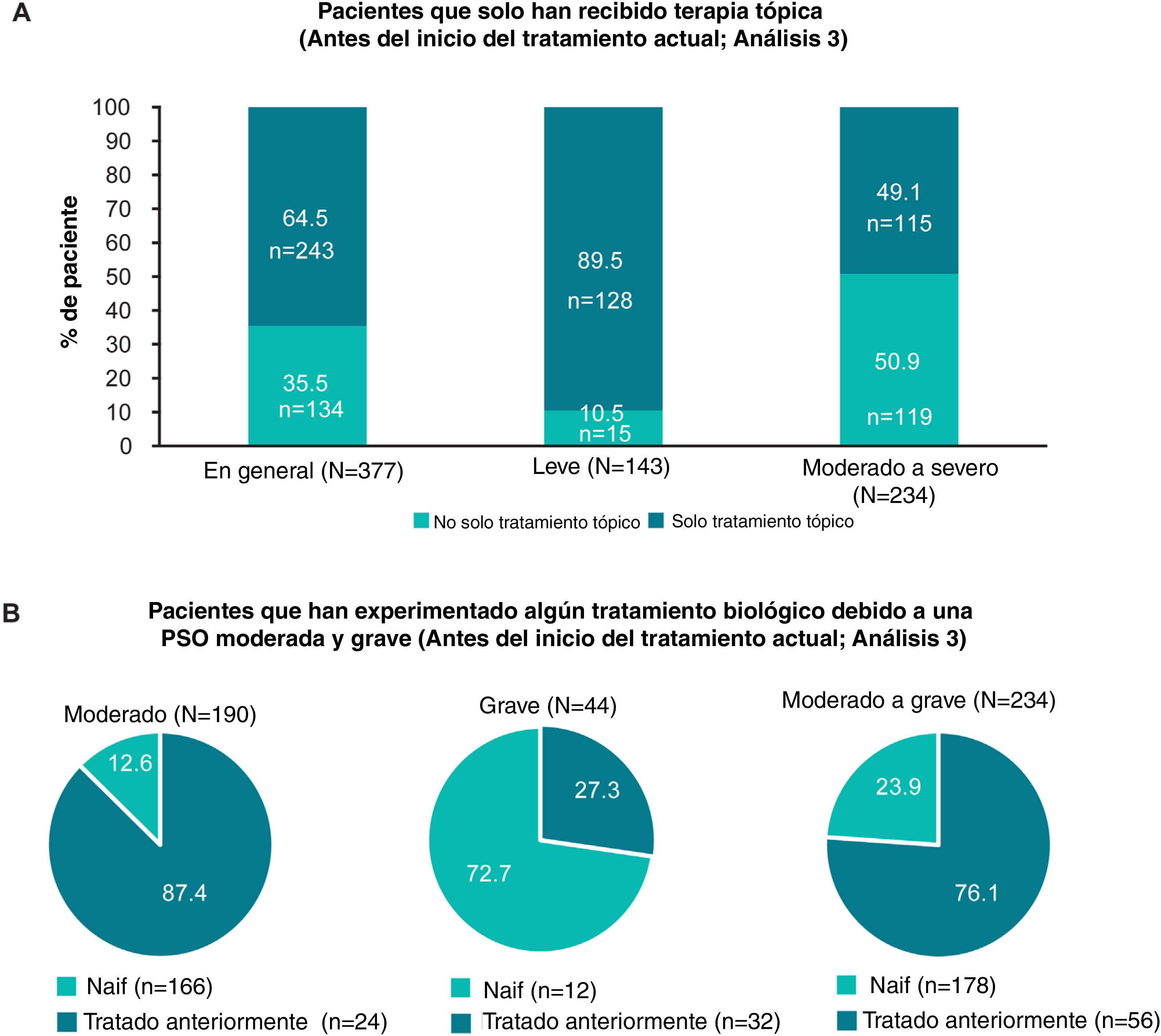
Patrones de tratamientoHistorial de tratamientoEn general, 95% (358/377) de los pacientes había recibido alguna vez terapia tópica, y solo 17,5% (66/377), 21,5% (81/377) y 15,7% (59/377) de los pacientes habían recibido alguna vez fototerapia, terapia sistémica convencional y tratamiento biológico, respectivamente (fig. 2A; Análisis 2, en el momento del diagnóstico). De los pacientes categorizados con enfermedad leve y moderada a grave en el momento del diagnóstico, 8,9% (14/158) y 30,6% (67/219) habían recibido alguna vez tratamiento sistémico convencional, y 7,6% (12/158) y 21,5% (47/219) habían recibido alguna vez terapia biológica para su PsO, respectivamente (Análisis 2, fig. 2A). Categorizados según la gravedad juzgada por el médico antes del inicio del tratamiento actual, 49,1% (115/234) de los pacientes con enfermedad de moderada a grave habían sido tratados alguna vez solo con una terapia tópica para su PsO (Análisis 3, fig. 3A). Cabe destacar que 93,3% (56/60) de los pacientes con enfermedad de moderada a grave tenía experiencia con la terapia biológica (fig. 3B).
Pacientes que recibieron solo terapia tópica y que tenían experiencia biológica, en general, y por gravedad antes del inicio del tratamiento actual (Análisis 3). A) Gráficos de barras que muestran la proporción de pacientes que solo habían recibido terapia tópica alguna vez, en general, y en pacientes con enfermedad leve y moderada a grave a juicio del médico antes del inicio del tratamiento actual (Análisis 3). B) Gráficos circulares que ilustran la frecuencia de pacientes sin tratamiento biológico previo y aquellos que ya lo han recibido, con enfermedad moderada, grave y de moderada a grave, determinada por el médico en el momento del inicio del tratamiento actual (Análisis 3).
n: número de pacientes con resultado; N: número total de pacientes en el grupo; Pso: psoriasis.
En general, 89,3% (335/375) de los pacientes recibían terapia tópica de PsO en el momento del muestreo en comparación con 8,8% (33/375), 10,4% (39/375) y 14,9% (56/375) de los pacientes que actualmente recibían fototerapia, tratamientos sistémicos convencionales y terapia biológica, respectivamente (fig. 2B). Para los pacientes con enfermedad de moderada a grave en el momento del muestreo, 31,7% (19/60) recibió terapia sistémica convencional y 28,3% (17/60) terapia biológica (fig. 2B). Una descripción detallada del tratamiento actual se presenta en la tabla 2.
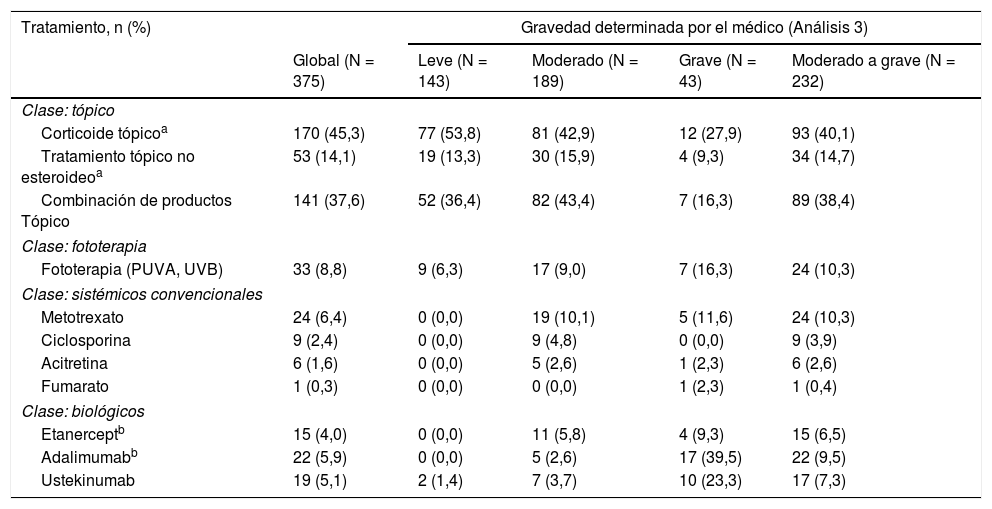
Tipo de tratamiento actual, en general y según la severidad en el momento del inicio de tratamiento actual (Análisis 3)
| Tratamiento, n (%) | Gravedad determinada por el médico (Análisis 3) | ||||
|---|---|---|---|---|---|
| Global (N = 375) | Leve (N = 143) | Moderado (N = 189) | Grave (N = 43) | Moderado a grave (N = 232) | |
| Clase: tópico | |||||
| Corticoide tópicoa | 170 (45,3) | 77 (53,8) | 81 (42,9) | 12 (27,9) | 93 (40,1) |
| Tratamiento tópico no esteroideoa | 53 (14,1) | 19 (13,3) | 30 (15,9) | 4 (9,3) | 34 (14,7) |
| Combinación de productos Tópico | 141 (37,6) | 52 (36,4) | 82 (43,4) | 7 (16,3) | 89 (38,4) |
| Clase: fototerapia | |||||
| Fototerapia (PUVA, UVB) | 33 (8,8) | 9 (6,3) | 17 (9,0) | 7 (16,3) | 24 (10,3) |
| Clase: sistémicos convencionales | |||||
| Metotrexato | 24 (6,4) | 0 (0,0) | 19 (10,1) | 5 (11,6) | 24 (10,3) |
| Ciclosporina | 9 (2,4) | 0 (0,0) | 9 (4,8) | 0 (0,0) | 9 (3,9) |
| Acitretina | 6 (1,6) | 0 (0,0) | 5 (2,6) | 1 (2,3) | 6 (2,6) |
| Fumarato | 1 (0,3) | 0 (0,0) | 0 (0,0) | 1 (2,3) | 1 (0,4) |
| Clase: biológicos | |||||
| Etanerceptb | 15 (4,0) | 0 (0,0) | 11 (5,8) | 4 (9,3) | 15 (6,5) |
| Adalimumabb | 22 (5,9) | 0 (0,0) | 5 (2,6) | 17 (39,5) | 22 (9,5) |
| Ustekinumab | 19 (5,1) | 2 (1,4) | 7 (3,7) | 10 (23,3) | 17 (7,3) |
De los pacientes con enfermedad de moderada a grave que no habían recibido un tratamiento biológico durante el muestreo, se preguntó a los médicos si estos pacientes se beneficiarían de uno; los médicos justificaron su uso en el 34,9% (15/43) de los pacientes. Las razones más frecuentes para no haber recibido un tratamiento biológico fueron: «paciente está en remisión» (23,8%, 10/42), «restricciones de formulario/seguro» (23,8%, 10/42), «inquietudes sobre la seguridad/efectos secundarios» (21,4%, 9/42) y que el «padre/tutor/cuidador no quisiera administrarlo» (21,4%, 9/42).
Tratamientos según el tipo de médicoEn el momento de iniciar el tratamiento, los pacientes que consultaron con pediatra o dermatólogo estaban recibiendo «en la actualidad» terapias convencionales (pediatra, 20,6%, 7/34; dermatólogo, 11,9%, 28/235) y terapia biológica (pediatra, 26,5%, 9/34; dermatólogo, 18,7%, 44/235), en comparación con los que consultaron con un médico de cabecera/PCP (tratamientos sistémicos convencionales, 0%, 0/88; biológicos, 1,1%, 1/88).
DiscusiónSeyger et al. describieron que a pesar de recibir tratamiento para la PsO, los pacientes pediátricos seguían exhibiendo una carga de enfermedad persistente y que una pequeña proporción de los pacientes con PsO moderada o grave no reciben un tratamiento eficiente16. El presente estudio es la continuación del de Seyger et al., cuyo objetivo principal fue identificar la carga de enfermedad informada por el médico y los patrones de tratamiento actuales en una cohorte de pacientes pediátricos con PsO del mundo real en España. Se excluyeron del análisis los pacientes con una duración del tratamiento < 4 semanas para la terapia tópica y/o < 12 semanas para la terapia convencional sistémica y/o biológica.
En el diagnóstico, el 58,2% de los pacientes y, el 15,9% en el muestreo, presentaban una psoriasis moderada - grave y habían recibido previamente o estaban recibiendo tratamiento para su psoriasis. Los pacientes que actualmente no estaban experimentando un brote mostraron puntuaciones de BSA y PASI elevadas, lo que sugiere que mientras que muchos pacientes pediátricos están bien controlados actualmente, una proporción de pacientes con psoriasis moderada - grave todavía tiene una elevada carga de la enfermedad, estén o no experimentando un brote, lo que sugiere la posibilidad de que estos pacientes no estén controlados de su psoriasis o incluso infra-tratados. Cabe señalar, que los pacientes adultos con psoriasis con PASI o BSA mayor a 10 se consideran candidatos a tratamientos sistémicos. Se deberían considerar los mismos objetivos terapéuticos para todos los pacientes con psoriasis pediátrica18,19.
Este estudio demostró que 93,3% de los pacientes con enfermedad de moderada a grave en el momento del muestreo tenían experiencia con la terapia biológica. Cualquier retraso en el inicio de los tratamientos biológicos podría explicarse por dos factores. En primer lugar, podría haber una ausencia de médicos con experiencia en pautar terapias biológicas a pacientes pediátricos. Una encuesta en pacientes adultos, que incluyó las respuestas de 300 dermatólogos en España, informó que 85% de los dermatólogos prescriben dos o más terapias tradicionales antes de prescribir un tratamiento biológico, lo que indica que los biológicos se reservan para su uso después de que otros tratamientos hayan fallado. El estudio informó que 73% de los pacientes con PsO en España tienen un retraso promedio de dos años antes de cambiar a un tratamiento biológico20. En segundo lugar, la aprobación del uso de terapias biológicas en España podría estar restringida por el sistema nacional de salud, variando el nivel de acceso a ellas dependiendo de las diferencias observadas en el territorio nacional.
Al igual que en los pacientes adultos, los niños y los adolescentes con un BSA superior a 10%, DLQI > 10, aquellos que no han respondido a las terapias estándar o tienen contraindicaciones, deben ser considerados para recibir una terapia biológica21. Algunos estudios aconsejan la utilización de terapias sistémicas más temprano en psoriasis leve y en pacientes con puntajes DLQI más bajos21. El permitir que los pacientes accedan a un tratamiento sistémico les mejorará la CdV y reducirá la progresión de la enfermedad.
De aquellos pacientes con enfermedad de moderada a grave que no recibieron una terapia biológica en el momento del muestreo, se preguntó a sus médicos si la condición actual de cada paciente justificaba el uso de uno; 34,9% de los médicos respondió que «sí». Las razones más frecuentes referidas por los médicos para justificar el no recetar un tratamiento biológico fueron que «paciente estaba en remisión» y debido a las «restricciones de formulario/seguro», lo que puede indicar que el coste de las terapias biológicas implica un gasto económico importante.
Los pacientes con enfermedad moderada y grave tenían más probabilidades de haber visitado a un dermatólogo que a un médico de cabecera o a un pediatra. Los médicos de cabecera y los pediatras con frecuencia derivaban a los pacientes con enfermedad moderada y grave a un especialista, ya que la fototerapia y los tratamientos sistémicos o biológicos para la PsO requieren instalaciones de unidades especializadas, o debido a que estos medicamentos están restringidos a la prescripción hospitalaria por parte de dermatólogos. De manera similar a los hallazgos de Seyger et al., es menos probable que los médicos de cabecera en España prescriban un tratamiento sistémico que los dermatólogos16. Las guías regionales para la derivación a especialistas en España hacen posible que los pacientes reciban el tratamiento adecuado antes. La intervención oportuna es fundamental, sobre todo en los casos graves, para modificar el curso inflamatorio de la enfermedad y prevenir complicaciones y secuelas en etapas posteriores de la vida15.
LimitacionesEn este estudio de pacientes con PsO pediátrica, es probable que los dermatólogos estuvieran sobrerrepresentados, ya que solo existe un pequeño porcentaje de pacientes tratados por pediatras y médicos generales. Por tanto, la proporción de pacientes pediátricos en España que acuden a cada tipo de médico puede no quedar reflejada con precisión en estos datos. Otras limitaciones del estudio fueron descritas previamente por Seyger et al.16
ConclusionesEstos datos de vida real reflejan la carga actual de la enfermedad y el panorama del tratamiento de la PsO pediátrica en España. El manejo de pacientes con PsO pediátrica podría mejorar si se incrementa la educación de los profesionales de la salud, así como si se les proporcionan pautas de tratamiento regionales para la PsO pediátrica. Esto puede reducir el retraso en la derivación de los pacientes con PsO a hospitales con una mayor experiencia en el manejo de la PsO con terapias biológicas y, por lo tanto, potencialmente superar las dificultades de acceso a las terapias biológicas en toda España.
FinanciaciónEste estudio fue financiado por Novartis Farmacéutica S.A, Barcelona, España. La encuesta fue realizada por Adelphi Real World de manera independientemente de Novartis.
Conflicto de interesesRaúl de Lucas no tiene ningún conflicto que declarar.
Asunción Vicente ha participado en ensayos clínicos como investigadora principal, subinvestigadora, brindó asesoría científica o presentaciones en congresos médicos remuneradas y/o asesoría de: Abbvie, Amgen, Amryt, Boehringer Ingelheim, Bristol-Myers Squibb, Ferrer, Galderma, Janssen, Leti, Eli Lilly and Company, Novartis, Pierre Fabre, Pfizer, Sanofi.
Antonio Torrelo dio conferencias para Novartis.
James Lucas y Liane Gillespie-Akar son empleados de Adelphi Real World.
Craig Richardson y Lara Gómez Labrador son empleados de Novartis.
Los autores agradecen a Ellen McKenna MSc y Philip O’Gorman PhD (Novartis Ireland Ltd, Dublín, Irlanda) por brindar apoyo y asistencia en la redacción médica, la cual que fue financiada por Novartis Pharmaceuticals Corporation de acuerdo con las pautas de Buenas Prácticas de Publicación (GPP 2022) (https://www.ismpp.org/gpp-2022).



![Cambio en la gravedad de la enfermedad del paciente y recopilación de datos. A) Esquema que ilustra la recopilación de los datos acerca de la gravedad recogido de manera retrospectiva (en el momento del diagnóstico, en el momento del inicio del tratamiento utilizado en la «actualidad» y en el momento del muestreo [actualmente]). B) Esquema que muestra la frecuencia de pacientes con PsO leve, moderada y grave, según la categorización en el momento del primer diagnóstico de PsO (retrospectivo) frente al momento del muestreo (actualmente). n: número de pacientes con resultado; N: número total de pacientes en el grupo; Pso: psoriasis. Cambio en la gravedad de la enfermedad del paciente y recopilación de datos. A) Esquema que ilustra la recopilación de los datos acerca de la gravedad recogido de manera retrospectiva (en el momento del diagnóstico, en el momento del inicio del tratamiento utilizado en la «actualidad» y en el momento del muestreo [actualmente]). B) Esquema que muestra la frecuencia de pacientes con PsO leve, moderada y grave, según la categorización en el momento del primer diagnóstico de PsO (retrospectivo) frente al momento del muestreo (actualmente). n: número de pacientes con resultado; N: número total de pacientes en el grupo; Pso: psoriasis.](https://static.elsevier.es/multimedia/00017310/0000011400000005/v2_202306061222/S0001731023003253/v2_202306061222/es/main.assets/thumbnail/gr1.jpeg?xkr=ue/ImdikoIMrsJoerZ+w9/t1/zx4Q/XH5Tma1a/6fSs=)