Sr. Director:
Presentamos el caso de un varón de 12 años con linfoma linfoblástico T que precisó trasplante alogénico de médula ósea de donante emparentado.
Sufrió una enfermedad de injerto contra huésped (EICH) aguda que fue controlada con ciclosporina y corticoides sistémicos.
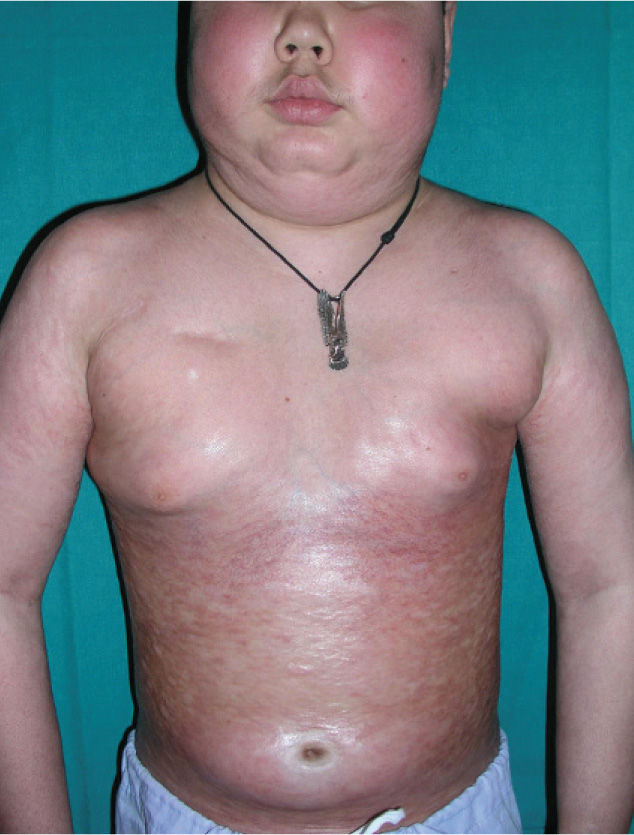
Alrededor del día 100 postrasplante comenzó a presentar placas induradas en tronco que fueron generalizándose hasta causar esclerosis difusa de la piel, con marcada retracción articular e impotencia funcional (fig. 1). Además presentó disnea que progresó hasta hacerse de mínimos esfuerzos.
Fue diagnosticado de EICH crónica esclerodermiforme con afectación cutánea y pulmonar, instaurándose tratamiento con ciclosporina (50mg/ 12 horas, vía oral) y metilprednisolona (20mg/24 horas, vía oral).
Ante la falta de respuesta al mismo, fue remitido a nuestro centro para tratamiento con fotoféresis. Se realizaron 2 sesiones en días consecutivos cada 3–4 semanas, hasta un total de 34 sesiones, durando el tratamiento aproximadamente un año.
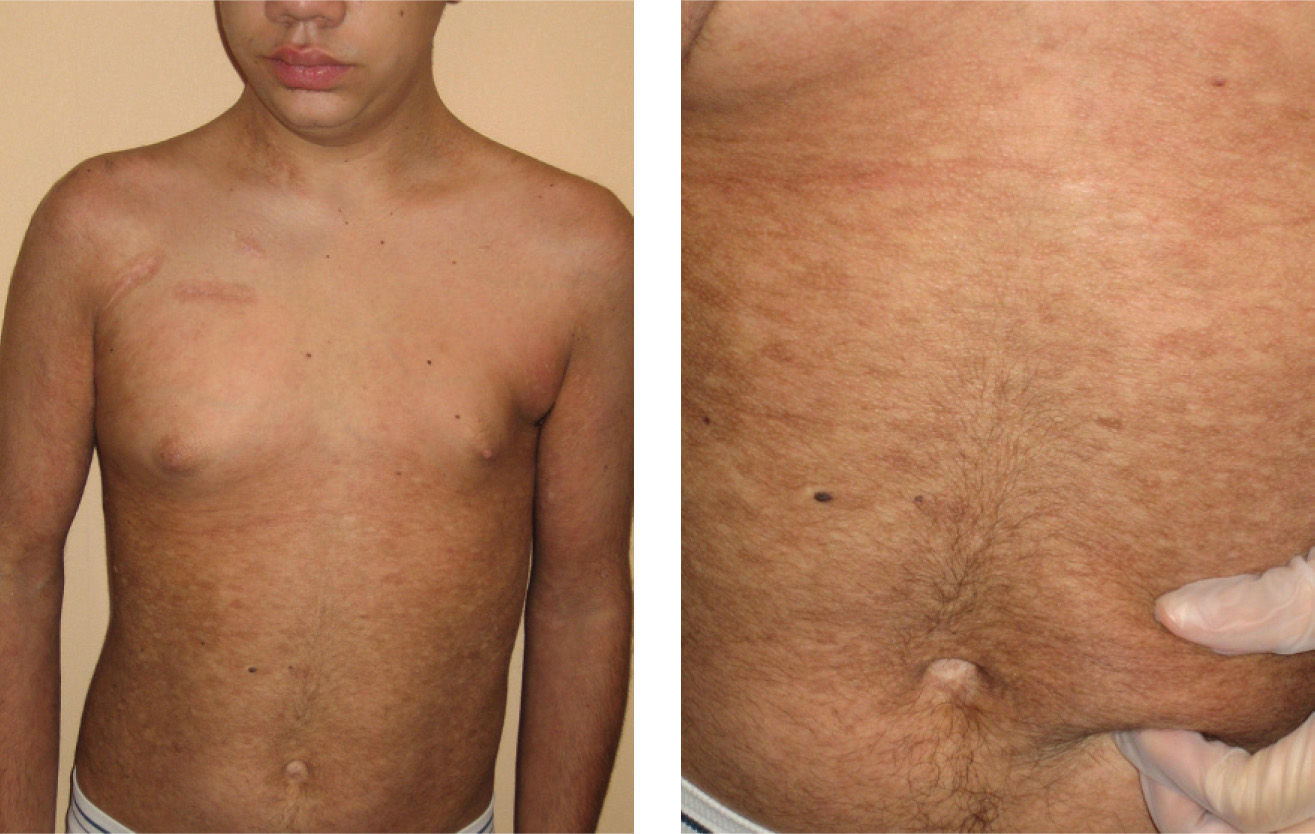
A lo largo del tratamiento se observó una mejoría de los síntomas, con clara disminución de la induración cutánea y marcada mejoría de la movilidad articular (fig. 2). Pudieron reducirse las dosis de metilprednisolona (8mg/ 24 horas a días alternos) y ciclosporina (50mg/24 horas) al alta de la fotoféresis. Un año después el paciente no precisa tratamiento inmunosupresor.
Se cree que la EICH crónica puede ser una continuación de la EICH aguda y/o el resultado de una reconstitución del sistema inmune disfuncional que genera autoanticuerpos y clones de linfocitos T autorreactivos1. Las teorías actuales implican un desequilibrio Th1:Th2, con aumento de la actividad Th22,3 y un importante papel de las células dendríticas en la inducción de la EICH crónica.
El tratamiento de elección para la EICH crónica son los corticoides sistémicos, aunque sólo una minoría de los pacientes mantienen la respuesta a este tratamiento de forma indefinida4. Se han utilizado otros inmunosupresores con resultados variables: ciclosporina, talidomida, tacrolimus, metotrexato, azatioprina, etretinato, clofazimina e irradiación linfoide total. Estos tratamientos tienen un riesgo importante de efectos adversos.
En 2001 Salvaneschi et al4 publicaron una serie de 14 niños con EICH crónica refractaria a terapia inmunosupresora tratados con fotoféresis. Nueve de ellos presentaron respuestas parciales o completas, pudiendo suspender el tratamiento inmunosupresor a 7 de ellos.
Dall'Amico y Messina5 realizaron una revisión de 20 series publicadas previamente, con un total de 204 casos de EICH crónica resistente tratados con fotoféresis. Observaron regresión de las lesiones cutáneas en el 76 % de los casos, con respuesta completa en el 35 % de ellos. Observaron también que las lesiones cutáneas responden lentamente, requiriendo más de 1 año para desaparecer. Aparentemente, según estos autores, la afectación hepática y bronquial tiene peor respuesta a este tratamiento.
Recientemente Couriel et al6 evaluaron retrospectivamente a 43 pacientes tratados con fotoféresis, un 61 % de los cuales respondieron y un 32 % tuvieron respuesta completa. Al año de iniciar el tratamiento el 22 % de los pacientes pudieron suspenderlo con corticoides.
La fotoféresis consiste en la exposición extracorpórea a radiación ultravioleta A de células mononucleares fotoactivadas mediante 8-metoxipsoraleno. Estas células se reinfunden posteriormente al paciente. El mecanismo por el que actúa la fotoféresis no está claramente definido. Fimiani et al1 describieron dos efectos aparentemente opuestos: activación del sistema inmune en contra de células neoplásicas (útil para linfomas T cutáneos7) y disminución de la actividad de los clones T en enfermedades autoinmunes y respuestas inmunes autoalogénicas (EICH).
Las células presentadoras de antígeno y los linfocitos T se inactivan con la fotoféresis, pero la muerte celular ocasionada por este mecanismo no parece ser suficiente para justificar la eficacia del tratamiento, dado que sólo se dañan unos 5-106 leucocitos circulantes. La fagocitosis de estas células apoptóticas parece activar las células dendríticas y aumentar las citoquinas inmunosupresoras. Además la fotoféresis a largo plazo consigue restaurar el equilibrio Th1:Th2.
No está claramente establecida la frecuencia del tratamiento con fotoféresis, actualmente los ciclos oscilan entre 1 y 4 semanas, según los centros. Parece que lo más oportuno, hasta que se realicen estudios aleatorizados, es individualizar en función de la intensidad de la clínica y la respuesta del paciente. Se ha observado que cuanto antes se comience el tratamiento mejor será el pronóstico4. Se ha visto que la fotoféresis es eficaz tanto en adultos como en niños5,8.
Presentamos el caso de un niño con EICH crónica con excelente respuesta a fotoféresis, que permitió la suspensión del tratamiento inmunosupresor. La fotoféresis es hoy día una alternativa efectiva para el tratamiento de la EICH crónica. Numerosas series de pacientes tratados con este sistema han demostrado que la fotoféresis puede ayudar a reducir las dosis de inmunosupresores e incluso suspenderlos, disminuyendo así el riesgo de complicaciones en estos pacientes.