La espironolactona es un diurético ahorrador de potasio con efecto antiandrogénico, de bajo coste y con un buen perfil de seguridad. Hemos observado en nuestra experiencia que es un fármaco infrautilizado en dermatología, pese a que existe evidencia de su uso en diversas patologías dermatológicas, especialmente en el acné femenino (nivel de evidencia ii-iii, fuerza de recomendación B), donde podría disminuir el uso de antibióticos y probablemente de isotretinoína. Otras enfermedades en las cuales puede ser útil son la hidrosadenitis supurativa y la alopecia androgenética femenina. Discutimos las indicaciones de la espironolactona, su dosificación en la práctica dermatológica, las precauciones que deben tener en cuenta y sus efectos secundarios. Además, presentamos nueva evidencia que avala su uso en dermatología sin necesidad de indicar pruebas complementarias en mujeres jóvenes y enfatiza su seguridad a largo plazo. Consideramos que la espironolactona debería estar entre los agentes comúnmente utilizados en la práctica clínica habitual.
Spironolactone is an economical potassium-sparing diuretic with an anti-androgenic effect and a good safety profile. Our experience suggests that this diuretic is underexploited in dermatology even though there is evidence supporting its use in several skin conditions. When prescribed for acne in female patients (level 1–2 evidence; strength of recommendation, B), for example, it can reduce the need for antibiotics and possibly isotretinoin. Other diseases in which spironolactone is potentially useful are hidradenitis suppurativa and female androgenetic alopecia. We discuss the indications for spironolactone, dosing in dermatology, precautions to consider, and adverse effects. We also review new evidence that stresses the safety of long-term therapy and supports the use of this drug without the need for complementary testing in young women. We think that spironolactone merits a place among the medications commonly used in routine clinical practice.
La espironolactona es un antagonista sintético del receptor de la aldosterona, con propiedades mineralocorticoides y antiandrogénicas1. Ha sido ampliamente utilizada como diurético y antiandrógeno en diversas especialidades médicas.
Los andrógenos contribuyen al desarrollo de varias enfermedades cutáneas, como el acné, la alopecia androgenética de patrón femenino (FAGA), el hirsutismo y la hidradenitis supurativa (HS), entre otras. Estas enfermedades pueden estar asociadas a un hiperandrogenismo, aunque la mayoría de los casos cursan sin anomalías androgénicas sistémicas2. La terapia antiandrogénica es una opción razonable en este contexto y la espironolactona es una alternativa de bajo coste y un buen perfil de seguridad.
El objetivo de esta revisión es analizar la evidencia científica sobre el uso de la espironolactona en enfermedad dermatológica, en especial en el acné, la HS, la FAGA y el hirsutismo. Discutimos sus indicaciones, la dosificación en la práctica dermatológica, las precauciones que se deben tener en cuenta y sus efectos adversos.
Papel de los andrógenos en la pielLos andrógenos tienen unos efectos fisiológicos importantes en la piel. Regulan distintos procesos relacionados con el recambio cutáneo, el crecimiento de los folículos pilosos, la proliferación de las glándulas sebáceas (especialmente las faciales), la producción de sebo y la embriogénesis, entre otros2,3. En la piel se pueden producir andrógenos de novo a partir del colesterol o de precursores suprarrenales o gonadales circulantes, como el sulfato de dehidroepiandosterona. La mayor densidad de receptores androgénicos se encuentra en las células basales y los sebocitos, así como en las papilas dérmicas, la vaina radicular externa del folículo piloso, las glándulas sudoríparas, el endotelio vascular, las células musculares lisas y los queratinocitos4,5. El receptor de andrógenos es un factor de transcripción dependiente de ligando, miembro de la superfamilia de receptores nucleares esteroidales. Consta de 3dominios funcionales básicos: el dominio de regulación de la transcripción N-terminal, el dominio de unión al ADN y el dominio de unión al ligando3. Cuando el receptor de andrógenos interactúa con su ligando de andrógenos, se disocia desde proteínas de choque térmico y este complejo receptor-ligando se transloca en el núcleo, uniéndose a los elementos de respuesta androgénica en la región promotora de genes regulados por los andrógenos, induciendo su transcripción de manera dependiente de la unión al ADN. Estos receptores también actúan de forma independiente de la unión al ADN, vía la activación rápida de cascadas de segundos mensajeros y otros mecanismos recientemente descritos3,6.
Mecanismo de acción y farmacocinética de la espironolactonaLa espironolactona se usa clásicamente como un agente diurético y antihipertensivo, dado por su antagonismo competitivo con el receptor de la aldosterona. Sus propiedades antiandrogénicas radican en la competencia con la testosterona y dihidrotestosterona por la unión a los receptores de andrógenos1,7. Al igual que otros antiandrógenos como el acetato de ciproterona, no es únicamente antagonista, sino que puede ser un agonista parcial débil. Sin embargo, en presencia de altas concentraciones de testosterona y de dihidrotestosterona, se comporta como un antagonista puro8. Por otro lado, degrada un cofactor del citocromo p450, necesario para la síntesis de testosterona a nivel gonadal y suprarrenal, además de aumentar los niveles de la globulina transportadora de hormonas sexuales, lo que disminuye los niveles de testosterona libre. El efecto de la espironolactona en la reducción de la actividad de la 5-alfa-reductasa es controvertido1,7. Un estudio mostró una disminución de la actividad enzimática en 11 de 13 pacientes con hirsutismo en tratamiento con este fármaco, sin conocerse con certeza si actúa a sobre la isoenzima 1 o 29 (tabla 1).
Mecanismo de acción e indicaciones no dermatológicas de la espironolactona
| Mecanismo de acción | Antagonismo de los receptores de andrógenos. Compite con la testosterona y la dihidrotestosteronaDegrada un cofactor del citocromo p450, inhibiendo la síntesis de testosteronaAumento de los niveles de la globulina transportadora de hormonas sexuales, disminuyendo la testosterona libreReducción la actividad de la 5-alfa-reductasa |
| Farmacocinética | Biodisponibilidad por vía oral del 90%Unión a proteínas en un 98%Su metabolito primario es la canrenonaLos alimentos aumentan su absorciónMetabolismo hepático, con vida media de 12,5 hExcreción por la orina y bilis |
| Indicaciones aprobadas por la FDA | Insuficiencia cardíacaHipertensión arterialEdema asociado a cirrosis hepática o síndrome nefróticoHiperaldosteronismo primario |
Su biodisponibilidad por vía oral es de aproximadamente un 90% y se encuentra unida a proteínas en un 98%. Su metabolito primario, la canrenona, se une a estas en un 90%. Este metabolito contribuye a las propiedades antiandrogénicas de la espironolactona7,10. Los alimentos aumentan la absorción de la espironolactona y su metabolismo es fundamentalmente hepático, con una vida media de 12,5 h. Sus metabolitos se excretan por la orina y bilis7.
Indicaciones aprobadasLa espironolactona se ha usado clásicamente como un diurético ahorrador de potasio, teniendo indicaciones aprobadas por la Food and Drug Administration (FDA) en insuficiencia cardíaca, hipertensión arterial, edema asociado a cirrosis hepática o síndrome nefrótico e hiperaldosteronismo primario7,10 (tabla 1). En dermatología, no existen indicaciones aprobadas, sin embargo, se ha utilizado fuera de indicación en acné, hirsutismo, HS y FAGA7,11.
Efectos adversos y toxicidadesEn términos generales, la espironolactona es bien tolerada. Sus principales efectos adversos son dependientes de la dosis y están relacionados con su efecto antiandrogénico. La irregularidad menstrual se presenta en el 15-30% de las pacientes y puede ser controlada con el uso concomitante de anticonceptivos orales combinados de tercera o cuarta generación, o con un dispositivo intrauterino hormonal. Otros efectos adversos descritos en menos del 5% de los casos son: sensibilidad mamaria, disminución de la libido, mareos, náuseas, cefalea, poliuria y fatiga1,11,12 (tabla 2).
Espironolactona en la práctica clínica: dosis, duración, monitorización y precauciones
| Dosis de inicio | 25 a 50 mg/día |
| Dosis de mantención | Acné: 50-100 mg/díaaHidrosadenitis supurativa: 100-200 mg/díaFAGA: 100-200 mg/díaHirsutismo: 100 mg/día |
| Duración del tratamiento | 3 a 24 meses |
| Monitorización | No se requiere analíticas de control en mujeres sanas menores de 45 años |
| Efectos adversos y precauciones | Frecuentes (15-30%): irregularidad menstrualInfrecuentes (< 5%): sensibilidad mamaria, disminución de la libido, mareos, náuseas, cefalea, poliuria y fatigaHiperpotasemia en pacientes con enfermedad renal crónica, insuficiencia cardíaca o consumo asociado a otros fármacosCategoría C del embarazo |
FAGA: alopecia androgenética de patrón femenino.
En acné, preferimos iniciar a dosis de 25mg/día durante una semana para luego aumentar a 50mg/día (y mantener esta dosis en la mayoría de las pacientes). No hemos necesitado utilizar dosis superiores a 100mg/día. Es frecuente combinarla con anticonceptivos mixtos de acción antiandrogénica de tercera o cuarta generación. Los comprimidos de espironolactona son fraccionables y se encuentran en presentaciones de 25 y 100mg.
Fuente: Salavastru et al.7 y Wolverton10.
La espironolactona, al ser un ahorrador de potasio, puede producir hiperpotasemia e hiponatremia, en especial en individuos con una insuficiencia renal o una insuficiencia cardíaca grave, si se utilizan dosis altas del fármaco12. En un estudio multicéntrico13 se analizaron los niveles de potasio en 974 mujeres entre 18 y 45 años con acné, en tratamiento con espironolactona 50 a 200mg/día. Solo 13 muestras (0,75%) mostraron hiperpotasemia y al repetir las pruebas en 6 de ellas se encontraron valores normales; estos resultados fueron similares a los controles de la misma edad. Los autores concluyeron que el control de los niveles de potasio en mujeres jóvenes sanas es innecesario, conclusión que también se obtuvo tras una revisión sistemática reciente11. El uso concomitante junto a anticonceptivos combinados con drospirenona, un derivado de la espironolactona, tampoco ha demostrado elevaciones significativas del potasio sérico14. Para las mujeres mayores de 45 años, según un estudio retrospectivo reciente, se sugiere que sería recomendable la determinación de niveles de potasio sérico durante el tratamiento con espironolactona, al observarse hasta un 16% de hiperpotasemia en este subgrupo de pacientes15.
En el embarazo, la espironolactona está incluida en la categoría C de la FDA (estudios en animales han mostrado algún efecto adverso fetal, sin contar con estudios controlados en mujeres embarazadas). Existe evidencia, en ratas y a dosis altas, de que puede causar un retraso en la maduración sexual del feto femenino y una feminización del feto masculino. No existen estudios controlados en humanos. Este fenómeno ocurriría entre la semana 6 y 14 de gestación, durante la diferenciación del tracto urogenital. La interrupción del fármaco antes de esta etapa podría evitar este efecto adverso7. Una reciente revisión sistemática encontró 5 casos de varones expuestos intraútero a la espironolactona (dosis entre 25 a 400mg/día), sin signos de feminización genital al nacer16. Se ha demostrado su excreción en la leche materna, pero con unos riesgos mínimos para el lactante7,12.
En estudios con animales se ha sugerido que la espironolactona tendría un efecto carcinogénico o mutagénico a altas dosis (100 veces mayores a las usadas en seres humanos). Sin embargo, 2estudios retrospectivos realizados en 2.300.000 y 1.290.625 mujeres no demostraron ninguna asociación entre este fármaco y el desarrollo de un cáncer de mama, de útero, de cuello uterino o de ovario17,18.
Se encontraron hallazgos similares en un estudio de cohorte reciente realizado en 74.272 pacientes, con una mediana de seguimiento de 11,5 años, donde no se demostró su asociación a ningún tipo de cáncer19.
Espironolactona en el acnéEn la última década se ha reconocido al acné como una enfermedad inflamatoria no infecciosa y se recomienda disminuir el uso de antibióticos12,20. Pese a esto, los antibióticos son uno de los fármacos sistémicos más indicados para el tratamiento del acné y existe una evidencia del aumento sostenido de la resistencia antibiótica21,22.
La espironolactona tiene un papel importante en el tratamiento del acné, sus efectos antiandrogénicos, inhibiendo la producción de sebo y la proliferación de sebocitos, favorecen la disminución de las lesiones, aun cuando no exista elevación de los andrógenos séricos. Al parecer, el acné estaría más asociado a las concentraciones locales de andrógenos y a una sensibilidad aumentada de los sebocitos1,2.
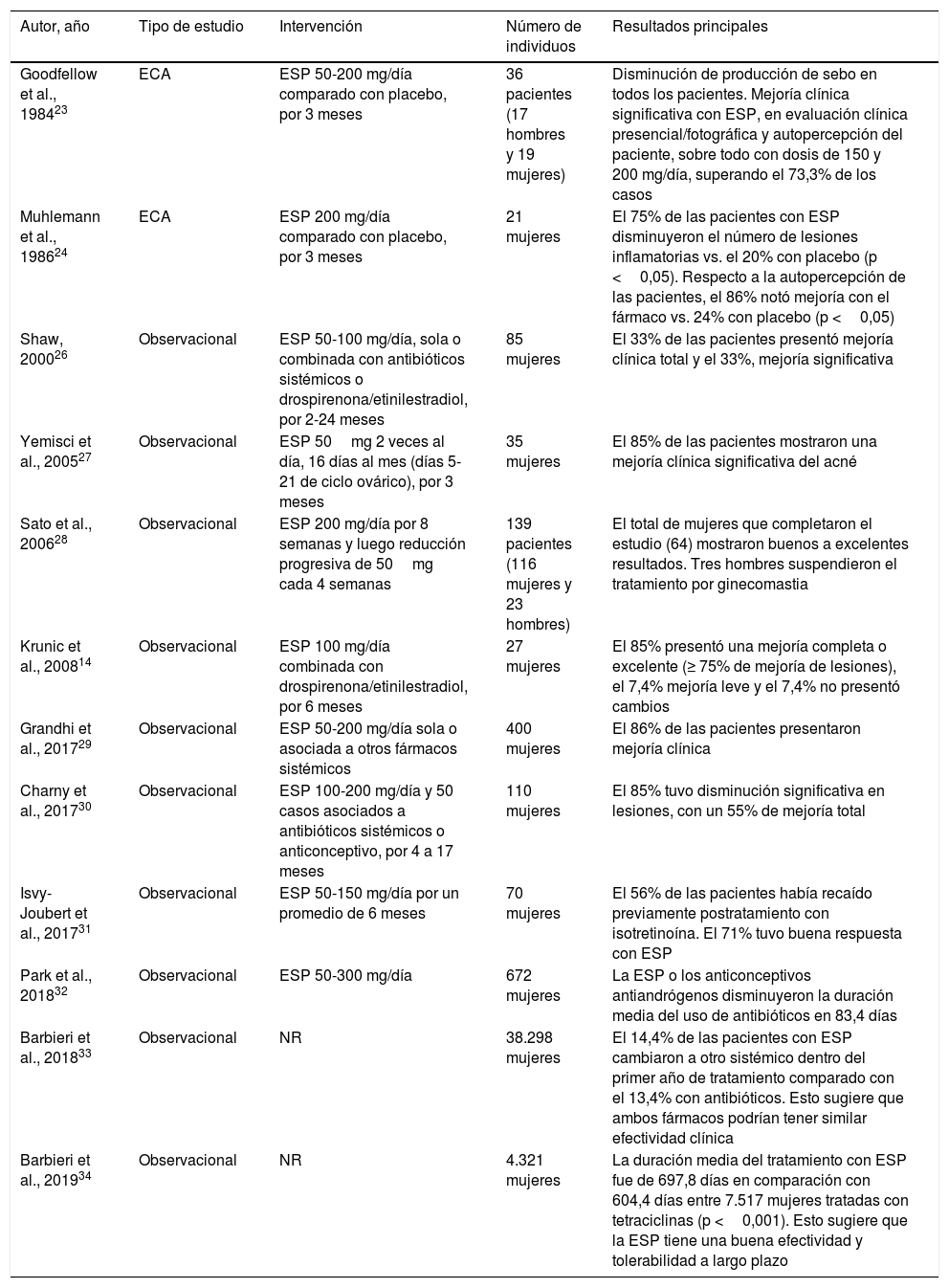
Existen 2ensayos clínicos controlados con placebo, que demostraron una disminución significativa en la producción de sebo y una mejoría clínica del acné23,24. Uno de ellos, de Muhlemann et al.24 incluyó a 29 pacientes de 18 a 38 años con un acné de moderado a severo. Recibieron espironolactona 200mg/día o placebo (sin otros tratamientos tópicos o sistémicos) durante 3 meses. Se analizó la respuesta clínica mediante la evaluación clínica (número de lesiones inflamatorias), fotografías y la percepción del paciente. En el 75% de los pacientes con espironolactona disminuyó el número de lesiones inflamatorias respecto al 20% en los pacientes tratados con placebo. Al evaluar las fotografías, el 58% presentó una mejoría clínica con espironolactona y el 21% con placebo. Todos los hallazgos fueron estadísticamente significativos. Respecto a los efectos directos en la tasa de excreción de sebo, se ha observado una reducción entre el 30 y el 50%, con unas dosis de espironolactona de 50 a 100mg, 2 veces al día25. Diversos estudios observacionales también avalan la utilidad del fármaco en el acné14,26-33 (tabla 3). Destaca el estudio de Barbieri et al.33 que incluyó a 38.298 mujeres con un acné en tratamiento con espironolactona o tetraciclinas, evaluando el cambio a otro agente sistémico dentro del primer año de tratamiento. El 14,4% de los pacientes con espironolactona cambiaron a otro sistémico, comparado con el 13,4% con tetraciclinas. Esto sugiere que ambos fármacos podrían tener una efectividad clínica similar. Dos estudios observacionales, muestran que el uso de espironolactona puede disminuir los días de uso de antibióticos sistémicos hasta en 83 días, además de tener una eficacia comparable a las tetraciclinas32,33. En otro estudio retrospectivo que incluyó a 4.321 mujeres se demostró que la duración del tratamiento con espironolactona es significativamente mayor (mayor «supervivencia») (media de 697,8 días) que con tetraciclinas (media de 604,4 días) (p<0,001), sugiriendo que en la práctica clínica puede tener una buena efectividad y tolerancia a largo plazo, y que podría ser una alternativa de primera línea terapéutica antes de utilizar antibióticos sistémicos34.
Estudios que avalan el uso de espironolactona en el tratamiento del acné
| Autor, año | Tipo de estudio | Intervención | Número de individuos | Resultados principales |
|---|---|---|---|---|
| Goodfellow et al., 198423 | ECA | ESP 50-200 mg/día comparado con placebo, por 3 meses | 36 pacientes (17 hombres y 19 mujeres) | Disminución de producción de sebo en todos los pacientes. Mejoría clínica significativa con ESP, en evaluación clínica presencial/fotográfica y autopercepción del paciente, sobre todo con dosis de 150 y 200 mg/día, superando el 73,3% de los casos |
| Muhlemann et al., 198624 | ECA | ESP 200 mg/día comparado con placebo, por 3 meses | 21 mujeres | El 75% de las pacientes con ESP disminuyeron el número de lesiones inflamatorias vs. el 20% con placebo (p <0,05). Respecto a la autopercepción de las pacientes, el 86% notó mejoría con el fármaco vs. 24% con placebo (p <0,05) |
| Shaw, 200026 | Observacional | ESP 50-100 mg/día, sola o combinada con antibióticos sistémicos o drospirenona/etinilestradiol, por 2-24 meses | 85 mujeres | El 33% de las pacientes presentó mejoría clínica total y el 33%, mejoría significativa |
| Yemisci et al., 200527 | Observacional | ESP 50mg 2 veces al día, 16 días al mes (días 5-21 de ciclo ovárico), por 3 meses | 35 mujeres | El 85% de las pacientes mostraron una mejoría clínica significativa del acné |
| Sato et al., 200628 | Observacional | ESP 200 mg/día por 8 semanas y luego reducción progresiva de 50mg cada 4 semanas | 139 pacientes (116 mujeres y 23 hombres) | El total de mujeres que completaron el estudio (64) mostraron buenos a excelentes resultados. Tres hombres suspendieron el tratamiento por ginecomastia |
| Krunic et al., 200814 | Observacional | ESP 100 mg/día combinada con drospirenona/etinilestradiol, por 6 meses | 27 mujeres | El 85% presentó una mejoría completa o excelente (≥ 75% de mejoría de lesiones), el 7,4% mejoría leve y el 7,4% no presentó cambios |
| Grandhi et al., 201729 | Observacional | ESP 50-200 mg/día sola o asociada a otros fármacos sistémicos | 400 mujeres | El 86% de las pacientes presentaron mejoría clínica |
| Charny et al., 201730 | Observacional | ESP 100-200 mg/día y 50 casos asociados a antibióticos sistémicos o anticonceptivo, por 4 a 17 meses | 110 mujeres | El 85% tuvo disminución significativa en lesiones, con un 55% de mejoría total |
| Isvy-Joubert et al., 201731 | Observacional | ESP 50-150 mg/día por un promedio de 6 meses | 70 mujeres | El 56% de las pacientes había recaído previamente postratamiento con isotretinoína. El 71% tuvo buena respuesta con ESP |
| Park et al., 201832 | Observacional | ESP 50-300 mg/día | 672 mujeres | La ESP o los anticonceptivos antiandrógenos disminuyeron la duración media del uso de antibióticos en 83,4 días |
| Barbieri et al., 201833 | Observacional | NR | 38.298 mujeres | El 14,4% de las pacientes con ESP cambiaron a otro sistémico dentro del primer año de tratamiento comparado con el 13,4% con antibióticos. Esto sugiere que ambos fármacos podrían tener similar efectividad clínica |
| Barbieri et al., 201934 | Observacional | NR | 4.321 mujeres | La duración media del tratamiento con ESP fue de 697,8 días en comparación con 604,4 días entre 7.517 mujeres tratadas con tetraciclinas (p <0,001). Esto sugiere que la ESP tiene una buena efectividad y tolerabilidad a largo plazo |
ECA: ensayo clínico aleatorizado; ESP: espironolactona; NR: no registrado.
Una revisión sistemática de la base Cochrane del año 200935 concluyó que esta evidencia era insuficiente para demostrar la eficacia de espironolactona en el acné. Al respecto, una revisión sistemática híbrida realizada posteriormente concluye que, pese a la escasez de estudios de alta calidad, no se puede asegurar la ineficacia del fármaco11. Con base en los resultados de los ensayos clínicos y estudios retrospectivos, diversas guías clínicas recomiendan el uso de espironolactona en el tratamiento del acné20,36. Según la guía americana de tratamiento del acné del año 2016, la espironolactona tendría un nivel de evidencia ii-iii, con una fuerza de recomendación B. La guía europea de tratamiento del acné del año 2016 no la incluye entre los fármacos evaluados/recomendados37.
Considerando que la espironolactona es un fármaco seguro con unos efectos adversos mínimos, puede ser una opción terapéutica en mujeres sanas de cualquier edad. De hecho, 3 de los estudios observacionales evaluaron su eficacia y tolerancia en pacientes adolescentes desde los 12 años28,30,32. La espironolactona puede ser una alternativa a los antibióticos sistémicos e inclusive debería considerarse en los casos de fracaso a isotretinoína, que en mujeres adultas puede llegar al 32%38. Puede ser especialmente útil en la mujer adulta con acné tardío/persistente, donde la tasa de fracaso a otras terapias puede llegar hasta el 82%38. Es importante destacar que la recaída postratamiento con isotretinoína puede ser un factor predictor de buena respuesta a espironolactona (odds ratio: 2,46; intervalo de confianza del 95%: 1,09-5,54; p=0,03)31. Cabe señalar que no se disponen de estudios comparativos entre espironolactona e isotretinoína en el tratamiento del acné.
En nuestra experiencia, hemos utilizado espironolactona en mujeres adolescentes desde los 12 años y adultas hasta los 40 años, recomendando anticoncepción estricta, sin necesidad de realizar pruebas complementarias, con una muy buena tolerancia y sin efectos adversos significativos. No la utilizamos en hombres dado el riesgo de ginecomastia y de disminución de la libido10,38. Preferimos iniciar a dosis de 25mg/día durante una semana para luego aumentar a 50mg/día (y mantener esta dosificación en la mayoría de las pacientes). No hemos necesitado utilizar dosis superiores a 100mg/día. Es frecuente que la combinemos con anticonceptivos mixtos de acción antiandrogénica de tercera o cuarta generación como la combinación de 2mg de dienogest y 0,03mg de etinilestradiol. La asociación con anticonceptivos mixtos antiandrogénicos de primera o segunda generación pueden disminuir la eficacia de la espironolactona31, por lo que se deben evitar, al igual que los anticonceptivos con progestágenos, sobre todo los pregnanos (acetato de medroxiprogesterona y acetato de progesterona) y los derivados de la nortestosterona de primera (linestrenol) y segunda generación (levonorgestrel), los que pueden empeorar el acné39. Los comprimidos de espironolactona son fraccionables y se encuentran en presentaciones de 25 y 100mg (tabla 2). Consideramos que la espironolactona debería ser parte del arsenal terapéutico de uso habitual en el manejo del acné (nivel de evidencia ii-iii, fuerza de recomendación B) y podría disminuir la utilización de antibióticos sistémicos y, por ende, de la resistencia antibiótica (tabla 4).
Beneficios potenciales de la espironolactona en el tratamiento del acné
| Disminución del uso de antibióticos sistémicos |
| Podría disminuir la resistencia antibiótica del Cutinebacterium acne |
| Fármaco seguro, con mínimos efectos adversos en mujeres sanasNo es fototóxico |
| No requiere pruebas complementarias rutinarias en mujeres sanas menores de 45 años |
La HS es una enfermedad inflamatoria crónica de etiopatogenia poco clara y aparentemente multifactorial. El factor común inicial es la oclusión del folículo piloso y su posterior inflamación, favorecido por una desregulación del sistema inmunitario innato y adaptativo. Tras la oclusión, el folículo se rompe y su contenido rico en queratina y bacterias se derrama en la dermis circundante, induciendo una respuesta quimiotáctica mediada por neutrófilos y linfocitos. Este infiltrado inflamatorio genera la formación de abscesos y la destrucción de la unidad pilo-sebácea40,41. El factor hormonal parece ser determinante, ya que los andrógenos pueden generar oclusión folicular por una mayor proliferación de queratinocitos foliculares, generando acantosis intrafolicular, queratosis y taponamiento40. Además, existe evidencia de que la HS predomina en mujeres, iniciándose generalmente en la pubertad, mejora con la menopausia y la gravedad puede cambiar con relación a la menstruación y embarazo42,43.
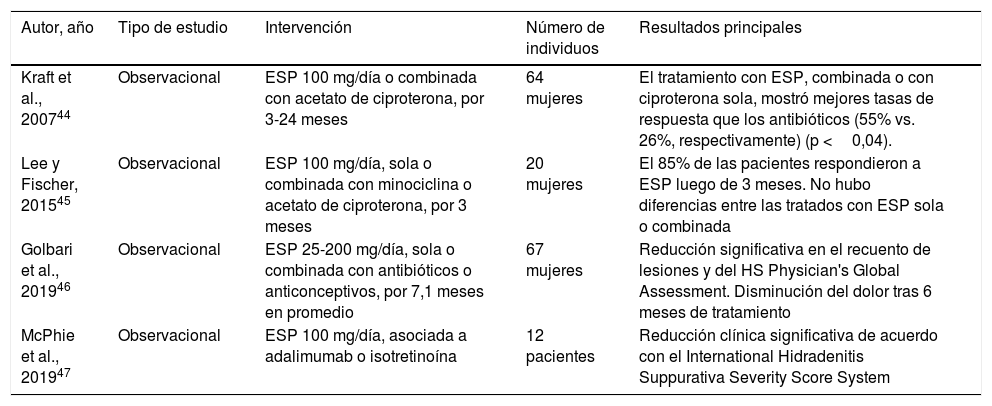
No existen ensayos clínicos controlados que evalúen la eficacia de la espironolactona en la HS. Hemos encontrando solo 4 estudios observacionales, que incluyen en total a alrededor de 150 pacientes, y muestran la utilidad del fármaco en esta patología44-47 (tabla 5). En la serie más numerosa hasta la fecha (n=67)46, el uso de espironolactona disminuyó significativamente el número de lesiones y la puntuación del Hidradenitis Suppurativa-Physician's Global Assessment a los 3 meses. Además, redujo el dolor evaluado con una escala numérica a los 6 meses. No se objetivaron diferencias entre dosis altas o bajas. Una revisión sistemática reciente concluyó que faltan estudios de buena calidad que permitan dar una recomendación sólida sobre su uso en HS48.
Estudios que avalan el uso de espironolactona en hidradenitis supurativa
| Autor, año | Tipo de estudio | Intervención | Número de individuos | Resultados principales |
|---|---|---|---|---|
| Kraft et al., 200744 | Observacional | ESP 100 mg/día o combinada con acetato de ciproterona, por 3-24 meses | 64 mujeres | El tratamiento con ESP, combinada o con ciproterona sola, mostró mejores tasas de respuesta que los antibióticos (55% vs. 26%, respectivamente) (p <0,04). |
| Lee y Fischer, 201545 | Observacional | ESP 100 mg/día, sola o combinada con minociclina o acetato de ciproterona, por 3 meses | 20 mujeres | El 85% de las pacientes respondieron a ESP luego de 3 meses. No hubo diferencias entre las tratados con ESP sola o combinada |
| Golbari et al., 201946 | Observacional | ESP 25-200 mg/día, sola o combinada con antibióticos o anticonceptivos, por 7,1 meses en promedio | 67 mujeres | Reducción significativa en el recuento de lesiones y del HS Physician's Global Assessment. Disminución del dolor tras 6 meses de tratamiento |
| McPhie et al., 201947 | Observacional | ESP 100 mg/día, asociada a adalimumab o isotretinoína | 12 pacientes | Reducción clínica significativa de acuerdo con el International Hidradenitis Suppurativa Severity Score System |
ESP: espironolactona; HS: hidradenitis supurativa.
A diferencia del uso de espironolactona en acné, en el que dosis de 50mg/día pueden ser eficaces, en HS se sugiere el uso de dosis más altas, desde 100 a 200mg/día, hecho que es concordante con nuestra experiencia en la práctica clínica. Creemos que la espironolactona puede ser una alternativa a considerar en esta patología, dado su bajo coste y buen perfil de seguridad, pese a la relativamente escasa evidencia disponible.
Espironolactona en las alopecias femeninasLa FAGA es el trastorno de caída de cabello más común en mujeres y su origen es poligénico y multifactorial. Si bien en la patogenia de la alopecia androgenética masculina el papel de las hormonas sexuales está claramente establecido, esto es menos claro en las mujeres. Ciertos factores genéticos predispondrían a que los receptores de andrógenos estén especialmente sensibilizados para unirse a los andrógenos circulantes, aun con unos niveles circulantes normales.
Se cree que la FAGA estaría mediada por los andrógenos, dado que se manifiesta habitualmente en mujeres posmenopáusicas2 y puede presentarse más precozmente en individuos con hiperandrogenismo. En el cuero cabelludo, los andrógenos tienen un efecto paradójico en las papilas dérmicas, ya que genera la transición de pelos terminales a vellos, en individuos genéticamente predispuestos2,49.
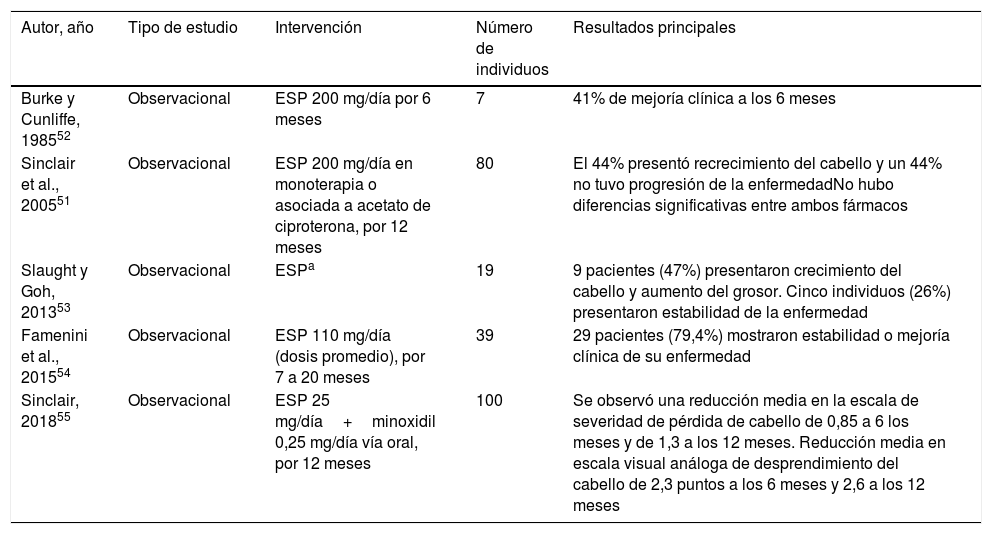
La espironolactona se suele utilizar hace varios años fuera de indicación en la FAGA, siendo el principal antiandrógeno indicado en Estados Unidos con este fin, pese a no contar con ensayos clínicos controlados50. Sinclair et al. describieron una serie de 40 mujeres tratadas con espironolactona 200mg/día y 40 mujeres con acetato de ciproterona durante 12 meses (la mayoría sin evidencia de hiperandrogenismo) donde el 44% presentó recrecimiento del cabello y otro 44% no tuvo progresión de la enfermedad. No hubo diferencias significativas entre ambos fármacos51. También se han visto resultados favorables en otros estudios observacionales52-54, incluyendo uno con espironolactona asociada a minoxidil oral55, y un caso asociado a minoxidil tópico56 (tabla 6). Sin embargo, hasta la fecha, tal como una revisión Cochrane de 2016 concluyó, faltan estudios clínicos controlados que evalúen la efectividad real de este fármaco en la FAGA57.
Estudios que avalan el uso de espironolactona en alopecia androgenética de patrón femenino
| Autor, año | Tipo de estudio | Intervención | Número de individuos | Resultados principales |
|---|---|---|---|---|
| Burke y Cunliffe, 198552 | Observacional | ESP 200 mg/día por 6 meses | 7 | 41% de mejoría clínica a los 6 meses |
| Sinclair et al., 200551 | Observacional | ESP 200 mg/día en monoterapia o asociada a acetato de ciproterona, por 12 meses | 80 | El 44% presentó recrecimiento del cabello y un 44% no tuvo progresión de la enfermedadNo hubo diferencias significativas entre ambos fármacos |
| Slaught y Goh, 201353 | Observacional | ESPa | 19 | 9 pacientes (47%) presentaron crecimiento del cabello y aumento del grosor. Cinco individuos (26%) presentaron estabilidad de la enfermedad |
| Famenini et al., 201554 | Observacional | ESP 110 mg/día (dosis promedio), por 7 a 20 meses | 39 | 29 pacientes (79,4%) mostraron estabilidad o mejoría clínica de su enfermedad |
| Sinclair, 201855 | Observacional | ESP 25 mg/día+minoxidil 0,25 mg/día vía oral, por 12 meses | 100 | Se observó una reducción media en la escala de severidad de pérdida de cabello de 0,85 a 6 los meses y de 1,3 a los 12 meses. Reducción media en escala visual análoga de desprendimiento del cabello de 2,3 puntos a los 6 meses y 2,6 a los 12 meses |
ESP: espironolactona.
Al igual que en el HS, en la FAGA la evidencia disponible sugiere que se requieren dosis de 100 a 200mg/día. En nuestra experiencia, hemos utilizado espironolactona asociada a minoxidil tópico en mujeres mayores de 30 años, con una buena respuesta, utilizando generalmente dosis iniciales de 50mg/día, para luego de una o 2semanas aumentar a 100mg/día, no requiriendo habitualmente dosis superiores.
En la alopecia frontal fibrosante se ha descrito el uso fuera de indicación de espironolactona solo en casos aislados; no existen estudios observacionales ni ensayos clínicos controlados58,59.
Espironolactona en el hirsutismoEl hirsutismo es un trastorno común en mujeres en edad fértil, con un importante efecto en la calidad de vida. Se caracteriza por el crecimiento de pelos terminales siguiendo un patrón masculino, en las áreas sensibles a andrógenos, tales como: el mentón, el labio superior o el tronco1,60. La principal causa es el síndrome de ovario poliquístico, seguido de la idiopática. Los andrógenos desempeñan un papel crítico en el hirsutismo, independiente de los niveles de andrógenos sistémicos, ya que en el folículo pilo-sebáceo existe una elevada actividad de la 5-alfa-reductasa. La escala de Ferriman-Gallwey es la más utilizada para evaluar el hirsutismo y considera 11 sitios corporales a través de un puntaje, categorizando a la paciente en normal, hirsutismo leve, moderado o severo60,61.
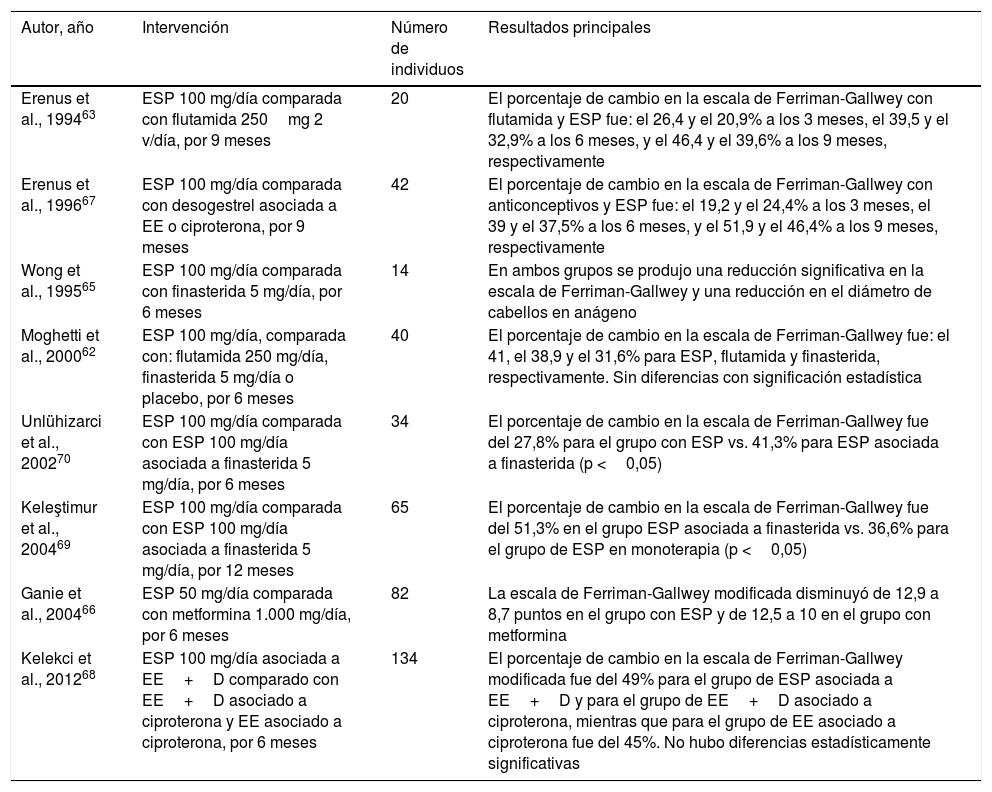
La espironolactona se ha sugerido como tratamiento del hirsutismo fuera de indicación. A diferencia del uso de este fármaco en el acné, la FAGA y el HS, se cuenta con varios ensayos clínicos aleatorizados que justifican su uso. En una revisión Cochrane del año 201561, se encontró que la espironolactona 100mg/día fue más efectiva que el placebo para reducir las puntuaciones de la escala Ferriman-Gallwey. Además, tuvo similar efectividad que la flutamida y el finasterida en 2estudios comparativos con estos fármacos62,63. Pese a esto, se destaca que la evidencia disponible es de baja calidad. A su vez, una revisión sistemática previa64, que evaluó los resultados de 26 ensayos clínicos controlados de diversos antiandrógenos, demostró que la espironolactona 100mg/día mejoró la puntuación de la escala de Ferriman-Gallwey en un 38,4% de promedio, siendo superior a finasterida y similar a los anticonceptivos orales y a la flutamida. Otros ensayos clínicos han avalado la efectividad del uso de espironolactona en monoterapia65,66 asociada a anticonceptivos orales67,68 y finasterida69,70, siendo superior la combinación que su uso en monoterapia (tabla 7).
Ensayos clínicos aleatorizados sobre el uso de espironolactona en hirsutismo
| Autor, año | Intervención | Número de individuos | Resultados principales |
|---|---|---|---|
| Erenus et al., 199463 | ESP 100 mg/día comparada con flutamida 250mg 2 v/día, por 9 meses | 20 | El porcentaje de cambio en la escala de Ferriman-Gallwey con flutamida y ESP fue: el 26,4 y el 20,9% a los 3 meses, el 39,5 y el 32,9% a los 6 meses, y el 46,4 y el 39,6% a los 9 meses, respectivamente |
| Erenus et al., 199667 | ESP 100 mg/día comparada con desogestrel asociada a EE o ciproterona, por 9 meses | 42 | El porcentaje de cambio en la escala de Ferriman-Gallwey con anticonceptivos y ESP fue: el 19,2 y el 24,4% a los 3 meses, el 39 y el 37,5% a los 6 meses, y el 51,9 y el 46,4% a los 9 meses, respectivamente |
| Wong et al., 199565 | ESP 100 mg/día comparada con finasterida 5 mg/día, por 6 meses | 14 | En ambos grupos se produjo una reducción significativa en la escala de Ferriman-Gallwey y una reducción en el diámetro de cabellos en anágeno |
| Moghetti et al., 200062 | ESP 100 mg/día, comparada con: flutamida 250 mg/día, finasterida 5 mg/día o placebo, por 6 meses | 40 | El porcentaje de cambio en la escala de Ferriman-Gallwey fue: el 41, el 38,9 y el 31,6% para ESP, flutamida y finasterida, respectivamente. Sin diferencias con significación estadística |
| Unlühizarci et al., 200270 | ESP 100 mg/día comparada con ESP 100 mg/día asociada a finasterida 5 mg/día, por 6 meses | 34 | El porcentaje de cambio en la escala de Ferriman-Gallwey fue del 27,8% para el grupo con ESP vs. 41,3% para ESP asociada a finasterida (p <0,05) |
| Keleştimur et al., 200469 | ESP 100 mg/día comparada con ESP 100 mg/día asociada a finasterida 5 mg/día, por 12 meses | 65 | El porcentaje de cambio en la escala de Ferriman-Gallwey fue del 51,3% en el grupo ESP asociada a finasterida vs. 36,6% para el grupo de ESP en monoterapia (p <0,05) |
| Ganie et al., 200466 | ESP 50 mg/día comparada con metformina 1.000 mg/día, por 6 meses | 82 | La escala de Ferriman-Gallwey modificada disminuyó de 12,9 a 8,7 puntos en el grupo con ESP y de 12,5 a 10 en el grupo con metformina |
| Kelekci et al., 201268 | ESP 100 mg/día asociada a EE+D comparado con EE+D asociado a ciproterona y EE asociado a ciproterona, por 6 meses | 134 | El porcentaje de cambio en la escala de Ferriman-Gallwey modificada fue del 49% para el grupo de ESP asociada a EE+D y para el grupo de EE+D asociado a ciproterona, mientras que para el grupo de EE asociado a ciproterona fue del 45%. No hubo diferencias estadísticamente significativas |
D: drospirenona; EE: etinil-estradiol; ESP: espironolactona.
El acné, la HS, la FAGA y el hirsutismo son enfermedades de origen multifactorial, donde el efecto hormonal mediado por andrógenos es uno de los pilares esenciales. La espironolactona, diurético ahorrador de potasio con efecto antiandrogénico, de bajo coste y buen perfil de seguridad, puede ser de utilidad en la práctica clínica en el manejo de estas enfermedades. Consideramos de especial interés su uso dentro de las primeras líneas de tratamiento del acné femenino, donde podría disminuir el uso de antibióticos, evitando la selección de patógenos con resistencia antibiótica y, probablemente, disminuir los costes asociados.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.