No se dispone de datos españoles sobre el coste asociado al linfoma cutáneo de célulasT (LCCT). Además, la incorporación de nuevos tratamientos hace necesario analizar el coste real de la enfermedad. El estudio MICADOS analizó dos objetivos principales: Por un lado, evaluó el impacto en la calidad de vida en los pacientes con LCCT, y por otro lado, estudió los costes de la enfermedad. En esta publicación se recoge el segundo de los objetivos del estudio.
MétodosEl coste de la enfermedad se estudió bajo la perspectiva del Sistema Nacional de Salud (SNS) con un horizonte temporal de un año. Participaron 23 dermatólogos y hematólogos de 15 hospitales públicos españoles. Se incluyeron pacientes adultos con LCCT del tipo micosis fungoide (MF) y síndrome de Sézary (SS).
ResultadosSe incluyeron 141 pacientes, el 57,4% masculinos, con una edad media de 63,6 años (IC95%: 61,4-65,7). Los costes directos anuales medios por pacientes del estudio fueron de 34.214€, siendo de 11.952,47€ en estadioI, 23.506,21€ en estadioII, 38.771,81€ en estadioIII y 72.748,84€ en estadioIV. El coste anual directo total estimado de todos los pacientes en España con MF/SS resultó en 78.301.171€, donde el 81% de los costes fueron atribuibles a pacientes en estadioI, el 7% al estadioII, el 6% al estadioIII y el 6% al estadioIV.
ConclusionesEste estudio ofrece una evaluación precisa del coste directo del LCCT en pacientes con MF/SS en España, mostrando costes que varían sustancialmente en función del estadio. Los costes soportados por el paciente y los costes indirectos deberán considerarse en futuras investigaciones.
The cost of treating cutaneous T-cell lymphoma (CTCL) in Spain is unknown. With the advent of new treatments, it is more important than ever to gain an accurate picture of the true costs involved. The MICADOS study had 2 primary objectives: 1)to evaluate the impact of CTCL on patient quality of life, and 2)to evaluate the costs associated with the disease. This article reports the results of the cost analysis.
MethodsWe estimated the cost of treating CTCL over a period of 1year from the perspective of the Spanish National Health System. Twenty-three dermatologists and hematologists from 15 public hospitals analyzed data for adult patients with mycosis fungoides (MF) or Sézary syndrome (SS).
ResultsA total of 141 patients (57.4% male) with a mean age of 63.6 years (95%CI: 61.4-65.7 years) were included. The mean direct annual cost of treating CTCL was €34,214 per patient. The corresponding costs by stage were €11,952.47 for stageI disease, €23,506.21 for stageII disease, €38,771.81 for stageIII disease, and €72,748.84 for stageIV disease. The total direct annual cost of treating MF/SS in public hospitals in Spain was estimated at €78,301,171; stageI disease accounted for 81% of all costs, stageII for 7%, and stagesIII andIV for 6% each.
ConclusionsThe MICADOS study offers an accurate picture of the direct cost of treating CTCL in patients with MF/SS in Spain and shows that costs vary significantly according to disease stage. Patient-borne and indirect costs should be analyzed in future studies.
El linfoma cutáneo de células T (LCCT) se considera una enfermedad rara por su baja incidencia, afectando a 2,9-3,9/1.000.000 personas en Europa1,2. Más de dos tercios de los LCCT son micosis fungoide (MF) y síndrome de Sézary (SS)3.
Al inicio de la enfermedad los pacientes presentan lesiones cutáneas en forma de parches, placas o tumores. El linfoma puede extenderse hacia la sangre periférica, los ganglios linfáticos y las vísceras, empeorando el pronóstico4,5. Según avanza el estadio, el pronóstico empeora drásticamente, pasando de una supervivencia de 35,5años en estadioIA a supervivencias menores de 5años a partir del estadioIIB6,7.
La European Society of Medical Oncology (ESMO) y la European Organisation for Research and Treatment of Cancer (EORTC) recomiendan diferentes tratamientos en función del estadio clínico5,8,9. En España, el registro del grupo español de linfoma cutáneo en el año 2008 mostró que las terapias dirigidas a la piel más administradas eran los corticosteroides tópicos, en el 90,8% de los pacientes, seguido de PUVA, en el 47,1%, y la fototerapia con UVBBE, en el 35,3%. En relación con los tratamientos sistémicos, los más administrados fueron interferón alfa en el 12,1%, quimioterapia sistémica en el 8,6% y retinoides sistémicos en el 6,9%10.
El objetivo principal de este estudio fue determinar el coste de la enfermedad en pacientes con MF/SS en España en función de su estadio clínico y explorar los factores sociodemográficos y clínicos que se pudieran relacionar con mayores costes.
MétodosSe diseñó un estudio observacional, transversal y retrospectivo, autorizado por el Comité de ética del Hospital Universitario 12 de Octubre de Madrid (14/01/2020; Código 20/018). Se siguieron las recomendaciones de estudios de coste de la enfermedad y para estudios de evaluación económica (CHEERS)11.
Participaron 23 médicos dermatólogos y hematólogos pertenecientes a 15 hospitales públicos españoles, que incluyeron pacientes entre mayo de 2020 y enero de 2021.
La perspectiva del estudio fue la del Sistema Nacional de Salud (SNS) español con horizonte temporal de un año sin aplicar tasas de descuento. Los resultados se presentan en euros (€) de 2020 con impuestos incluidos.
Se incluyeron pacientes de ambos sexos, mayores de 18años; con diagnóstico anatomopatológico de LCCT de tipo MF o SS, según la clasificación OMS12, confirmado al menos 1año antes de la inclusión en el estudio; en cualquier estadio. Los pacientes firmaron el consentimiento informado.
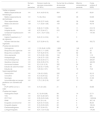
Para el objetivo principal se diseñó un modelo económico para recoger información en el momento de la realización del estudio y durante el año previo, registrando el nombre comercial o el tipo de intervención, la dosis unitaria y sus unidades, el número de dosis diarias administradas, la vía de administración y la fecha de inicio y finalización del tratamiento. También se recogió el número de unidades consumidas de cada recurso sanitario, incluyendo visitas e ingresos, pruebas de laboratorio y pruebas de imagen. Los tratamientos que estaban recibiendo los pacientes en el momento del estudio se muestran en la tabla 1, mientras que los costes unitarios de los recursos sanitarios y de los tratamientos farmacológicos y no farmacológicos se muestran en las tablas 2 y 3. En la tabla suplementaria 1 (ver material suplementario) se muestra el coste de las intervenciones terapéuticas no farmacológicas dependiendo del número de pacientes y del número de sesiones durante el último año.
Tratamientos administrados a los pacientes en el momento actual
| Tratamiento actual | Estadio del paciente en el momento actual | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| I | II | III | IV | Total | ||||||
| T | % | T | % | T | % | T | % | T | % | |
| Ninguno | 25 | 46,3 | 9 | 18,8 | 5 | 17,2 | 6 | 10,2 | 45 | 23,7 |
| Corticosteroide tópico | 11 | 20,4 | 10 | 20,8 | 3 | 10,3 | 6 | 10,2 | 30 | 15,8 |
| Retinoide | 6 | 11,1 | 11 | 22,9 | 8 | 27,6 | 8 | 13,6 | 33 | 17,4 |
| Fotoexposición solar | 1 | 1,9 | 0 | 0 | 0 | 0 | 0 | 0 | 1 | 0,5 |
| PUVA | 1 | 1,9 | 2 | 4,2 | 0 | 0 | 0 | 0 | 3 | 1,6 |
| UVBBE | 0 | 0 | 0 | 0 | 0 | 0 | 1 | 1,7 | 1 | 0,5 |
| TSEBT | 0 | 0 | 4 | 8,3 | 0 | 0 | 1 | 1,7 | 5 | 2,6 |
| Corticosteroide sistémico | 1 | 1,9 | 1 | 2,1 | 3 | 10,3 | 1 | 1,7 | 6 | 3,2 |
| Fotoféresis extracorpórea | 2 | 3,7 | 0 | 0 | 5 | 17,2 | 7 | 11,9 | 14 | 7,4 |
| Interferón alfa | 2 | 3,7 | 4 | 8,3 | 2 | 6,9 | 6 | 10,2 | 14 | 7,4 |
| Metotrexato | 0 | 0 | 0 | 0 | 0 | 0 | 1 | 1,7 | 1 | 0,5 |
| Anticuerpo monoclonal | 1 | 1,9 | 3 | 6,3 | 1 | 3,4 | 14 | 23,7 | 19 | 10 |
| Doxorubicina | 0 | 0 | 2 | 4,2 | 0 | 0 | 1 | 1,7 | 3 | 1,6 |
| Gemcitabina | 0 | 0 | 1 | 2,1 | 0 | 0 | 2 | 3,4 | 3 | 1,6 |
| Otros antineoplásicos | 0 | 0 | 1 | 2,1 | 0 | 0 | 4 | 6,8 | 5 | 2,6 |
| Alotrasplante de médula ósea | 1 | 1,9 | 0 | 0 | 0 | 0 | 1 | 1,7 | 2 | 1,1 |
| Antiviral | 1 | 1,9 | 0 | 0 | 0 | 0 | 0 | 0 | 1 | 0,5 |
| Antiinflamatorio | 2 | 3,7 | 0 | 0 | 0 | 0 | 0 | 0 | 2 | 1,1 |
| Hipolipemiante | 0 | 0 | 0 | 0 | 1 | 3,4 | 0 | 0 | 1 | 0,5 |
| Hormona | 0 | 0 | 0 | 0 | 1 | 3,4 | 0 | 0 | 1 | 0,5 |
| Total T | 54 | 100 | 48 | 100 | 29 | 100 | 59 | 100 | 190 | 100 |
Otros antineoplásicos: neoplásicos que no han sido recogidos en la tabla; PUVA: fototerapia con psoralenos y rayos ultravioleta A - Phototherapy with psoralens and ultraviolet A light; T: número de tratamientos de cada tipo en tratamiento actual; la suma total de tratamientos no coincide con el número total de pacientes debido a que un mismo paciente puede estar recibiendo más de un tratamiento simultáneamente; TSEBT: radioterapia total con haz de electrones - Total skin electron beam therapy; UVBBE: fototerapia con rayos ultravioleta B de banda estrecha - Narrow-band ultraviolet B phototherapy.
Consumo de recursos sanitarios durante el último año y coste unitario de cada recurso
| Número de pacientes | Número medio de recursos consumidos (IC 95%) | Suma total de unidades de recursos consumidas | Máximo consumido por paciente | Coste unitario (€ 2020) | |
|---|---|---|---|---|---|
| Visitas e ingresos | |||||
| Médico especialista de hematología | 141 | 6,41 (4,63-8,19) | 904 | 67 | 83,61 |
| Médico especialista de dermatología | 141 | 7,3 (6,2-8,4) | 1.029 | 38 | 63,68 |
| Otros especialistas | 141 | 3,42 (2,37-4,46) | 482 | 38 | 63,68 |
| Médico de atención primaria | 139 | 1,11 (0,63-1,58) | 154 | 22 | 44,79 |
| Urgencias | 141 | 0,38 (0,17-0,58) | 53 | 11 | 212,19 |
| Hospital de día | 140 | 4,37 (3,04-5,7) | 612 | 30 | 265,10 |
| Unidad de hospitalización domiciliaria | 141 | 0,01 (−0,01-0,02) | 1 | 1 | 147,93 |
| Ingreso hospitalario (n.° de ingresos) | 141 | 0,24 (0,14-0,34) | 34 | 3 | |
| Número total de días ingresado | 141 | 2,57 (0,99-4,15) | 362 | 80 | 502,72 |
| Pruebas de laboratorio | |||||
| Hemograma | 141 | 11,53 (8,48-14,59) | 1.626 | 146 | 4,15 |
| Bioquímica de urgencias | 141 | 2,05 (1,11-2,99) | 289 | 32 | 20 |
| Bioquímica completa | 141 | 7,97 (6,20-9,74) | 1.124 | 82 | 30 |
| Orina elemental | 141 | 0,74 (0,39-1,09) | 104 | 16 | 1,12 |
| Histopatología | 141 | 1,04 (0,75-1,32) | 146 | 11 | 316,69 |
| Inmunohistoquímica | 141 | 0,55 (0,40-0,71) | 78 | 5 | 209,67 |
| Genética molecular | 141 | 0,54 (0,35-0,73) | 76 | 8 | 422,09 |
| Hormonas tiroideas | 141 | 2,5 (1,81-3,18) | 352 | 24 | 38 |
| Estudio de autoinmunidad | 141 | 0,33 (0,17-0,49) | 47 | 6 | 55 |
| Estudio de hipercoagulabilidad | 141 | 1,09 (0,6-1,57) | 153 | 18 | 73,5 |
| Hemocultivo | 141 | 1,56 (0,5-2,62) | 220 | 47 | 20,10 |
| Urocultivo | 141 | 0,13 (0,05-0,2) | 18 | 3 | 12,75 |
| Serología | 141 | 0,69 (0,4-0,98) | 97 | 15 | 21,36 |
| Inmunofenotipo en sangre periférica con citometría de flujo | 141 | 1,75 (1,32-2,18) | 247 | 15 | 190 |
| PCR SARS-CoV-2 o CMV | 141 | 0,15 (0-0,30) | 21 | 8 | 83,88 |
| Pruebas de imagen | |||||
| Radiografía simple | 141 | 0,7 (0,43-0,98) | 99 | 14 | 27,71 |
| TAC | 141 | 0,67 (0,48-0,87) | 95 | 6 | 205 |
| PET-TAC | 141 | 0,35 (0,23-0,48) | 50 | 4 | 1.202,94 |
| RNM | 141 | 0,07 (0-0,14) | 10 | 4 | 307,18 |
| Ecografía convencional | 141 | 0,23 (0,14-0,33) | 33 | 4 | 80,34 |
| Ecografía doppler | 141 | 0,16 (0,09-0,23) | 22 | 2 | 160,34 |
| Electrocardiograma | 141 | 0,27 (0,04-0,5) | 38 | 16 | 99,39 |
| Linfogammagrafía | 141 | 0,01 (-0,01-0,02) | 1 | 1 | 176,95 |
Consumo de tratamientos farmacológicos y no farmacológicos durante el último año y sus costes unitarios
| Principio activo o intervención (unidades) | Vía de administración | Dosis unitaria | Número de pacientes que recibieron el tratamiento en un año (%) | Número total de dosis unitarias consumidas | Coste unitario (€ 2020) |
|---|---|---|---|---|---|
| Ningún tratamiento | − | − | 21 (14,9) | − | − |
| Tratamientos farmacológicos | |||||
| Aciclovir (mg) | Oral | 200 | 1 (0,7) | 60 | 0,39 |
| Acitretina (mg) | Oral | 10 | 4 (2,8) | 610 | 0,37 |
| Acitretina (mg) | Oral | 25 | 3 (2,1) | 805 | 0,94 |
| Alemtuzumab (mg) | Intravenosa | 12 | 1 (0,7) | 5 | 7.858,15 |
| Aprepitant (mg) | Oral | 125 | 1 (0,7) | 1 | 50,00 |
| Aprepitant (mg) | Oral | 80 | 1 (0,7) | 2 | 50,00 |
| Atezolizumab (mg) | Intravenosa | 840 | 3 (2,1) | 35 | 4.726,45 |
| Azatioprina (mg) | Oral | 50 | 1 (0,7) | 244 | 0,22 |
| Beclometasona dipropionato (mg/g) | Tópica | 0,25 | 1 (0,7) | 241 | 0,05 |
| Betametasona (ml) | Subcutánea | 2 | 1 (0,7) | 3 | 3,92 |
| Bexaroteno (mg) | Oral | 75 | 45 (31,9) | 49.543 | 13,09 |
| Brentuximab vedotina (mg/ml) | Intravenosa | 5 | 14 (9,9) | 105 | 3.490,15 |
| Ciclofosfamida (mg/ml) | Intravenosa | 1.000 | 2 (1,4) | 28 | 16,24 |
| Clorambucilo (mg) | Oral | 2 | 2 (1,4) | 50 | 0,07 |
| Deflazacort (mg) | Oral | 6 | 1 (0,7) | 365 | 0,19 |
| Doxorubicina hidrocloruro (2 mg/ml) | Intravenosa | 50 | 9 (6,4) | 78 | 42,62 |
| Ésteres etílicos de ácidos grasos omega-3 (mg) | Oral | 1.000 | 1 (0,7) | 21 | 0,41 |
| Fenofibrato (mg) | Oral | 145 | 1 (0,7) | 2 | 0,16 |
| Fenofibrato (mg) | Oral | 160 | 1 (0,7) | 33 | 0,18 |
| Fluticasona propionato (mg/g) | Tópica | 50 | 4 (2,8) | 1.096 | 0,16 |
| Gemcitabina (mg) | Intravenosa | 1.000 | 1 (0,7) | 2 | 68,22 |
| Gemcitabina (mg) | Intravenosa | 1.500 | 1 (0,7) | 6 | 102,33 |
| Gemcitabina (mg) | Intravenosa | 2.000 | 8 (5,7) | 46 | 136,44 |
| Gentamicina betametasona (mg/g) | Tópica | 1 | 1 (0,7) | 238 | 0,47 |
| Imiquimod (mg/g) | Tópica | 50 | 2 (1,4) | 1.570 | 3,15 |
| Interferón alfa (millones de unidades) | Subcutánea | 3 | 17 (12,1) | 8.880 | 21,04 |
| Lacutamab (mg/ml) | Intravenosa | 1 (0,7) | 2 | Ensayo clínico | |
| Levotiroxina sódica (mg) | Oral | 50 | 1 (0,7) | 40 | 0,03 |
| Metilprednisolona (mg) | Intravenosa | 1.000 | 1 (0,7) | 3 | 14,11 |
| Metilprednisolona aceponato (mg/g) | Tópica | 1 | 13 (9,2) | 1.281 | 0,23 |
| Metotrexato (mg) | Oral | 2,5 | 4 (2,8) | 66 | 0,10 |
| Metotrexato (mg/ml) | Subcutánea | 10 | 1 (0,7) | 52 | 13,75 |
| Metotrexato (mg/1,5 ml) | Subcutánea | 15 | 3 (2,1) | 80 | 20,64 |
| Metoxaleno (mg) | Oral | 10 | 1 (0,7) | 135 | 73,15 |
| Mogamulizumab (mg/5 ml) | Intravenosa | 20 | 14 (9,9) | 751 | 1.543,10 |
| Oxaliplatino (mg/20 ml) | Intravenosa | 100 | 2 (1,4) | 5 | 179,99 |
| Peginterferon alfa 2 A (μg) | Subcutánea | 90 | 2 (1,4) | 52 | 174,94 |
| Peginterferon alfa 2 A (μg) | Subcutánea | 180 | 3 (2,1) | 107 | 213,62 |
| Pimecrolimus (mg/g) | Tópica | 10 | 3 (2,1) | 917 | 1,14 |
| Prednisona (mg) | Oral | 10 | 7 (5) | 1.416 | 0,08 |
| Prednisona (mg) | Oral | 30 | 3 (2,1) | 733 | 0,13 |
| Propionato de clobetasol (mg/g) | Tópica | 0,5 | 28 (19,9) | 4.117 | 0,09 |
| Resminostat (mg) | Oral | 1 (0,7) | 22 | Ensayo clínico | |
| Romidepsina (mg/ml) | Intravenosa | 10 | 3 (2,1) | 44 | 1.998,76 |
| Triamcinolona acetónido (mg) | Intramuscular | 40 | 2 (1,4) | 24 | 2,39 |
| Vincristina (mg/ml) | Intravenosa | 1 | 2 (1,4) | 42 | 4,43 |
| Vorinostat (mg) | Oral | 100 | 1 (0,7) | 1.148 | 107,58 |
| Tratamientos no farmacológicos | |||||
| Fotoexposición solar | Percutánea | 1 | 2 (1,4) | − | 0 |
| Fotoféresis extracorpórea | Intravenosa | 1 | 20 (14,2) | 306 | 1.793,10 |
| ILD | Intravenosa | 1 | 1 (0,7) | 4 | 1.820 |
| PUVA | Percutánea | 1 | 13 (9,2) | 681 | 87,37 |
| Radioterapia local | Percutánea | 1 | 10 (7,1) | 114 | 65,11 |
| Trasplante alogénico de médula ósea | Intravenosa | 1 | 3 (2,1) | 3 | 67.470,15 |
| TSEBT | Percutánea | 1 | 13 (9,2) | 342 | 312,09 |
| UVBBE | Percutánea | 1 | 14 (9,9) | 526 | 136,08 |
ILD: infusión de linfocitos del donante; PUVA: fototerapia con psoralenos y rayos ultravioleta A - Phototherapy with psoralens and ultraviolet A light; TSEBT: radioterapia total con haz de electrones - Total skin electron beam therapy; UVBBE: fototerapia con rayos ultravioleta B de banda estrecha - Narrow-band ultraviolet B phototherapy.
Los costes médicos se calcularon multiplicando el número de recursos utilizados por su coste unitario. Estos costes unitarios se calcularon según el valor medio de los precios públicos de seis comunidades autónomas: Andalucía, Castilla y León, Galicia, Murcia, Madrid y País Vasco13-18.
Para los costes unitarios de los tratamientos farmacológicos se usó como referencia el Nomenclátor del Ministerio de Sanidad y Consumo19, de Vademecum (https://www.vademecum.es/). Los precios de los fármacos no comercializados en España se obtuvieron de bases de datos internacionales20,21.
Los precios de los tratamientos no farmacológicos se calcularon con el valor medio de los precios públicos de las comunidades autónomas13-18 y de la referencia de Ortiz-Romero et al.22.
Se recogió información sobre: edad, sexo, raza, enfermedades en tratamiento actual, peso, talla, fecha de la anatomía patológica diagnóstica, tipo de LCCT. Se registraron en el momento del diagnóstico, y cuando se realizó el estudio: clasificación TNMB, estadio clínico5, estado funcional ECOG y valor normal o elevado de lactato deshidrogenasa (LDH). Los pacientes completaron el cuestionario EORTC-QLQ-C30 versión3 para la evaluación de la calidad de vida relacionada con la salud en pacientes con cáncer23.
Para el cálculo de la muestra se consideró como referencia el coste mensual del cáncer de mama metastásico en España, que es de 1.489€. Para una desviación estándar de 250€, un nivel de confianza del 95% y una precisión de 41,68€ para la media, se estimó necesaria una muestra de 140 pacientes24.
Se realizó el análisis descriptivo de las variables cuantitativas con su media y el intervalo de confianza del 95%, mediante la prueba de t de Student para datos independientes, o por ANOVA con corrección de Bonferroni o Games-Howell, para el control del error por comparaciones múltiples. Las variables cualitativas fueron frecuencias y porcentajes para cada categoría de la variable y se realizaron mediante la prueba de Fisher o chi-cuadrado1. Dado que los costes no siguen una distribución normal, se aplicaron modelos de regresión lineal, ajustando respecto a las variables que pudieran estar asociadas con el uso de recursos. Las variables dependientes, como el coste total y los diferentes subtipos de costes analizados, se transformaron logarítmicamente25. Se utilizó el modelo lineal generalizado multivariante del coste total por paciente en función de diferentes covariables, seleccionando la familia Gamma y la función de enlace link logístico ya que mostraron los valores menores del estadístico AIC. El nivel de significación considerado fue del 5%. Se utilizó el programa IBM-SPSS 27.0 para el análisis estadístico.
ResultadosParticiparon 141 pacientes con una edad media de 63,6años (IC95%: 61,4-65,7), de los cuales el 77,3% eran MF y el 22,7% SS. En la tabla 4 se muestran los datos demográficos, antropométricos y clínicos de los pacientes. La edad de los pacientes en el momento del diagnóstico era de 56,2años (IC95%: 53,9-58,6). El tiempo medio de evolución de la enfermedad desde su diagnóstico fue de 6,7años (IC95%: 5,8-7,6). El estadio clínico fue IA en 37 pacientes (26,2%), IB en 12 pacientes (8,5%), IIA en 6 pacientes (4,3%), IIB en 31 pacientes (22%), IIIA en 13 pacientes (9,2%), IIIB en 4 (2,8%), IVA1 en 21 pacientes (14,9%), IVA2 en 15 pacientes (10,6%) y IVB en 2 pacientes (1,4%). Esto representa el 39% de los pacientes en enfermedad temprana (IA, IB y IIA) y el 61% en estadios avanzados.
Datos demográficos, antropométricos y clínicos de los pacientes
| n | % | |
|---|---|---|
| Sexo | ||
| Hombre | 81 | 57,4 |
| Mujer | 60 | 42,6 |
| Raza | ||
| Caucásica | 138 | 97,9 |
| Negra | 0 | 0 |
| Asiática | 1 | 0,7 |
| Hispana | 1 | 0,7 |
| Otra | 1 | 0,7 |
| Categorías según IMC | ||
| Caquexia IMC <20 kg/m2 | 8 | 5,8 |
| Normal IMC ≥20 y <25 kg/m2 | 47 | 33,8 |
| Sobrepeso IMC≥25 y <30 kg/m2 | 55 | 39,6 |
| Obesidad IMC≥30 kg/m2 | 29 | 20,9 |
| No evaluable | 2 | |
| Clasificación del linfoma cutáneo de células T | ||
| Micosis fungoide | 109 | 77,3 |
| Síndrome de Sézary | 32 | 22,7 |
| Estadio del paciente en el momento del diagnóstico | ||
| I | 68 | 48,9 |
| II | 26 | 18,7 |
| III | 21 | 15,1 |
| IV | 24 | 17,3 |
| Estado funcional ECOG en el momento del diagnóstico | ||
| ECOG-0 | 105 | 78,4 |
| ECOG-1 | 24 | 17,9 |
| ECOG-2 | 5 | 3,7 |
| ECOG-3 | 0 | 0 |
| No determinado | 7 | |
| LDH en el momento del diagnóstico | ||
| Normal | 71 | 71 |
| Elevada | 29 | 29,0 |
| No determinada | 41 | |
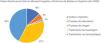
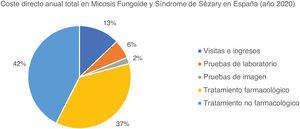
El coste directo anual total de la MF/SS fue de 78.301.171€, del cual el 42% corresponde a tratamientos farmacológicos, el 37% a tratamientos farmacológicos, el 13% son costes de visitas e ingresos, el 6% son costes de pruebas de laboratorio y el 2% son las pruebas de imagen (tabla 6, fig. 1). Si analizamos el coste directo anual medio por paciente vemos que fue de 34.214,97€, y que incrementaba conforme aumentaba el estadio de la enfermedad, siendo de 11.952,47€ en el estadioI hasta 72.748,84€ en elIV. Se observaron diferencias estadísticamente significativas entre pacientes en estadioI vs IV (p<0,0001), en estadioII vs IV (p<0,0001) y en estadioIII vs IV (p=0,021) (tabla 5).
Coste directo anual medio por paciente en función del estadio de la enfermedad y total, desagregado por tipo de recurso sanitario y por tratamiento farmacológico y no farmacológico
| Estadio I | Estadio II | Estadio III | Estadio IV | Todos los estadios | |
|---|---|---|---|---|---|
| Recursos sanitarios (€ 2020) | Coste anual medio e IC 95% por paciente (€ 2020) | Coste anual medio e IC 95% por paciente (€ 2020) | Coste anual medio e IC 95% por paciente (€ 2020) | Coste anual medio e IC 95% por paciente (€ 2020) | Coste anual medio e IC 95% por paciente (€ 2020) |
| Visitas e ingresos hospitalarios | 1.721,52 (166,13-3.276,91) | 2.878,78 (1.613,02-4.144,53) | 4.469,89 (1.073,96-7.865,82) | 7.189,21 (4.454,61-9.923,82) | 3.796,72 (2.729,05-4.864,40) |
| Pruebas de laboratorio | 796,10 (411,46-1.180,74) | 1.443,18 (997,55-1.888,82) | 1.981,19 (978,89-2.983,49) | 2.567,60 (1.975,23-3.159,96) | 1.586,21 (1.304,09-1.868,33) |
| Pruebas de imagen | 255,50 (95,68-415,32) | 661,45 (342,92-979,99) | 812,07 (287,62-1.336,53) | 1.178,18 (744,45-1.611,92) | 677,80 (506,98-848,62) |
| Coste de consumo de tratamientos farmacológicos | 4.106,79 (1.132,83-7.080,75) | 13.986,67 (6.617,74-21.355,60) | 20.114,22 (4.171,07-36.057,36) | 49.129,03 (31.301,87-66.956,19) | 20.763,01 (14.583,79-26.942,22) |
| Coste de tratamientos no farmacológicos | 6.191,25 (766,58-11.615,91) | 4.536,13 (1.760,92-7.311,33) | 11.394,44 (2.151,79-20.637,10) | 11.307,90 (5.032,73-17.583,06) | 7.763,22 (4.967,28-10.559,15) |
| Coste directo sanitario total | 11.952,47 (3.368,62-20.536,33) | 23.506,21 (15.380,02-31.632,39) | 38.771,81 (17.836,58-59.707,05) | 72.748,84 (53.435,75-92.061,93) | 34.213,97 (26.538,28-41.889,66) |
En la tabla 5 vemos también el coste anual medio por paciente desagregado por tipo de recurso sanitario, donde se observaron diferencias estadísticamente significativas en el coste anual medio por paciente por visitas e ingresos hospitalarios entre pacientes en estadioI vs estadioIV (p<0,0001), y en estadioII vs IV (p=0,016). Estas diferencias también se dan por pruebas de laboratorio entre pacientes en estadioI vs IV (p<0,0001), estadioI vs III (p=0,046) y estadioII vs IV (p=0,013).
De igual manera, en las pruebas de imagen hay diferencias entre pacientes en estadioI vs IV (p<0,0001). Sin embargo, no se observaron diferencias por tratamientos no farmacológicos.
Para el cálculo de la carga económica de la enfermedad bajo la perspectiva del SNS, se estimó la prevalencia por estadio según lo descrito en datos internacionales7, al no haber datos de prevalencia según estadio de MF/SS en España en la actualidad.
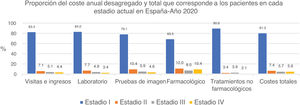
De manera similar, en la tabla 6 se presentan los resultados del coste directo anual total para los todos los pacientes con MF/SS en España en función del estadio de la enfermedad y desagregado por tipo de recurso. El gasto anual total estimado fue de 78.301.171€; de ellos, el 81,3% se atribuyó a los pacientes en estadioI, el 7,4% en estadioII, el 5,7% en estadioIII y el 5,6% en estadioIV. En la figura 2 se representa la proporción del coste anual total de cada tipo de recurso asignada a los pacientes por cada estadio. En el estadioI, el mayor porcentaje del gasto fueron los costes no farmacológicos, frente al estadioIV, donde el mayor porcentaje corresponde a los tratamientos farmacológicos.
Coste directo anual total en función del estadio de la enfermedad, desagregado por tipo de recurso sanitario y por tratamiento farmacológico y no farmacológico
| Estadio | I | II | III | IV | Todos los estadios |
|---|---|---|---|---|---|
| Número de casos prevalentes en España | n=4.872 | n=247 | n=115 | n=61 | n=5.295 |
| Coste anual (€ 2020) | Coste anual (€ 2020) | Coste anual (€ 2020) | Coste anual (€ 2020) | Coste anual (€ 2020) | |
| Visitas e ingresos hospitalarios | 8.387.245 | 711.059 | 514.037 | 438.542 | 10.050.883 |
| Pruebas de laboratorio | 3.878.599 | 356.465 | 227.837 | 156.624 | 4.619.525 |
| Pruebas de imagen | 1.244.796 | 163.378 | 93.388 | 71.869 | 1.573.431 |
| Tratamientos farmacológicos | 20.008.281 | 3.454.707 | 2.313.135 | 2.996.871 | 28.772.994 |
| Tratamientos no farmacológicos | 30.163.770 | 1.120.424 | 1.310.361 | 689.782 | 33.284.337 |
| Costes directos anuales totales | 63.682.692 | 5.806.034 | 4.458.758 | 4.353.687 | 78.301.171 |
En el análisis multivariante se observó una relación estadísticamente significativa del coste directo sanitario anual por paciente con la edad (p<0,0001), a mayor edad menor coste; el estadio del paciente en el momento actualI vs II (p<0,0001) a mayor estadio mayor coste, I vs III (p=0,009), I vs IV (p<0,0001).
DiscusiónDebido a las dificultades intrínsecas de la investigación de enfermedades raras, la realización de estudios de costes de la enfermedad, y en especial cuando hay nuevos tratamientos, es necesaria para dar una dimensión correcta al problema socioeconómico.
En el estudio encontramos que el coste directo sanitario anual medio por paciente en MF/SS fue de 34.214€. Estos resultados fueron comparables a los costes directos anuales medios por paciente en estadios metastásicos de los cánceres más comunes en España, y es notablemente superior a los costes de cánceres en estadios localizados. En primer lugar, tendríamos el cáncer colorrectal metastásico, con un coste medio anual de 34.738€, seguido del cáncer de mama, cuyo estadio metastásico tiene un coste de 35.732€, y el cáncer de pulmón, con un coste anual de 34.272€26. Sin embargo, el coste por paciente en MF/SS está por debajo del cáncer hematológico en estadio local y metastásico, que se estima en 55.578€ en ambos casos.
Con una incidencia anual estimada de 260 pacientes con MF/SS, se calculó que en España había 5.295 pacientes en el año 2020. El coste directo sanitario anual total de seguimiento y tratamiento de pacientes con MF/SS se valoró en 78.301.171€, atribuyendo el 81% de este coste a pacientes en estadio clínicoI (tabla 6, fig. 2). Asumiendo que todos los pacientes en estadioIV equivalen a pacientes con SS, podemos estimar el coste por patología, siendo así mucho más alto el coste anual medio por paciente en SS, con 71.317€, que en MF, estimado en 25.116€.
En el estudio se demostró un mayor coste directo sanitario anual en estadios avanzados de la enfermedad, pero costes menores cuando el paciente tenía mayor edad o mejor estado de calidad de vida (datos no mostrados).
La información sobre el coste de la enfermedad por LCCT es limitada, habiéndose descrito en tres estudios.
La American Academy of Dermatology (AAD) analizó el coste de la enfermedad de 24 afecciones dermatológicas registradas en el año 201327,28. En los pacientes estadounidenses se estimó un coste medio anual por paciente de 3.182,60$, suponiendo un coste anual total de 180 millones de dólares consumidos por 56.243 pacientes27,28. En nuestro estudio observamos un importe 10,8 veces mayor por paciente, pudiendo ser debido a que en la ADD no se incluyeron los costes de tratamientos no farmacológicos, sumado a la diferencia en el número de visitas necesarias.
En un segundo estudio, Semenov et al.29 estimaron el coste de la enfermedad a partir de los resultados de la calidad de vida de los pacientes, donde se encontró una pérdida de 1,48 AVAC por paciente. Considerando 50.000$ por AVAC, el coste de la enfermedad se estimó en 73.889$29. En nuestro estudio también se observó una relación significativa entre los costes y la calidad de vida, y una pérdida en la calidad de vida similar al deterioro de otros pacientes con cáncer.
Por último, en un tercer estudio, realizado en España, se analizó el coste de los tratamientos que se administraban en los estadios iniciales de la enfermedad, que osciló entre 7.426,42€ y 10.046,58€ en 6meses. En nuestro estudio se estimó un coste anual de 11.952,47€ y de 23.506,21€ en los pacientes en estadiosI yII, respectivamente, concordando con los datos del estudio español (tabla 5)22.
En nuestro estudio, más del 80% del coste de la enfermedad se atribuye a pacientes en estadioI (tabla 6, fig. 2) debido a que, aunque haya un coste medio menor (tabla 5), es el grupo más numeroso. Además, debido a que la mediana de supervivencia de los pacientes con MF/SS se estima en 18,3años, siendo mucho mayor en los pacientes en estadioI, el impacto económico de la enfermedad a lo largo de la vida es más alto.
El coste del cáncer en España desde la perspectiva social se ha estimado en 5.458 millones de euros en 2015, siendo 4.818 millones de euros costes directos (88,3%) y 640 millones de euros costes indirectos (11,7%)30. En general se ha estimado que el 55% de los costes del cáncer los asume el SNS, y el 45% restante las familias y los pacientes26. En nuestro estudio significaría que cada paciente con MF/SS soporta un coste de 27.993€ anuales en España; no obstante, no hay datos que constaten estos costes indirectos en MF/SS, y podrían ser motivo de estudios adicionales.
Nuestro estudio presenta varias limitaciones. La primera fue la exclusión de costes indirectos, subestimando así el coste real de la enfermedad. Sumado a ello, los estudios retrospectivos presentan limitaciones per se, en este caso, que haya costes no registrados que hayan podido infravalorar el coste real de LCCT.
Por último, debemos considerar que el estudio se realizó durante el año 2020, el año afectado mundialmente por la pandemia por SARS-CoV-2, limitando las visitas médicas. Los datos anuales registrados en el estudio abarcan desde mayo de 2019 hasta enero de 2021.
ConclusionesEl coste directo anual en España del LCCT se estimó en 78.301.171€, siendo el coste directo anual medio por paciente de 34.214,97€. El mayor impacto en costes para el SNS se observa en los estadios tempranos de la enfermedad, debido a la mayor proporción de pacientes en estadiosI/II frente a estadiosIII/IV. Cuando se analiza el coste anual medio por paciente, este aumenta según avanza el estadio de la enfermedad, siendo hasta 6 veces superior en estadioIV vs estadioI. El tipo de recurso sanitario que más contribuye a los costes directos totales de la enfermedad son los tratamientos no farmacológicos, seguido de los tratamientos farmacológicos y, en menor proporción, visitas e ingresos hospitalarios. En futuras evaluaciones, los costes del paciente y los costes indirectos debidos a la pérdida de productividad deberán considerarse para describir el impacto social real de la enfermedad.
FinanciaciónEl estudio fue financiado en su totalidad por Kyowa Kirin Farmacéutica, S.L.
Conflicto de interesesLos doctores Pablo Luis Ortiz Romero y Belén Navarro Matilla percibieron honorarios por la coordinación del estudio. Pablo Viguera y Julia Blanco son empleados de Kyowa Kirin Farmacéutica, S.L. Los demás autores declaran no tener conflictos de intereses.
Es una obligación agradecer a los pacientes que aceptaron participar en el estudio su generosidad y su colaboración desinteresada.
El proyecto fue desarrollado en el marco del programa Máster en Economía de la Salud y del Medicamento impartido por la UPF Barcelona School of Management, centro adscrito a la Universidad Pompeu Fabra.