INTRODUCCION
Los linfomas cutáneos de células T (LCCT) son neoplasias de linfocitos T en las que se agrupan varias entidades clínico-patológicas que difieren en sus características clínicas y pronostico, y que suelen requerir un tratamiento y seguimiento crónicos. Las formas clínicas más frecuentes son la micosis fungoide y el síndrome de Sézary, que conforman el 75 % de los LCCT y el 50 % de todos los linfomas cutáneos 1. El pronóstico depende del estadio clínico de la enfermedad en el momento de la presentación inicial. Así, mientras que los pacientes en estadios iniciales (IA) tienen una supervivencia equivalente a la de los individuos control, a partir de los estadios tumorales el pronóstico empeora y la supervivencia a los 5 años disminuye hasta el 40 % 2 (tabla 1).
Hoy por hoy no existe ningún tratamiento curativo para la micosis fungoide y el síndrome de Sézary. Ninguna de las opciones terapéuticas con las que contamos para el tratamiento de este grupo de enfermedades ha demostrado una prolongación en la supervivencia global por lo que el objetivo del tratamiento es el control de los síntomas y prevenir o lentificar la progresión de la enfermedad 3. La elección del tratamiento depende del estadio clínico y del estado general del paciente, y adquirir actitudes terapéuticas más agresivas en estadios iniciales no ofrece ninguna ventaja en cuanto a supervivencia 4.
El bexaroteno es un fármaco que forma parte de los llamados rexinoides, grupo de retinoides sintéticos agonistas de los receptores X de los retinoides. Aunque se desconoce su mecanismo de acción exacto, se sabe que actúa a través de los heterodímeros formados entre receptores X de los retinoides y los diversos receptores hormonales nucleares. Estos heterodímeros modulan la expresión de genes vitales, que desempeñan su función de tal forma que se inhibe la proliferación de células tumorales, induce su diferenciación y fomenta la apoptosis 5. La dosis óptima recomendada es de 300 mg/m 2/día y los efectos adversos más frecuentes son la hipertrigliceridemia y el hipotiroidismo central, que son dependientes de la dosis y reversibles una vez suspendido el tratamiento 6. El bexaroteno fue aprobado por la Food and Drug Administration (FDA) en diciembre de 1999 para el tratamiento de LCCT refractarios a al menos un tratamiento sistémico previo. Más allá de su aplicación en los LCCT, el papel del bexaroteno se ha estudiado en otras enfermedades, en especial los cánceres de mama y pulmón.
MATERIAL Y MÉTODOS
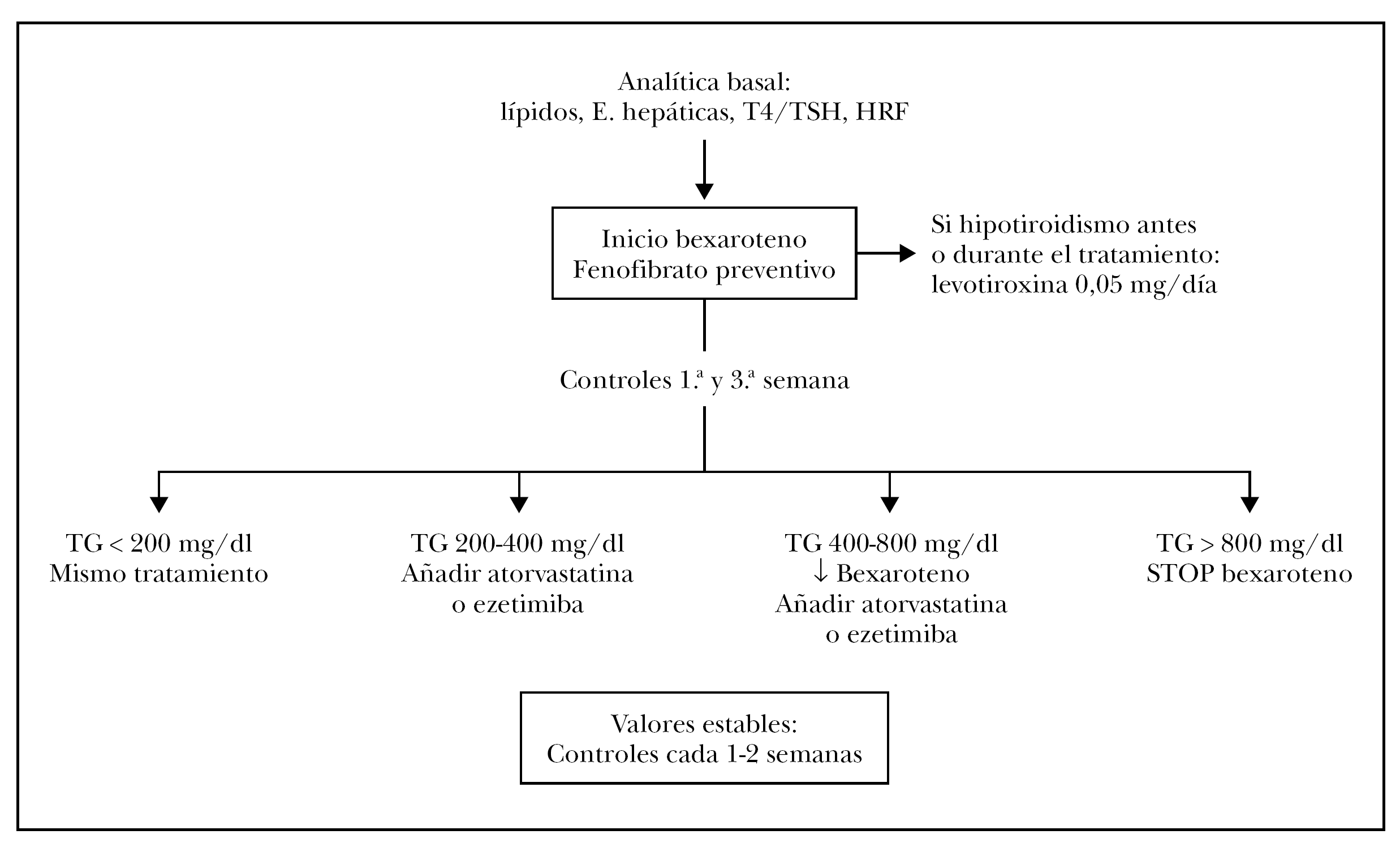
Realizamos un estudio descriptivo de los pacientes que han sido tratados con bexaroteno en la Unidad de Linfomas de nuestro servicio. Se trata de 9 pacientes diagnosticados de micosis fungoide y síndrome de Sézary refractarios a al menos un tratamiento sistémico previo. El tratamiento con bexaroteno se inicia en dosis de 300 mg/m 2/día, y desde el principio todos los pacientes reciben tratamiento hipolipemiante concomitante con fenofibrato. El algoritmo de tratamiento del bexaroteno que seguimos con nuestros pacientes está ilustrado en la figura 1. En un principio se realiza una analítica basal que determina los perfiles lipídicos y hepáticos, hormonas tiroideas y hematimetría. Una vez iniciado el tratamiento, se realizan controles analíticos a la semana y a las 3 semanas de iniciar el tratamiento y se analizan las concentraciones de triglicéridos, ajustando la dosis de bexaroteno y/o añadiendo un segundo agente hipolipemiante dependiendo de los resultados. Si el paciente desarrolla hipotiroidismo antes del tratamiento (frecuentemente precipitado por el interferón (IFN) con el que han sido tratados con anterioridad) o durante el tratamiento, se inicia terapia sustitutiva con levotiroxina hasta conseguir una cifra de T4 normal. Una vez conseguidos valores analíticos estables se realizan controles periódicos cada 1 o 2 meses.
Fig. 1.--Algoritmo de manejo del bexaroteno.
Describimos las características clínicas, tratamientos previos recibidos, eficacia del tratamiento, evolución y efectos adversos registrados en los pacientes tratados con bexaroteno.
RESULTADOS
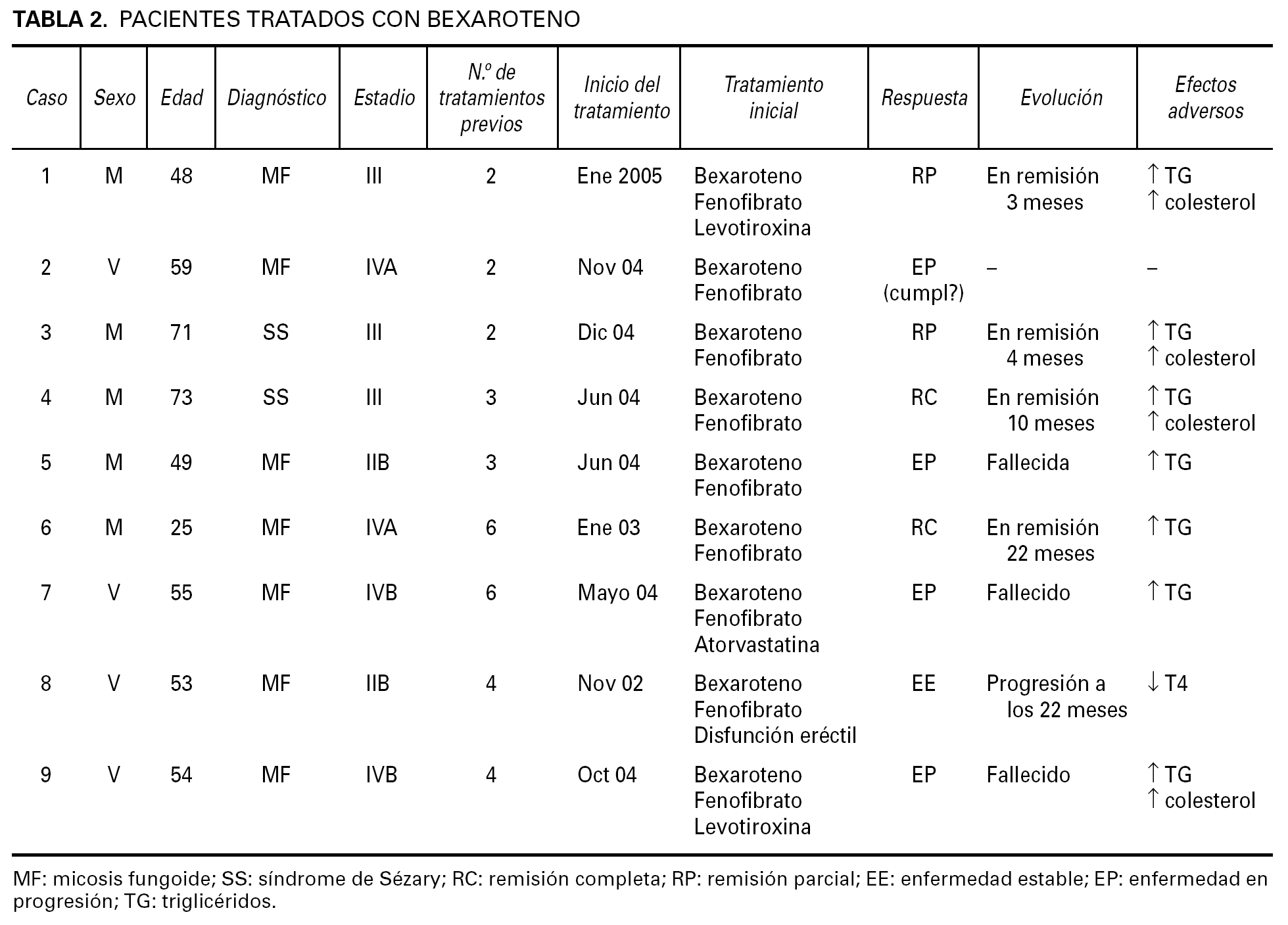
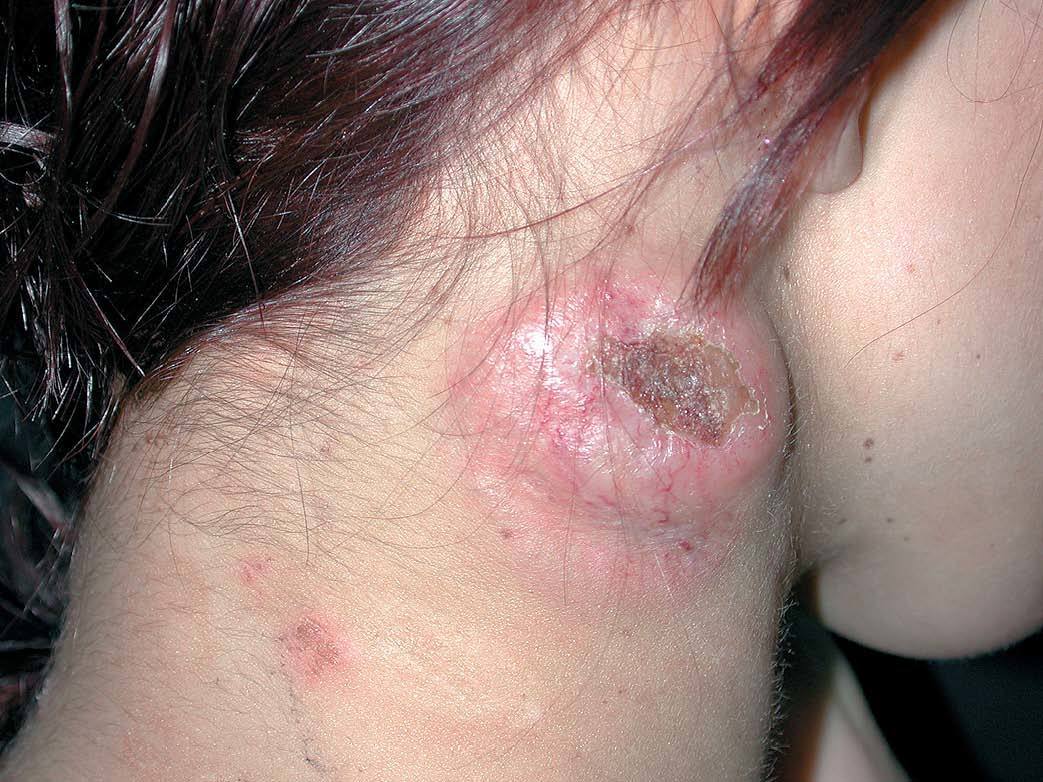
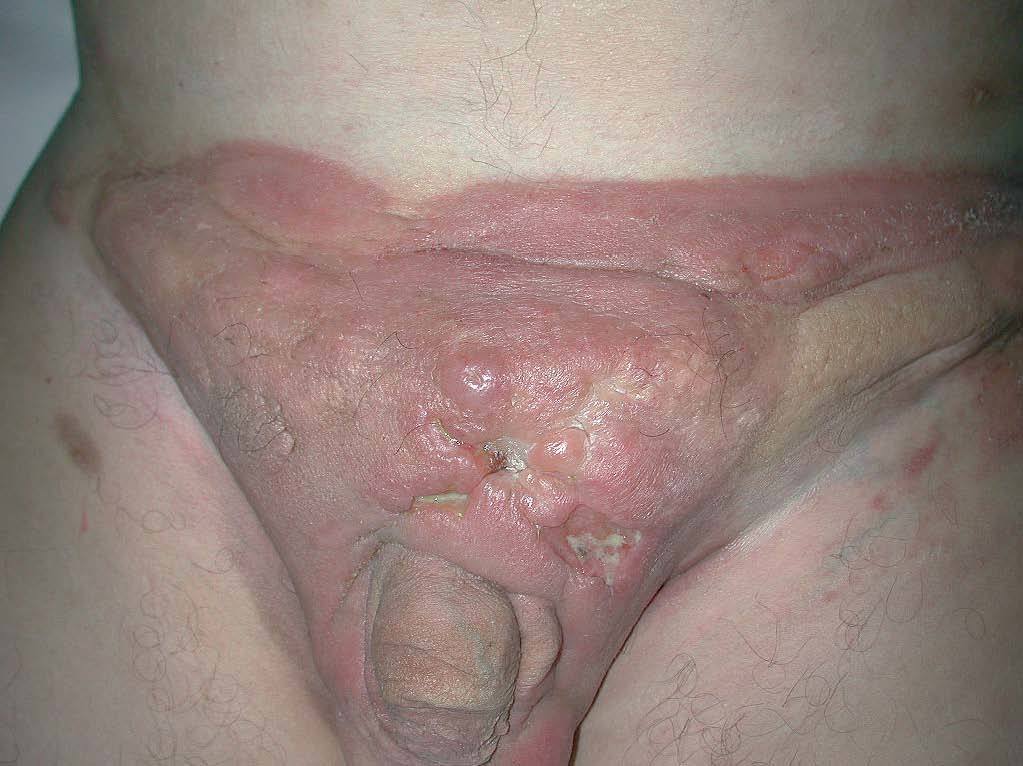
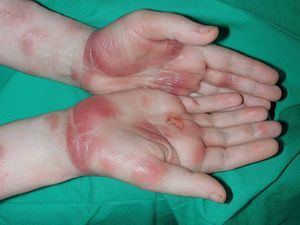
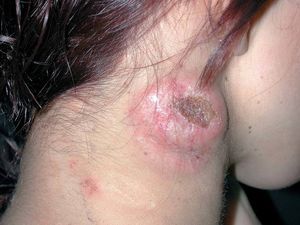
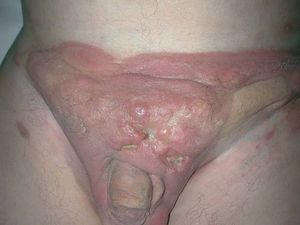
Los resultados obtenidos se resumen en la tabla 2. Hasta 9 pacientes han sido tratados con bexaroteno desde noviembre de 2002 hasta hoy, cinco de ellos mujeres y 4 hombres. La edad media de los pacientes era de 54 años con un rango de edad entre 25 y 73 años. El diagnóstico en 7 pacientes era de micosis fungoide y en los 2 casos restantes era de síndrome de Sézary. Todos los pacientes correspondían a estadios avanzados de la enfermedad, dos micosis fungoides tumorales (estadio IIB) (fig. 2), dos síndrome de Sézary y una micosis fungoide eritrodérmica (estadio III), 2 pacientes con afectación ganglionar (estadio IVA) (fig. 3) y otros 2 pacientes con metástasis viscerales (estadio IVB) (fig. 4).
Fig. 2.--Paciente con micosis fungoide tumoral (estadio IIB).
Fig. 3.--Micosis fungoide con afectación de ganglioma (estadio IVA).
Fig. 4.--Paciente con metástasis viscerales (estadio IVB).
Los pacientes habían recibido entre 2 y 6 tratamientos previos, entre los que se encuentran los corticoides tópicos, mostazas nitrogenadas, la fototerapia, las diferentes modalidades tópicas, el interferón y la radioterapia convencional entre los más frecuentes. Además, 3 pacientes habían sido tratados con tratamiento combinado con clorambucilo y prednisona, dos con acitretina, uno con metotrexato y la paciente más joven de nuestra serie había sido sometida previamente a un trasplante autólogo de progenitores hematopoyéticos y quimioterapia coadyuvante.
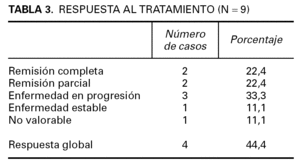
De acuerdo con la reducción de la masa tumoral y de la superficie corporal afectada, la respuesta al tratamiento se clasifica como remisión completa (resolución de más del 80 % de las lesiones), remisión parcial (mejoría de al menos el 50 %), enfermedad estable y enfermedad progresiva. La respuesta obtenida en nuestros pacientes está reflejada en la tabla 3. Presentaron una remisión completa 2 pacientes y otros dos, una remisión parcial. La tasa global de respuesta es de 4 pacientes, lo que en nuestra pequeña serie corresponde al 44,4 %. En lo que refiere al resto de pacientes, uno se mantuvo estable mientras estaba en tratamiento y en tres la enfermedad progresó a pesar del tratamiento. Consideramos no valorable la respuesta de uno de los casos porque dudamos del cumplimiento de la terapia por parte del paciente.
En cuanto a la evolución, los pacientes que tuvieron una respuesta completa al tratamiento se mantienen en remisión a los 22 y 10 meses de seguimiento. El primer caso es una mujer de 25 años diagnosticada de micosis fungoide estadio IVA y tratada previamente con 6 modalidades terapéuticas entre las que se incluye el trasplante autólogo de progenitores hematopoyéticos. Durante el tratamiento con bexaroteno se ha mantenido asintomática y no ha desarrollado nuevas lesiones tumorales. El segundo caso que obtuvo una remisión completa es una mujer de 73 años, diagnosticada de síndrome de Sézary, a la cual se le suspendió el tratamiento previo con clorambucilo y prednisona por los efectos adversos que desarrolló. Desde que inició el tratamiento con bexaroteno se mantiene asintomática y la alopecia secundaria que había desarrollado ha revertido completamente. Los pacientes que obtuvieron una respuesta parcial se mantienen en remisión a los 3 y 4 meses de seguimiento. El paciente con enfermedad estable ha presentado progresión de la enfermedad a los 22 meses de seguimiento. Por último, todos los pacientes que no respondieron al tratamiento fallecieron, dos de ellos por sepsis y otro por un accidente cerebrovascular agudo.
En cuanto a los efectos adversos registrados, los más frecuentes fueron la hipertrigliceridemia, la hipercolesterolemia y el hipotiroidismo central (tabla 4). En comparación con los efectos adversos registrados por Ligand Pharmaceuticals, nosotros no hemos tenido ningún caso de leucopenia, elevación de enzimas hepáticas, alopecia ni prurito por bexaroteno. Por el contrario, debemos destacar un caso de disfunción eréctil, efecto adverso que no está registrado hasta el momento. Es el caso de un varón con micosis fungoide tumoral, que presenta disfunción eréctil claramente relacionada con el inicio del tratamiento, y que persiste a pesar de cambiar los agentes hipolipemiantes concomitantes al tratamiento.
DISCUSION
Ninguna de las múltiples opciones terapéuticas que existen para el tratamiento de los LCCT ha mostrado un aumento de la supervivencia global. La elección del tratamiento dependerá del estadio clínico y la extensión de la enfermedad; además tendremos que tener en cuenta otros factores como son la edad del paciente, su estado general, la disponibilidad de tratamiento y el grado de cumplimiento esperado para cada paciente. Los pacientes en estadios iniciales de la enfermedad generalmente presentan un curso crónico y benigno, por lo que son tratados con modalidades terapéuticas tópicas como corticoides, mecloretamina o carmustina, fototerapia (psoraleno y radiación ultravioleta A [PUVA] o radiación ultravioleta B [UVB] TL01) y radioterapia con emisión de electrones. Sin embargo, a partir de estadios tumorales el pronóstico empeora y son necesarios tratamientos sistémicos que controlen la enfermedad como el IFN, radioterapia convencional, quimioterapia o combinaciones de las previas. El bexaroteno está indicado a partir de estadios IB-IIA previo fracaso de otro tratamiento sistémico.
Los resultados obtenidos en dos ensayos multicéntricos 7,8 hicieron que la FDA aprobara el uso del bexaroteno en el tratamiento de los LCCT. El primero de ellos se llevó a cabo en 58 pacientes con estadios I-IIA y el segundo en 94 pacientes con estadios IIB-IVB, y la tasa global de respuesta fue del 54 y 45 %, respectivamente. Aunque nuestra experiencia está limitada a una pequeña serie de 9 pacientes, los resultados que hemos obtenido son similares a los descritos antes. Los efectos adversos más frecuentes que presentaron nuestros pacientes también se corresponden con los registrados, salvo un único caso de disfunción eréctil en uno de nuestros pacientes que constituye un hallazgo por el momento no descrito.
El bexaroteno constituye una modalidad terapéutica eficaz en todos los estadios de LCCT. Ofrece la ventaja de una administración cómoda por vía oral, no invasiva y en general se tolera muy bien. Los efectos adversos más frecuentes son analíticos y fácilmente tratables con agentes hipolipemiantes, terapia sustitutiva con hormona tiroidea y ajuste de dosis 9. Por otro lado, que no produzca inmunosupresión y de que sus efectos tóxicos se solapen mínimamente con los de otras opciones terapéuticas hacen que sea posible combinarlo con otros tratamientos, disminuyendo las dosis y, con ello, los posibles efectos adversos. De hecho, existen ya numerosos trabajos que describen combinaciones del bexaroteno con PUVA, IFN, fotoféresis y denileukin diftitox (Ontak®) 10-13. En el caso de este último, estudios in vitro han demostrado un efecto sinérgico del empleo conjunto de estos dos productos 14. Aunque no se ha demostrado que ningún tratamiento sea por si solo curativo en el LCCT, el tratamiento combinado puede actuar de manera sinérgica e inducir una remisión mantenida.