La urticaria crónica espontánea (UCE) es una enfermedad que puede tener repercusiones importantes en los pacientes y sus familiares1. Según estudios realizados en Francia y Alemania, el coste estimado derivado del tratamiento farmacológico por paciente se sitúa entre los 900 y 3000dólares/año1. La administración de antihistamínicos en dosis convencionales o superiores permite el control de la enfermedad en un 20-70% de los pacientes y ante el fracaso terapéutico, se puede emplear omalizumab y/o ciclosporina para aumentar el control de la enfermedad en un 30-40%2. Los instrumentos para definir el control de la enfermedad con estos tratamientos se basan en parámetros como la calidad de vida, la actividad de la enfermedad o el control percibido por el paciente. Aunque existe una correlación moderada entre las escalas disponibles (r=0,301-0,501)3,4, en algunos casos, las discrepancias en sus resultados podrían conducir a la toma de diferentes decisiones en cuanto al cambio de tratamiento farmacológico antihistamínico por omalizumab. Recientemente, la guía EAACI/GA2LEN/EuroGuiDerm/APAAACI5 recomienda como parámetro para la toma de decisiones farmacológicas el Urticaria Control Test (UCT), el cual se basa en la percepción del control de la enfermedad por parte del paciente durante el último mes. Esta guía sustituye su recomendación anterior de utilizar el Urticaria Activity Score (UAS7), basado en el registro de la actividad de la enfermedad durante la última semana, según la intensidad y frecuencia de los síntomas. El hecho de que estas dos herramientas definan el “control” con base en distintos parámetros, altera la toma de decisiones en cuanto a posibles cambios a realizar en el tratamiento. Estas decisiones pueden tener repercusiones importantes en el sistema sanitario, especialmente en términos económicos, pues implican la transición de un tratamiento relativamente barato y asequible (antihistamínicos) a uno de mayor coste (omalizumab), especialmente en países de renta media-baja.
En este estudio nos propusimos evaluar la frecuencia en la indicación de omalizumab según UAS7 o UCT. Además, evaluamos la frecuencia del control alcanzado con omalizumab según las diferentes escalas. Estos resultados explorarán el impacto de estos cambios desde una perspectiva de coste social.
Se seleccionaron pacientes con UCE que requirieron el uso de antihistamínicos en dosis máximas (un aumento de cuatro veces la dosis estándar), y se evaluó el grado de control según las escalas UAS7 y UCT. Los pacientes que no presentaban un control de la enfermedad (UAS7>6 puntos, UCT<12 puntos) tras al menos un mes de antihistamínicos, recibieron dosis de 300mg/mes de omalizumab y se sometieron a 6 meses de seguimiento.
Los pacientes fueron reclutados durante 2020-2021 para la cohorte URTICA en 3 centros diferentes de Colombia. Los pacientes eran mayores de 12 años, con diagnóstico de urticaria crónica según las guías internacionales5. Los criterios de exclusión fueron la presentación de enfermedades sistémicas potencialmente asociadas a la urticaria y el uso de esteroides sistémicos durante las últimas 3 semanas antes del reclutamiento o cualquier otra terapia que pudiera interferir con la evaluación de los síntomas. Se excluyeron los pacientes que presentaban angioedema exclusivamente. Este estudio fue aprobado por el Comité de Ética de la IPS Universitaria Clínicas y la Universidad de Antioquia (registro no. BE-IIM 200910 y no. IN13-2013, respectivamente). Todos los sujetos o su tutor legal (menores de 18 años) firmaron un consentimiento informado aprobando su participación voluntaria en el estudio.
Los análisis estadísticos se realizaron con SPSS versión 26.0 (SPSS Inc, Chicago, Ill) y PRISMA versión 9. Para los datos categóricos se informó el número total y la proporción. Se obtuvieron las tasas de frecuencia y sus IC del 95%. Se utilizó la prueba U de Mann-Whitney para la comparación de variables continuas al inicio del estudio y en pacientes con omalizumab después de seis meses. Las diferencias entre proporciones se analizaron mediante la prueba de chi-cuadrado de Pearson (o la prueba de McNemar, si procedía).
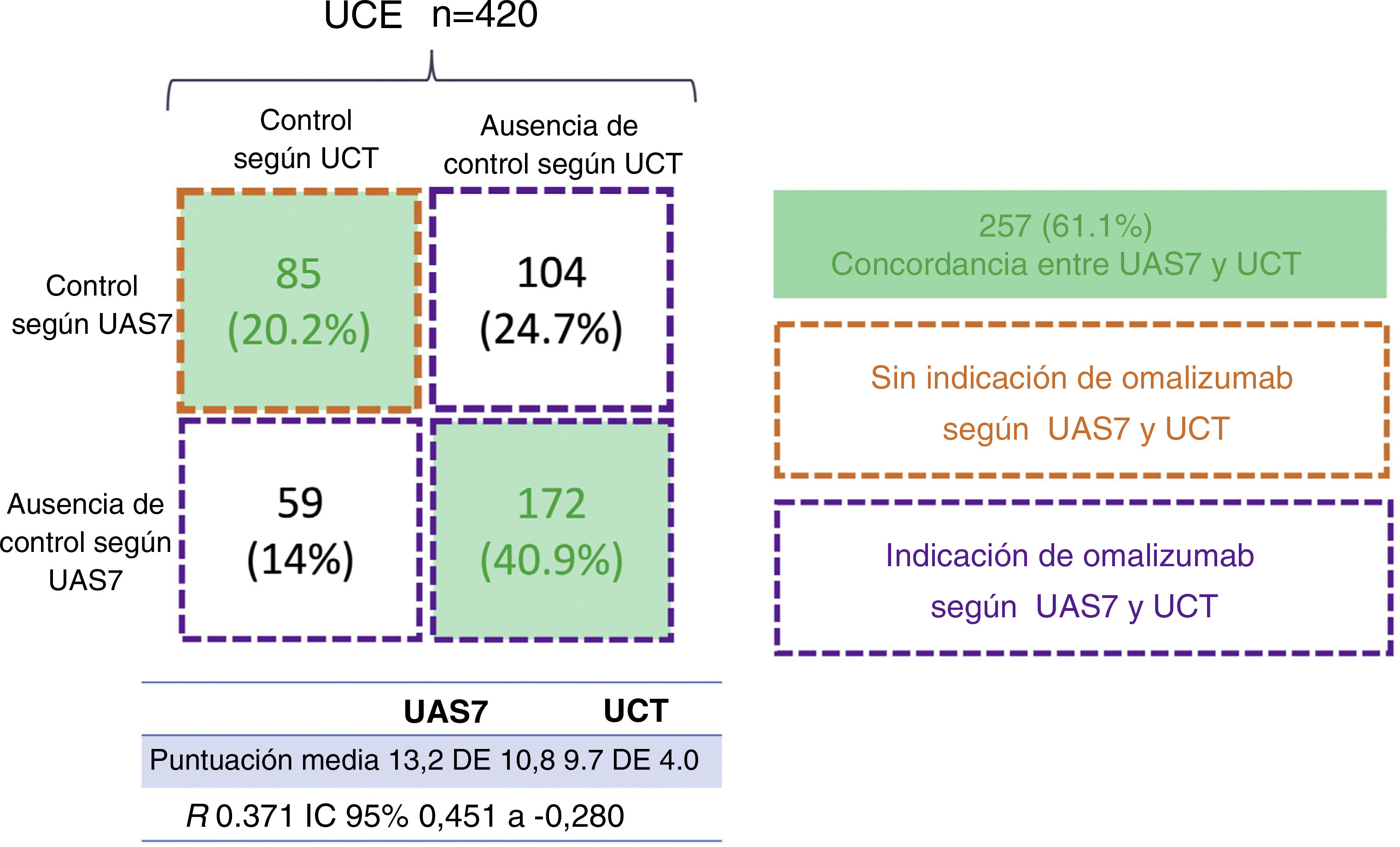
Cuatrocientos veinte pacientes fueron incluidos (edad media: 47 años, rango 16-68; n=300 (71,4%) mujeres). La media de las puntuaciones del UAS7 fue de 13,2 puntos (DE 10,8) y de 9,7 (DE 4) en el caso de UCT. Los puntos bajos y altos en UAS7 y UCT indican control, respectivamente; se observó una correlación inversa entre las dos escalas (r=−0.370; −0.280 a −0.451 IC 95%; p<0.001). Ambas coincidieron en la decisión de administrar omalizumab (20,2%) o no (40,9%) en 257 pacientes (61,1%). De manera significativa, se observó una mayor frecuencia en la necesidad de omalizumab según UCT que en el caso del UAS7 (276 (65,7%) frente a 231 (55%) (diferencia 10,7%, IC 95% 7,6-14,5%; p 0,01). El uso exclusivo de UCT para determinar el cambio a omalizumab genera un incremento en su indicación del 10,7%, lo que podría suponer un aumento significativo de los costes del tratamiento para el sistema sanitario. Por el contrario, el uso de las dos escalas podría reducir este coste y permitiría reservar la terapia a aquellos pacientes más interesados en recibirla.
Un total de 335 (79,7%) pacientes tenían indicación de omalizumab según UAS7 o UCT (fig. 1), pero 292 pacientes decidieron no recibir el tratamiento. Los motivos para no recibir omalizumab fueron: el/la paciente considera que no necesita omalizumab porque cree que sus síntomas están controlados (n=150, 51,3%), barreras logísticas (n=72, 24,6%), temores relacionados con el medicamento o la forma de aplicación (n=36, 12,3%), otros motivos (n=34, 11,6%). En Colombia, todos los pacientes pertenecientes al sistema general de salud que cubre al 98% de la población tienen acceso gratuito a omalizumab.
Control de la enfermedad en pacientes con UCE según UAS7 y UCT. El control de la enfermedad se definió según el punto de corte en la escala clinimétrica; UAS7 control<6 puntos; UCT control>12 puntos. Los dos recuadros verdes indican concordancia entre las dos escalas; el recuadro con una línea naranja muestra los pacientes que no tienen indicación de omalizumab y los tres recuadros con la línea morada muestran los pacientes con indicación de omalizumab según una o ambas escalas.
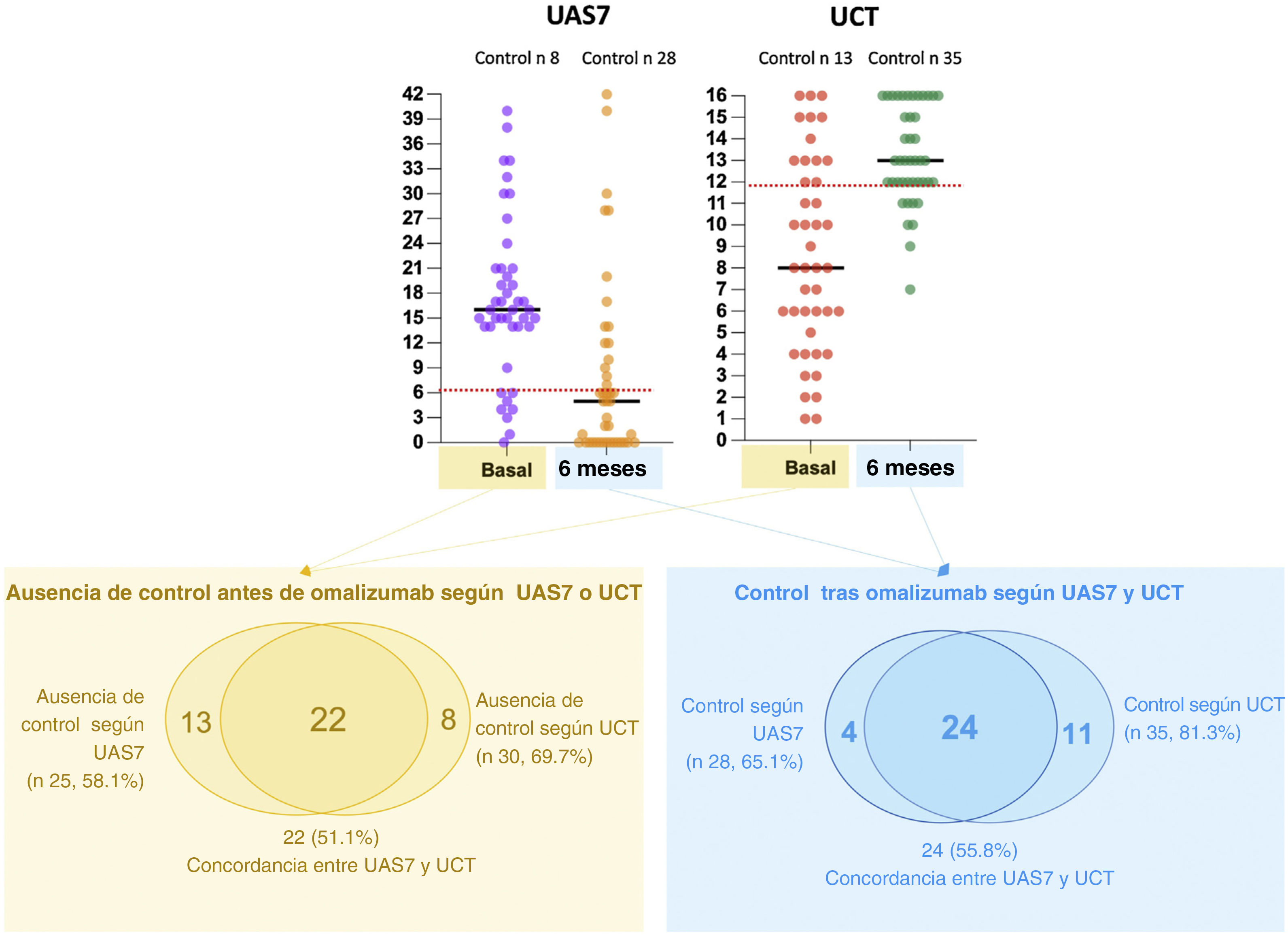
Cuarenta y tres pacientes aceptaron recibir omalizumab; las indicaciones correspondían a 35 según UAS7 y a 30 según UCT. Tras el inicio de omalizumab, 20 (46,5%) pacientes adicionales obtuvieron el control de la enfermedad según UAS7 y 22 (51,1%) según UCT. No hubo diferencias estadística ni clínicamente significativas en cuanto al beneficio neto del control obtenido utilizando cualquiera de las dos escalas para la evaluación del control clínico con omalizumab (20 frente a 22: diferencia neta 2 de 43 (4,6%), p 0,3) (fig. 2).
Las escalas clinimétricas son útiles durante el seguimiento de los pacientes y en la toma de decisiones sobre el tratamiento. Otros aspectos además de la actividad de la enfermedad (por ejemplo, la percepción de los pacientes) han cobrado relevancia a la hora de definir el control de la enfermedad y, recientemente, algunas directrices sugieren la sustitución de UAS7 por UCT en la toma de decisiones del tratamiento farmacológico en la urticaria5. En comparación con UAS7, un aspecto positivo de UCT es que esta escala valora la percepción del paciente sobre el impacto de la enfermedad en las actividades diarias. Además, UAS7 requiere una evaluación de 7 días, lo que suele dificultar su correcta realización.
Sin embargo, según nuestros resultados, este cambio podría tener un impacto en el sistema sanitario, pues la aplicación de UCT supone un aumento en la indicación de omalizumab, y por tanto, un mayor coste para el sistema sanitario. La evaluación del coste-beneficio de los tratamientos desempeña un papel importante en la toma de decisiones, especialmente en cuanto a la normativa del sistema sanitario. Un elevado número de pacientes de nuestro estudio prefirieron no utilizar omalizumab a pesar de que, según una de las escalas, no tenían controlada la enfermedad. En la mayoría de los pacientes que aceptaron utilizar omalizumab se observó la ausencia de control de los síntomas según las dos escalas UAS7 y UCT. Cada escala evalúa un aspecto específico, y nuestros resultados indican la necesidad de evaluar múltiples parámetros para reconocer mejor las preferencias de los pacientes antes de iniciar una nueva terapia. Esto podría resultar en la reducción de tratamientos innecesarios, lo que supondría un beneficio para el paciente y el sistema sanitario.
En conclusión, entre los pacientes con UCE que utilizan dosis elevadas de antihistamínicos, la escala UCT identifica un número más elevado de pacientes que requieren omalizumab que UAS7. El control de la enfermedad en estos pacientes requiere una evaluación realizada desde diferentes perspectivas para definir si el beneficio obtenido justifica el incremento del coste del nuevo tratamiento.
Conflicto de interesesLos autores declaran que no tienen conflictos de interés.