La rosácea es una enfermedad crónica que afecta negativamente a la calidad de vida y la salud mental de los pacientes. La escala Rosacea Quality of Life (RosaQoL) podría ser una herramienta útil para seguir a los pacientes durante el tratamiento de la rosácea, ya que mide el impacto en la calidad de vida y ayuda a adaptar el tratamiento a las necesidades del paciente. Es una escala validada, que se cumplimenta en pocos minutos.
Materiales y métodosSe realizó la traducción y retrotraducción de la escala original, por parte de dos traductores nativos, con el consejo de un comité de expertos cuando fue necesario. Esta versión fue testada en 21 pacientes para comprobar la correcta comprensión. Las características psicométricas y su validez se determinaron utilizando varias medidas (sensibilidad y especificidad mediante curva ROC y consistencia interna por alfa de Cronbach). La correlación entre escalas RosaQoL y SF-12 se realizó mediante coeficientes de correlación de Pearson.
ResultadosUn total de 531 participantes respondieron a la escala (481 con rosácea y 50 controles). La escala presentó una excelente sensibilidad y especificidad (curva ROC: 0,96; IC 95%: 0,92-0,99) y una elevada correlación interna (alfa de Cronbach: 0,96). La escala RosaQoL se correlacionó con la SF-12. Una mayor puntuación en la escala RosaQoL se asoció con una peor calidad de vida en todas las dimensiones de la escala SF-12.
ConclusionesLa versión española de la escala RosaQoL presenta características psicométricas similares a la escala original, y es útil para evaluar la calidad de vida en los pacientes con rosácea.
Rosacea is a chronic disease negatively impacting the patients’ quality of life and mental health. The Rosacea Quality of Life (RosaQoL) scale could be a useful tool to monitor patients while on therapy vs rosacea, as it measures the impact on quality of life and helps individualize treatment to meet the patients’ needs. RosaQoL is a validated scale that can be completed within a few minutes.
Materials and methodsThe original scale was translated and back translated by 2 native translators, with input from an expert committee when necessary. This version was tested on 21 patients to ensure proper understanding. Psychometric characteristics and validity were determined using various measures (sensitivity and specificity via ROC curve and internal consistency via Cronbach's alpha). The correlation between RosaQoL and SF-12 scales was assessed using Pearson correlation coefficients.
ResultsA total of 531 participants responded to the scale (481 with rosacea and 50 controls). The scale demonstrated excellent sensitivity and specificity (ROC curve, 0.96; 95%CI, 0.92-0.99) and high internal consistency (Cronbach's alpha, 0.96). RosaQoL correlated with SF-12. A higher score on the RosaQoL scale was associated with worse quality of life in all dimensions of the SF-12 scale.
ConclusionsThe Spanish version of the RosaQoL scale exhibits psychometric characteristics, which are similar to the original scale. Also, the RosaQoL scale is useful to assess the quality of life of patients with rosacea.
La rosácea es una enfermedad cutánea crónica que puede afectar también a los ojos. Suele presentarse en adultos de mediana y avanzada edad, con fototipo claro, especialmente en mujeres. Los síntomas incluyen enrojecimiento, pápulas y pústulas, y, en algunos pacientes, engrosamiento y fibrosis de la piel denominado fima1.
La rosácea afecta negativamente la calidad de vida y la salud mental de los pacientes debido a la presencia de eritema y lesiones faciales que alteran seriamente la autoimagen y la autoestima2,3.
Los instrumentos de medición de la calidad de vida relacionada con la salud (CVRS) buscan evaluar de manera objetiva cómo afecta una enfermedad a la vida del individuo. Estos cuestionarios ofrecen una visión del impacto de la enfermedad en la calidad de vida global o en áreas específicas (funcionalidad, emociones, etc.)4.
La medición de la CVRS puede hacerse de dos formas: mediante instrumentos genéricos, que evalúan la calidad de vida de forma global (p. ej.: cuestionario SF-125); y mediante instrumentos específicos, focalizados en problemas asociados con trastornos concretos, tipos de pacientes o áreas funcionales6,7 (p. ej.: el Dermatology Life Quality Index [DLQI]8 o el SKINDEX-299, ambos validados en castellano).
La escala SF-12, ampliamente utilizada en investigación, ha sido correlacionada con escalas específicas, como el DLQI en dermatitis atópica10. Sin embargo, estas escalas genéricas pueden no recoger adecuadamente el impacto de determinadas enfermedades como la rosácea. La escala Rosacea Quality of life (RosaQoL), específica de rosácea, está disponible en inglés y mide el impacto de sus síntomas sobre la calidad de vida, siendo más precisa que las escalas generalistas11. Disponer de una herramienta validada en español permitirá valorar el impacto en la calidad de vida del paciente, permitiendo una personalización efectiva del tratamiento4,5.
Los objetivos de este estudio son: 1) realizar el proceso de validación y adaptación transcultural al castellano de la escala RosaQol y 2) analizar la correlación de la escala RosaQol con la escala SF-12.
Materiales y métodosDiseño del estudioEl estudio, realizado entre agosto y diciembre de 2021 con la aprobación del Comité de Ética del Hospital Universitario Sagrat Cor de Barcelona, consistió en la traducción y adaptación transcultural de la escala RosaQol al español, siguiendo las 5 etapas indicadas en la literatura internacional12–14: 1) traducción directa del cuestionario original al español, por al menos dos traductores bilingües de forma independiente; 2) síntesis y resolución de posibles discrepancias en las traducciones; 3) traducción inversa al idioma original por al menos dos traductores independientes que desconocían la versión original; 4) revisión por un comité de expertos, formado por los tres coordinadores del estudio, reconocidos como Key Opinion Leaders en rosácea para asegurar equivalencia semántica, idiomática, cultural y conceptual; y 5) prueba piloto del cuestionario traducido, con 21 sujetos (7 controles sanos, 2 pacientes con rosácea y 12 pacientes con patologías dermatológicas variadas), similar a la población diana.
Para asegurar que el momento de la respuesta no influía en el resultado, se llevó a cabo un test-retest, en el que un grupo de 10 pacientes volvieron a responder a la escala en un plazo no superior a 1-2 días desde la visita inicial. Adicionalmente, y para analizar el grado de discriminación entre casos y controles, un grupo de 50 sujetos sin rosácea (controles) completó también la escala. Al finalizar esta fase se obtuvo una versión final del cuestionario RosaQol listo para su validación.
En una segunda fase, 481 pacientes cumplimentaron las escalas RosaQoL y SF-12 para validar el cuestionario.
Para evaluar la sensibilidad al cambio, 3 meses más tarde los mismos pacientes volvieron a responder ambas escalas.
PacientesEl proceso de validación transcultural al idioma español se llevó a cabo en 531 participantes mayores de edad que acudieron a 17 consultas de dermatología en España. La muestra constaba de 481 participantes con diferentes grados de gravedad de rosácea según la escala Investigator Global Assessment (IGA)15 (casos) y de 50 participantes sanos (controles).
Cuestionario RosaQoLEl cuestionario RosaQoL se encuentra disponible en inglés y mide el impacto del trastorno y sus síntomas sobre la calidad de vida, siendo una escala más precisa que las generalistas, ya que es una escala específica de calidad de vida de rosácea11.
Se trata de una herramienta autoadministrada que se desarrolló a partir del cuestionario SKINDEX-29 y se compone de 21 ítems repartidos en 3 dimensiones o dominios: síntomas (7 ítems), funcionalidad (3 ítems) y estado emocional (11 ítems). Cada ítem tiene una escala de respuesta con 5 posibles opciones, siendo 0: nunca; 1: raramente; 2: a veces; 3; a menudo; y 4: siempre11.
Cuestionario SF-12El cuestionario de salud SF-12 se encuentra disponible en castellano y mide 8 aspectos de la CVRS16,17.
La escala SF-12 es una herramienta autoadministrada que se desarrolló a partir de la escala SF-36 y se compone de 12 ítems repartidos en 8 dimensiones o dominios: función física (2 ítems), rol físico (2 ítems), dolor corporal (1 ítem), salud general (1 ítem), vitalidad (1 ítem), rol emocional (2 ítems), función social (1 ítem) y salud mental (2 ítems)16.
Escala IGALa escala IGA es una escala ordinal con 5 categorías que evalúan la gravedad de las lesiones. La clasificación tiene un rango desde 0 (no hay lesiones inflamatorias presentes ni eritema) hasta 4 (eritema intenso y/o numerosas pápulas y pústulas)15.
Análisis estadísticoEl análisis de los datos se llevó a cabo utilizando el paquete estadístico SAS System versión 9.4 (SAS Institute Inc., Carey, Carolina del Norte, EE.UU.).
Se considerará que el cuestionario es discriminativo cuanto más se aproxime el área bajo la curva ROC (Receiver Operating Characteristic) al valor de 1,0018. La sensibilidad y especificidad del cuestionario se evaluaron utilizando el criterio de Youden19, y la fiabilidad de la consistencia interna del cuestionario se midió mediante el coeficiente alfa de Cronbach20. Siguiendo el criterio recomendado por George y Mallery21, un coeficiente alfa de Cronbach ≥0,90 indica una excelente consistencia interna. Para evaluar la fiabilidad del test-retest se empleó el método propuesto por Bland y Altman22 y el coeficiente de correlación intraclase propuesto por Shrout y Fleiss23. Un coeficiente de correlación intraclase superior a 0,90 indica una elevada fiabilidad del cuestionario24. El análisis de la convergencia entre la escala RosaQoL y la escala más generalista SF-12 se obtuvo mediante una correlación de Pearson, donde se estimó que resultados entre 0,4 y 0,7 se consideraban satisfactorios25.
ResultadosSe facilitó el cuestionario RosaQoL traducido (tabla 1) a 531 participantes con una edad media de 47 años (DE: 13,4 [IC 95%: 45,8-48,1]), de los cuales el 71% (n=369) eran mujeres, y el 29% (n=151) eran hombres. Entre los que padecían rosácea, el tipo papulopustulosa era el más habitual, representado con un 65,9% de los casos.
Ítems del cuestionario RosaQoL
| ¿Con qué frecuencia se ha sentido identificado con estas frases durante las últimas 4 semanas? | |
|---|---|
| 1 | Me preocupa que mi rosácea pueda ser grave |
| 2 | Mi rosácea me quema o me pica |
| 3 | Me preocupa tener cicatrices a causa de mi rosácea |
| 4 | Me preocupa que mi rosácea pueda empeorar |
| 5 | Me preocupan los efectos secundarios de los medicamentos para la rosácea |
| 6 | Mi rosácea está irritada |
| 7 | Mi rosácea me avergüenza |
| 8 | Estoy frustrado/a por mi rosácea |
| 9 | Mi rosácea hace que mi piel sea sensible |
| 10 | Estoy molesto/a por mi rosácea |
| 11 | Me molesta el aspecto de mi piel (enrojecimiento, manchas) |
| 12 | Mi rosácea me hace sentir cohibido |
| 13 | Trato de tapar mi rosácea (con maquillaje) |
| 14 | Me molesta la persistencia/recurrencia de mi rosácea |
| 15 | Evito ciertas comidas y bebidas a causa de mi rosácea |
| 16 | Mi piel parece que tenga bultos (desigual, no suave, irregular) |
| 17 | Mi piel se enrojece |
| 18 | Mi piel se irrita fácilmente (cosméticos, lociones para después del afeitado, desmaquillantes) |
| 19 | Mis ojos me molestan (los siento secos o con arenilla) |
| 20 | Pienso en mi rosácea |
| 21 | Evito ciertos ambientes (calor, humedad, frío) debido a mi rosácea |
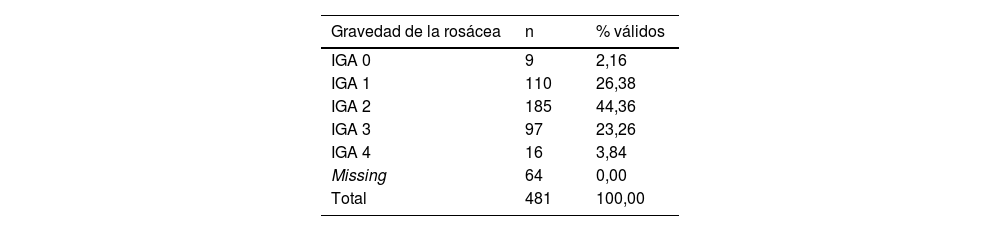
Según la escala IGA, el grado IGA 2 era el más común, con un 44,4% de los casos (tabla 2).
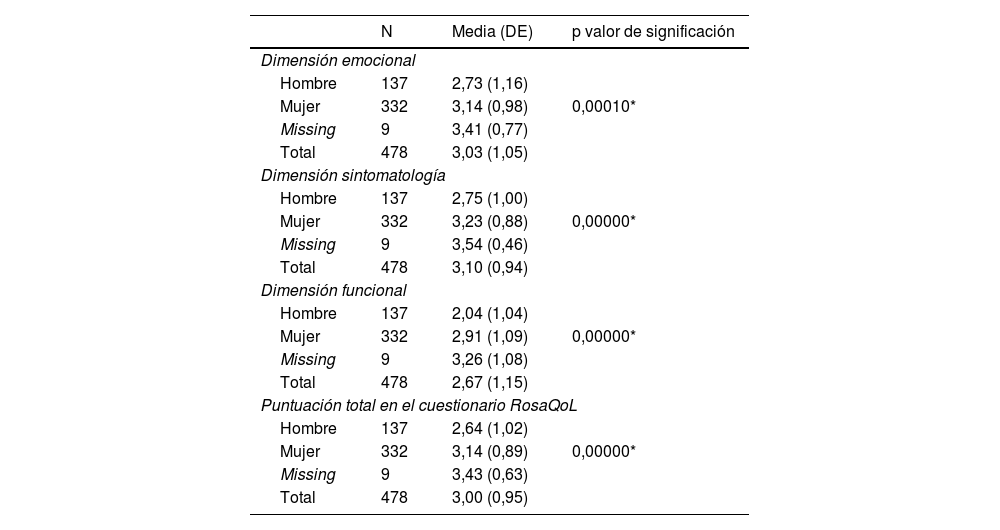
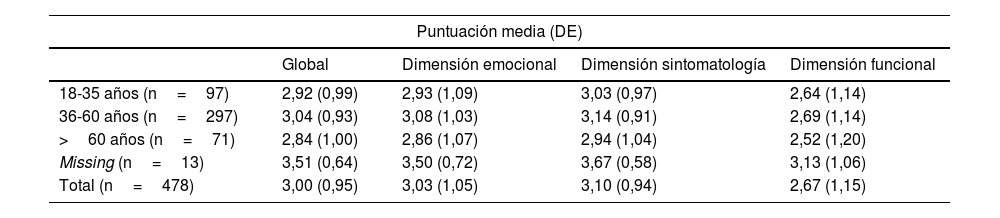
Se observaron diferencias estadísticamente significativas entre hombres y mujeres en la puntuación global del cuestionario RosaQoL y en cada una de las 3 dimensiones de la escala (síntomas, funcionalidad y estado emocional; p<0,001) (tabla 3), aunque estas diferencias no fueron significativas cuando se analizó en función de la edad (tabla 4).
Diferencias en las puntuaciones en el cuestionario RosaQoL en la visita inicial por sexos
| N | Media (DE) | p valor de significación | |
|---|---|---|---|
| Dimensión emocional | |||
| Hombre | 137 | 2,73 (1,16) | |
| Mujer | 332 | 3,14 (0,98) | 0,00010* |
| Missing | 9 | 3,41 (0,77) | |
| Total | 478 | 3,03 (1,05) | |
| Dimensión sintomatología | |||
| Hombre | 137 | 2,75 (1,00) | |
| Mujer | 332 | 3,23 (0,88) | 0,00000* |
| Missing | 9 | 3,54 (0,46) | |
| Total | 478 | 3,10 (0,94) | |
| Dimensión funcional | |||
| Hombre | 137 | 2,04 (1,04) | |
| Mujer | 332 | 2,91 (1,09) | 0,00000* |
| Missing | 9 | 3,26 (1,08) | |
| Total | 478 | 2,67 (1,15) | |
| Puntuación total en el cuestionario RosaQoL | |||
| Hombre | 137 | 2,64 (1,02) | |
| Mujer | 332 | 3,14 (0,89) | 0,00000* |
| Missing | 9 | 3,43 (0,63) | |
| Total | 478 | 3,00 (0,95) | |
Resultado de la puntuación en el cuestionario de RosaQoL por grupos de edad (solamente casos)
| Puntuación media (DE) | ||||
|---|---|---|---|---|
| Global | Dimensión emocional | Dimensión sintomatología | Dimensión funcional | |
| 18-35 años (n=97) | 2,92 (0,99) | 2,93 (1,09) | 3,03 (0,97) | 2,64 (1,14) |
| 36-60 años (n=297) | 3,04 (0,93) | 3,08 (1,03) | 3,14 (0,91) | 2,69 (1,14) |
| >60 años (n=71) | 2,84 (1,00) | 2,86 (1,07) | 2,94 (1,04) | 2,52 (1,20) |
| Missing (n=13) | 3,51 (0,64) | 3,50 (0,72) | 3,67 (0,58) | 3,13 (1,06) |
| Total (n=478) | 3,00 (0,95) | 3,03 (1,05) | 3,10 (0,94) | 2,67 (1,15) |
p no significativa para todos los grupos de edad.
No se encontraron diferencias significativas en la puntuación de RosaQoL entre el grupo control (pacientes sanos [n=50], puntuación media global 43,5 [DE 13,7]) y el grupo de pacientes ([n=468], puntuación media global 47,3 [DE 13,3]; p=0,052).
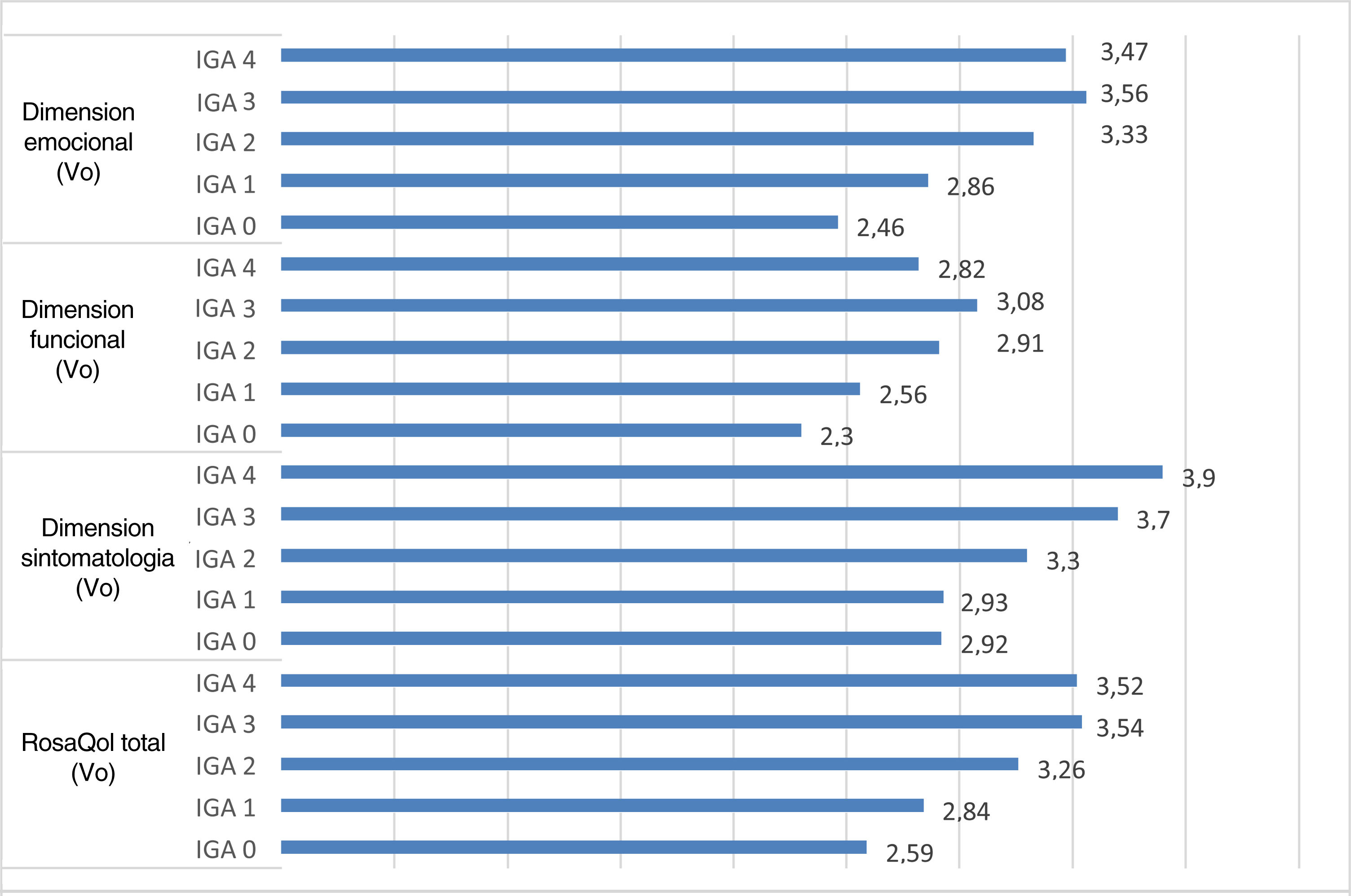
Se observa, asimismo, que la puntuación obtenida en RosaQoL es mayor en grados más severos de rosácea, y mayor es el impacto observado en la dimensión de sintomatología (fig. 1).
El método de consistencia interna, basado en el alfa de Cronbach, permite estimar la fiabilidad de un instrumento de medida a través de un conjunto de ítems que se espera que midan el mismo constructo o dimensión teórica. El valor alfa de Cronbach valorado sobre el total de cuestionarios fue de 0,96, en consonancia con el criterio general recomendado por George y Mallery21, según el cual valores de 0,9 o superiores indican una elevada consistencia interna.
Al eliminar cada uno de los ítems de forma individual de la escala, no se obtuvo una mejoría en el alfa de Cronbach, por tanto, se establece que ningún ítem es susceptible de ser eliminado. El poder del cuestionario para discriminar casos mediante la curva ROC permitió obtener un área bajo la curva (AUC) de 0,96 (IC 95%: 0,92-0,99). Considerando que valores superiores a 0,9 indican un alto poder discriminativo, puede afirmarse que el cuestionario tiene una alta capacidad para detectar casos.
La evaluación de la sensibilidad y especificidad mediante el criterio de Youden permitió obtener un punto de corte en la puntuación de RosaQoL >1,476, lo cual proporciona al cuestionario una elevada sensibilidad, con un valor de 0,99, y una especificidad para detectar casos de 0,85. Para este punto de corte se obtuvieron 425 verdaderos positivos, 43 verdaderos negativos, 7 falsos positivos y 3 falsos negativos.
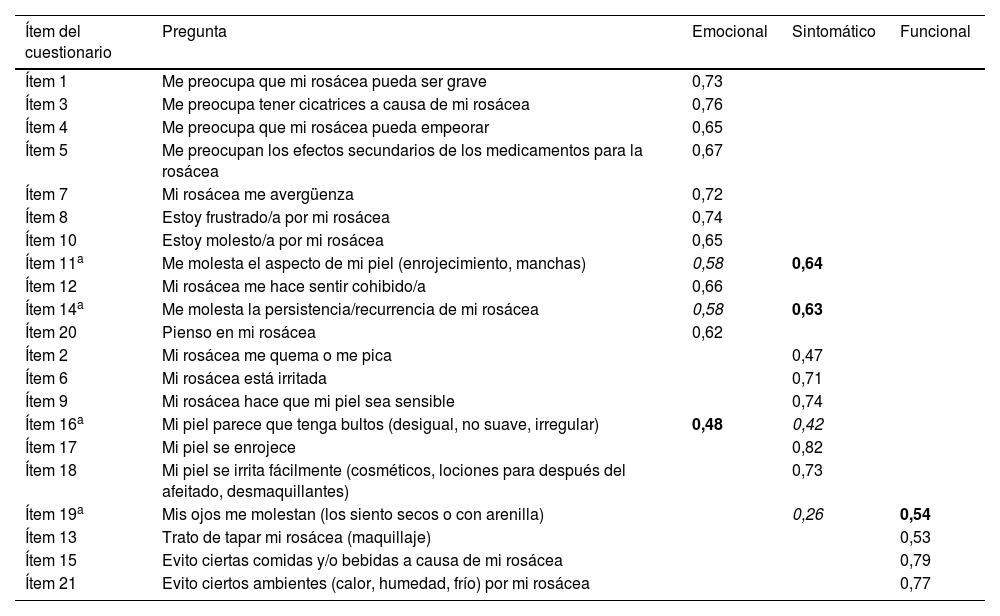
La matriz de componentes rotados Varimax para 3 factores contribuye en la validación del constructo de la escala, mostrando que los ítems tienden a agruparse en los factores funcional, emocional y sintomático propuestos en la escala original26 (tabla 5).
Matriz de componentes rotados del modelo factorial Varimax del cuestionario RosaQoL (solamente casos)
| Ítem del cuestionario | Pregunta | Emocional | Sintomático | Funcional |
|---|---|---|---|---|
| Ítem 1 | Me preocupa que mi rosácea pueda ser grave | 0,73 | ||
| Ítem 3 | Me preocupa tener cicatrices a causa de mi rosácea | 0,76 | ||
| Ítem 4 | Me preocupa que mi rosácea pueda empeorar | 0,65 | ||
| Ítem 5 | Me preocupan los efectos secundarios de los medicamentos para la rosácea | 0,67 | ||
| Ítem 7 | Mi rosácea me avergüenza | 0,72 | ||
| Ítem 8 | Estoy frustrado/a por mi rosácea | 0,74 | ||
| Ítem 10 | Estoy molesto/a por mi rosácea | 0,65 | ||
| Ítem 11a | Me molesta el aspecto de mi piel (enrojecimiento, manchas) | 0,58 | 0,64 | |
| Ítem 12 | Mi rosácea me hace sentir cohibido/a | 0,66 | ||
| Ítem 14a | Me molesta la persistencia/recurrencia de mi rosácea | 0,58 | 0,63 | |
| Ítem 20 | Pienso en mi rosácea | 0,62 | ||
| Ítem 2 | Mi rosácea me quema o me pica | 0,47 | ||
| Ítem 6 | Mi rosácea está irritada | 0,71 | ||
| Ítem 9 | Mi rosácea hace que mi piel sea sensible | 0,74 | ||
| Ítem 16a | Mi piel parece que tenga bultos (desigual, no suave, irregular) | 0,48 | 0,42 | |
| Ítem 17 | Mi piel se enrojece | 0,82 | ||
| Ítem 18 | Mi piel se irrita fácilmente (cosméticos, lociones para después del afeitado, desmaquillantes) | 0,73 | ||
| Ítem 19a | Mis ojos me molestan (los siento secos o con arenilla) | 0,26 | 0,54 | |
| Ítem 13 | Trato de tapar mi rosácea (maquillaje) | 0,53 | ||
| Ítem 15 | Evito ciertas comidas y/o bebidas a causa de mi rosácea | 0,79 | ||
| Ítem 21 | Evito ciertos ambientes (calor, humedad, frío) por mi rosácea | 0,77 |
Se marca en negrita el resultado del análisis factorial en la dimensión donde queda clasificada en la escala española.
Se marca en cursiva el resultado del análisis factorial en la dimensión que ocupaba en la escala original.
Todos los ítems del cuestionario aparecen clasificados como en el cuestionario original, salvo ligeras discrepancias en 4 de ellos. Los ítems 11 «Me molesta el aspecto de mi piel (enrojecimiento, manchas)» y 14 «Me molesta la persistencia/recurrencia de mi rosácea», que en la escala original aparecen agrupados en la dimensión emocional, parecen tener un poco más de peso en la dimensión sintomática en la versión española. Respecto al ítem 16 «Mi piel parece que tenga bultos (desigual, no suave, irregular)», pese a que debería estar representado en la dimensión sintomática, se encuentra ligeramente mejor representado en la emocional. Por último, el ítem 19 «Mis ojos me molestan (los siento secos o con arenilla)», debería estar mejor representado en la dimensión sintomática, pero se encontró mejor representado en la dimensión funcional. Dado que la diferencia de pesos de estos 4 ítems era mínima, se decidió mantener la clasificación original de las dimensiones a efectos de la valoración comparativa con otras versiones de la escala.
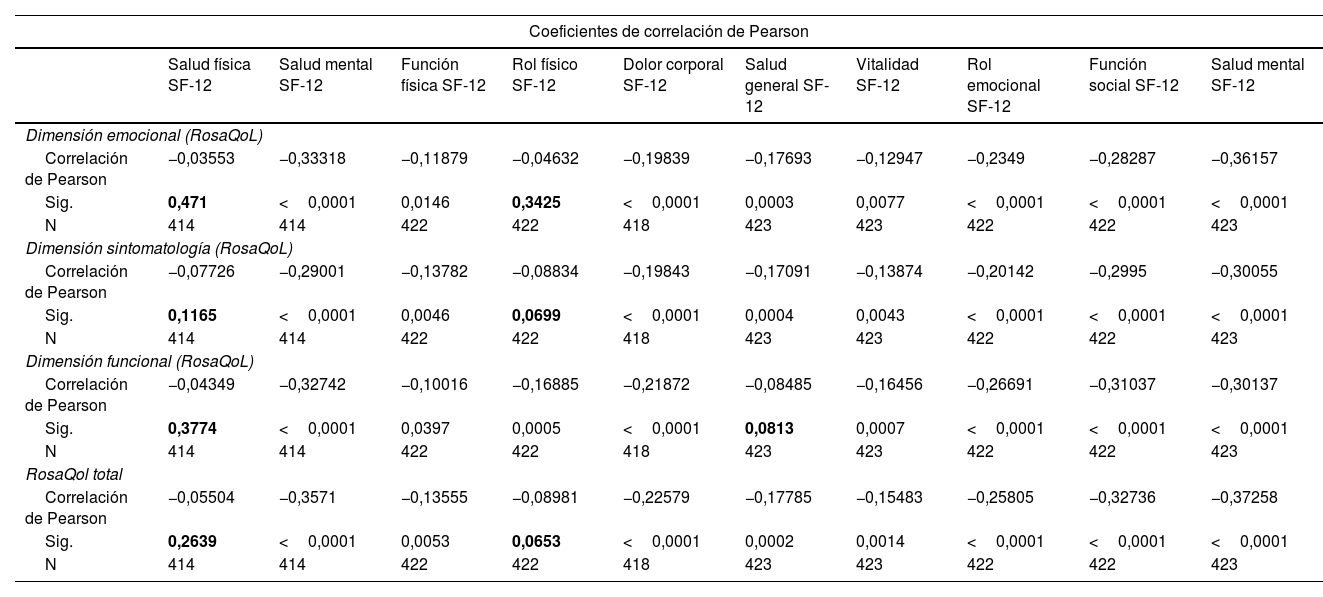
Cuando se analizó la correlación entre la escala RosaQoL y la escala más generalista, la escala SF-12, la mayoría de las correlaciones estudiadas fueron estadísticamente significativas y en su totalidad negativas. Una mayor puntuación en la escala RosaQoL en cualquiera de las dimensiones (funcional, emocional y sintomática) se asocia a una peor calidad de vida en todas las dimensiones de la escala SF-12 (tabla 6).
Correlación de las escalas RosaQoL y SF-12
| Coeficientes de correlación de Pearson | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Salud física SF-12 | Salud mental SF-12 | Función física SF-12 | Rol físico SF-12 | Dolor corporal SF-12 | Salud general SF-12 | Vitalidad SF-12 | Rol emocional SF-12 | Función social SF-12 | Salud mental SF-12 | |
| Dimensión emocional (RosaQoL) | ||||||||||
| Correlación de Pearson | −0,03553 | −0,33318 | −0,11879 | −0,04632 | −0,19839 | −0,17693 | −0,12947 | −0,2349 | −0,28287 | −0,36157 |
| Sig. | 0,471 | <0,0001 | 0,0146 | 0,3425 | <0,0001 | 0,0003 | 0,0077 | <0,0001 | <0,0001 | <0,0001 |
| N | 414 | 414 | 422 | 422 | 418 | 423 | 423 | 422 | 422 | 423 |
| Dimensión sintomatología (RosaQoL) | ||||||||||
| Correlación de Pearson | −0,07726 | −0,29001 | −0,13782 | −0,08834 | −0,19843 | −0,17091 | −0,13874 | −0,20142 | −0,2995 | −0,30055 |
| Sig. | 0,1165 | <0,0001 | 0,0046 | 0,0699 | <0,0001 | 0,0004 | 0,0043 | <0,0001 | <0,0001 | <0,0001 |
| N | 414 | 414 | 422 | 422 | 418 | 423 | 423 | 422 | 422 | 423 |
| Dimensión funcional (RosaQoL) | ||||||||||
| Correlación de Pearson | −0,04349 | −0,32742 | −0,10016 | −0,16885 | −0,21872 | −0,08485 | −0,16456 | −0,26691 | −0,31037 | −0,30137 |
| Sig. | 0,3774 | <0,0001 | 0,0397 | 0,0005 | <0,0001 | 0,0813 | 0,0007 | <0,0001 | <0,0001 | <0,0001 |
| N | 414 | 414 | 422 | 422 | 418 | 423 | 423 | 422 | 422 | 423 |
| RosaQol total | ||||||||||
| Correlación de Pearson | −0,05504 | −0,3571 | −0,13555 | −0,08981 | −0,22579 | −0,17785 | −0,15483 | −0,25805 | −0,32736 | −0,37258 |
| Sig. | 0,2639 | <0,0001 | 0,0053 | 0,0653 | <0,0001 | 0,0002 | 0,0014 | <0,0001 | <0,0001 | <0,0001 |
| N | 414 | 414 | 422 | 422 | 418 | 423 | 423 | 422 | 422 | 423 |
Se marcan en negrita las correlaciones estadísticamente no significativas.
La fiabilidad temporal del cuestionario se confirmó a través de la prueba test-retest al no detectarse discrepancias en el tiempo entre las respuestas de los pacientes.
Con el fin de evaluar la sensibilidad al cambio, se realizó una nueva visita a los 3 meses del inicio del estudio, donde se pidió a los pacientes de rosácea que volvieran a cumplimentar tanto el cuestionario RosaQoL como el SF-12. En una gran mayoría de las correlaciones calculadas, se observó una relación negativa estadísticamente significativa. A mayor incremento en la escala RosaQoL y en todas las dimensiones (funcional, emocional y sintomática), se observó una peor evolución de la calidad de vida en todas las dimensiones de la escala SF-12. Esta misma correlación también se observó cuando se analizaba por grupo de edad y por gravedad de la enfermedad.
DiscusiónPara considerar una escala válida como instrumento para medir la CVRS, no es suficiente una simple traducción, sino que son necesarios una serie de pasos pautados y estructurados13. Para comprobar que se cumplen los requisitos de fiabilidad y validez de este tipo de herramientas, es necesaria la evaluación de las propiedades de medida de la versión traducida en una población de características similares y después someterla a un proceso de validación25.
Se demuestra mediante el estudio de las propiedades de medida, que la versión traducida al español y culturalmente adaptada del cuestionario RosaQoL permite, al igual que la versión original, obtener diferencias estadísticamente significativas entre la población sana y la población con rosácea. El nivel de afectación en la escala RosaQoL en todas las dimensiones fue directamente proporcional a la gravedad de la rosácea, y el mayor grado de afectación se obtuvo en la dimensión de sintomatología.
Nicholson et al.11 pusieron en evidencia la validez de RosaQoL para discriminar a los pacientes con rosácea en comparación con SKINDEX-29. El instrumento específico RosaQoL, en su versión original, presentaba un mayor grado de respuesta a los 4-6 meses que SKINDEX-29 para la puntuación total, en aquellos pacientes que reportaban mejoría de su rosácea, mostrando una mayor especificidad.
El estudio de la fiabilidad del cuestionario RosaQoL demuestra que la herramienta posee un alto grado de consistencia interna, al obtenerse un valor alfa de Cronbach de 0,96, y que su poder discriminativo para detectar casos es extremadamente alto, al obtenerse un AUC en la curva ROC de 0,96.
La reproducibilidad es uno de los puntos importantes a tener en cuenta en la valoración de una herramienta para medir la CVRS. Para valorar la reproducibilidad, se comprueba si pueden obtenerse puntuaciones similares cuando se aplica en dos momentos distintos a la misma población por parte de los mismos evaluadores y utilizando el mismo método. Es importante evitar que se produzca el «efecto aprendizaje», por eso, el tiempo que transcurre entre el test inicial y el retest no debe ser muy largo27. En nuestro estudio, la puntación obtenida con el cuestionario RosaQoL no varía significativamente entre el resultado del test y retest del mismo paciente (intervalo de 1 a 2 días). Nuestros resultados del test-retest evidencian una correlación muy alta entre ambos test en las 3 dimensiones del cuestionario, lo que indica un elevado grado de fiabilidad.
El estudio de la validez de constructo mediante el análisis factorial mostró que los ítems de la escala RosaQoL tienden a agruparse según las dimensiones funcional, emocional y sintomática, al igual que en la versión original de la escala, y que los ítems que conforman cada una de ellas tienden a agruparse de forma consistente en cada dimensión.
En nuestro estudio también se analizó la convergencia («correlación») entre la escala RosaQoL y la escala más generalista SF-12 y se obtuvo que esta era positiva, evidenciando que las escalas son conceptualmente congruentes o similares25: a mayor incremento en la escala RosaQol y en todas las subdimensiones (funcional, emocional y sintomática), se detectó una peor evolución de la calidad de vida en todas las dimensiones de la escala SF-12.
ConclusionesLa escala RosaQoL, adaptada al español, ha demostrado ser una herramienta válida, sensible y fiable para medir la calidad de vida, en todas sus dimensiones (síntomas, funcionalidad y estado emocional), en la población española con rosácea. Los resultados indican que cuanto mayor es la gravedad de la rosácea, mayor es la afectación de la calidad de vida, siendo las dimensiones de sintomatología y la emocional las más afectadas, especialmente en mujeres.
Conflicto de interesesEste proyecto ha recibido financiación y soporte por parte de Laboratorios Galderma S.A.U. Los doctores Salleras y Pozo declaran no tener ningún conflicto de intereses. Por su parte, el doctor Ribera ha recibido ayudas y pagos relacionados con investigación, asesoría y formación de las siguientes compañías: AbbVie, Almirall, Amgen, Boehringer Ingelheim, Bristol Myers Squibb, Galderma, Gebro Pharma, Janssen, LEO Pharma, Eli Lilly, Novartis, Pfizer, Pierre-Fabre, Sandoz, SKB y UCB.
Agradecemos a todos los participantes del grupo su colaboración para la realización de este manuscrito, a Laboratorios Galderma S.A.U., por la financiación del proyecto y a la CRO Crossdata, por su asesoramiento en la realización del proyecto y la redacción de este artículo.