Los inhibidores de puntos de control inmunitario (ICI) pueden producir toxicidades cutáneas inmunomediadas entre las que se encuentran las reacciones sarcoideas. Nuestro objetivo fue analizar retrospectivamente los datos clínicos e histológicos de los pacientes en tratamiento con ICI que desarrollaron reacciones sarcoideas cutáneas entre 2019 y 2022. Se incluyeron siete pacientes (seis mujeres y un varón, con una edad mediana de 65años). La mediana de tiempo de instauración de la clínica fue de 4meses y la forma de presentación más frecuente fue la sarcoidosis papulosa de las rodillas, seguida de la sarcoidosis subcutánea. En todos se confirmó el diagnóstico histológicamente y no se observaron diferencias respecto a la sarcoidosis idiopática. Solo en dos casos fue preciso retirar la inmunoterapia. Las reacciones sarcoideas por ICI suelen ser leves y no suelen requerir la interrupción del tratamiento. Es fundamental obtener una confirmación histológica para distinguirlas de la progresión tumoral.
Immune checkpoint inhibitors (ICIs) can cause immune-mediated cutaneous adverse events, including sarcoid-like reactions. The aim of this study was to retrospectively analyze clinical and histologic data from patients who developed cutaneous sarcoid-like reactions between 2019 and 2022 while under treatment with ICIs. We studied 7 patients (6 women and 1 man) with a median age of 65years. Median time to onset of symptoms was 4months. The most common presentation was papular sarcoidosis of the knees followed by subcutaneous sarcoidosis. Diagnosis was confirmed histologically in all cases, and no differences were observed relative to idiopathic sarcoidosis. Discontinuation of ICI therapy was required in just two patients. ICI-induced sarcoid-like reactions tend to be mild and generally do not require treatment discontinuation. Histologic confirmation is essential for distinguishing these reactions from tumor progression.
Los inhibidores de puntos de control inmunitario (ICI) son cada vez más utilizados en el tratamiento de distintas neoplasias malignas. Su mecanismo de acción favorece la aparición de un nuevo espectro de toxicidades conocidas como «acontecimientos adversos relacionados con la inmunidad», entre los que se encuentran las reacciones sarcoideas1.
El objetivo de este trabajo fue estudiar las características clínicas e histológicas de las lesiones cutáneas compatibles con reacciones sarcoideas relacionadas con ICI en nuestro hospital y valorar si había diferencias respecto a las lesiones de sarcoidosis idiopática.
Material y métodosSe estudiaron retrospectivamente los casos de reacciones sarcoideas por ICI diagnosticados entre enero de 2019 y septiembre de 2022, e identificados a partir del registro iconográfico del Servicio de Dermatología del Hospital Universitario de Bellvitge (Barcelona). Se trata de un hospital universitario que proporciona asistencia terciaria a una población de aproximadamente 1millón de personas. Se recogieron datos demográficos (edad, sexo, neoplasia de base, inmunoterapia recibida, antecedentes de enfermedades autoinmunes), clínicos (tipo de lesiones cutáneas y localización, afectación extracutánea, gravedad del cuadro y necesidad de tratamiento específico y/o de suspensión del ICI), analíticos (función renal y valores de enzima convertidora de angiotensina, calcemia y enzimas hepáticas) e histológicos (tipo y localización de los granulomas, presencia de cuerpos extraños, de corona de linfocitos, de necrosis o de fibrosis, cambios epidérmicos), y se llevó a cabo un estudio descriptivo.
ResultadosSe identificaron 7 pacientes (6 mujeres y 1 varón), con una edad mediana de 65años (rango: 44-74). Ninguno tenía antecedentes de enfermedades autoinmunes antes de iniciar la inmunoterapia.
Seis pacientes recibieron inmunoterapia en monoterapia (3 un fármaco anti-PD1, y otros 3, uno anti-PDL1) y uno recibió la combinación de un anti-PDL1 con un anti-CTLA-4. Entre las neoplasias de base la más frecuente fue el melanoma (3pacientes), seguida del carcinoma de endometrio (2), de tiroides (1) y de pulmón (1).
La mediana de tiempo desde el inicio del tratamiento hasta el diagnóstico de la sarcoidosis fue de 4meses (rango: 2-9) y la forma de presentación cutánea más frecuente fue la sarcoidosis papulosa de las rodillas, que estuvo presente en 5 de los 7 pacientes. Tres pacientes presentaron nódulos subcutáneos, uno placas infiltradas en la frente y en la zona alta de la espalda y, por último, una paciente presentó infiltración por granulomas de xantelasmas preexistentes (caso publicado en la literatura)2.
A nivel extracutáneo, los órganos más afectados por orden de frecuencia fueron los ganglios hiliares y mediastínicos (4pacientes), el pulmón (3pacientes, en forma de múltiples nódulos pulmonares de pequeño tamaño), las articulaciones2, y un paciente tuvo una nefritis túbulo-intersticial granulomatosa aguda. Ningún paciente presentó afectación ocular, cardíaca, hepática o del sistema nervioso central.
En todos los pacientes se realizó una biopsia cutánea para confirmar histológicamente el diagnóstico, así como biopsias de los demás órganos afectados. En todos los pacientes se descartó progresión de su neoplasia, así como infección por hongos y micobacterias, a través de tinciones y de cultivos de los tejidos.
Se revisaron las biopsias cutáneas de todos los pacientes, observando granulomas formados por agregados de histiocitos epitelioides con escaso componente linfocítico. En los pacientes con sarcoidosis papulosa de las rodillas los granulomas estaban localizados predominantemente en la dermis superficial y era frecuente observar la presencia de cuerpos extraños (se hallaron en 3 de los 4pacientes biopsiados). En cambio, en los pacientes con sarcoidosis subcutánea los granulomas estaban prácticamente limitados al tejido celular subcutáneo, rodeados de una mayor cantidad de linfocitos, y se observaba presencia de fibrosis en 2 de los 3pacientes (tabla 1 y fig. 1). Desde un punto de vista histológico no se observaron diferencias respecto a la sarcoidosis idiopática.
Información histológica recogida de las biopsias cutáneas de los 7 pacientes estudiados
| Localización biopsia | Tipo granuloma | Localización granulomas | Cuerpo extraño | Corona linfocitos | Necrosis central | Epidermis | Dermatitis interfase | Eosinófilos | Fibrosis | |
|---|---|---|---|---|---|---|---|---|---|---|
| 1 | Antebrazo | Sarcoideo | Subcutáneos | − | ++ | − | Normal | − | − | Sí |
| 2 | Rodilla | Sarcoideo | Dermis sup | Sí | − | − | Normal | − | − | − |
| 3 | Espalda | Sarcoideo | Dermis sup | − | − | − | Normal | − | − | − |
| 4 | Antebrazo | Sarcoideo | Subcutáneos | − | ++ | Sí | Normal | − | − | Sí |
| Rodilla | Sarcoideo | Dermis sup+retic | − | - | Sí | Normal | − | − | − | |
| 5 | Rodilla | Sarcoideo | Dermis sup | Sí | + | − | Hiperqueratosis focal | − | − | − |
| 6 | Dedo mano | Sarcoideo | Subcutáneos | − | + | − | Normal | − | − | − |
| 7 | Párpado | Sarcoideo | Dermis | Sí | + | − | Normal | − | − | − |
| Rodilla | Sarcoideo | Dermis sup+retic | Sí | + | − | Ortoqueratosis | − | − | − |
+: escasa cantidad. ++: moderada cantidad. −: ausencia; retic: reticular; sup: superficial.
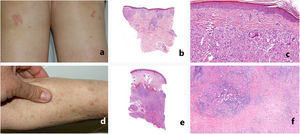
Aspecto clínico e histológico de las reacciones sarcoideas relacionadas con ICI. a-c) Sarcoidosis papulosa de las rodillas. Los granulomas están localizados predominantemente en la dermis superficial y es frecuente observar la presencia de cuerpos extraños. d-f) Sarcoidosis subcutánea. Los granulomas están prácticamente limitados al tejido celular subcutáneo, rodeados de una mayor cantidad de linfocitos e importante fibrosis.
Las pruebas de laboratorio mostraron una elevación de enzima convertidora de angiotensina en 3pacientes; no se objetivó hipercalcemia ni elevación de enzimas hepáticas en ningún paciente. En los pacientes con afectación pulmonar o adenopática se llevaron a cabo pruebas funcionales respiratorias, y en la mitad de ellos se observó una disminución de la capacidad de difusión del monóxido de carbono.
La mayoría de pacientes presentaron un cuadro leve y autolimitado, sin necesidad de tratamiento específico ni de suspensión del ICI, excepto dos pacientes, que tuvieron un curso clínico más agresivo, con afectación renal y pulmonar, que requirió suspender la inmunoterapia e iniciar corticoides sistémicos a dosis entre 0,5 y 1mg/kg/día, seguido de mantenimiento con hidroxicloroquina.
En cuanto a la neoplasia de base, 4pacientes consiguieron una remisión completa o parcial, 2pacientes fallecieron por progresión de la neoplasia y uno de ellos mantuvo la enfermedad estable.
DiscusiónLa sarcoidosis asociada a la inmunoterapia con ICI aparece en alrededor del 5% de los pacientes hacia los 5meses de tratamiento3,4 y es más frecuente en los pacientes en tratamiento con anti-CTLA-4, y especialmente en los que llevan doble inmunoterapia, en los que además puede ser más precoz y más grave4-7.
A la hora de establecer el diagnóstico es fundamental la confirmación histológica para poder diferenciarlo de una progresión tumoral, especialmente en los casos con lesiones pulmonares y mediastínicas, que pueden ser indistinguibles en las pruebas de imagen, incluso en la PET-TC8. El dermatólogo tiene un papel importante, pues uno de cada cinco pacientes tiene afectación cutánea y la piel es un órgano accesible para la biopsia7. El diagnóstico correcto va a determinar la actitud sobre el tratamiento oncológico.
La mayoría de reacciones sarcoideas por ICI son leves y autolimitadas, como en nuestros pacientes, por lo que cada vez se tiende a ser menos agresivo y a limitar el tratamiento a pacientes muy sintomáticos o con afectación cardíaca, renal, neurológica u ocular4,9. En estos casos se administran tandas de corticoides sistémicos e hidroxicloroquina, y raramente se requieren inmunosupresores10. Las manifestaciones cutáneas pueden tratarse con corticoides tópicos, aunque es frecuente que se resuelvan espontáneamente3,6.
Según la literatura, en más de la mitad de los casos se suspende la inmunoterapia al diagnosticar las reacciones sarcoideas con el objetivo de eliminar el desencadenante7. Sin embargo, cada vez tenemos mayor evidencia de que estas reacciones tienen un curso benigno y de que, en los casos leves, mantener la inmunoterapia no comporta un empeoramiento2. Por todo esto, ligado a la importancia que tiene el tratamiento de la neoplasia en la supervivencia del paciente, se cree que, excepto en los casos graves, debe priorizarse el mantenimiento del ICI7,9,10.
Estudios recientes sugieren que los pacientes en tratamiento con ICI que desarrollan reacciones sarcoideas tienen un pronóstico favorable en lo que refiere a su neoplasia de base2,7,11-13 y una mayor supervivencia respecto a los grupos control, incluso ajustando la supervivencia por otras variables como la edad, el tipo de tratamiento, las líneas de tratamiento recibidas y el tumor de base14.
Como limitaciones de este trabajo hay que destacar que se trata de un estudio unicéntrico, retrospectivo y con un número reducido de pacientes.
En resumen, las reacciones sarcoideas cutáneas relacionadas con la inmunoterapia remedan clínica e histológicamente las diferentes formas de sarcoidosis cutánea. Suelen tener un curso leve y autolimitado, y su aparición se ha asociado a una mayor supervivencia de los pacientes, por lo que, siempre que sea posible, debe priorizarse el mantenimiento de la inmunoterapia. Aunque los hallazgos clínicos, analíticos y radiológicos sean sugestivos de reacción sarcoidea, se recomienda obtener una confirmación histológica, pues el principal diagnóstico diferencial es la progresión tumoral.
FinanciaciónNo se ha dispuesto de ninguna ayuda financiera para la realización de este manuscrito.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.