Desde la implantación de las terapias biológicas para el tratamiento de la psoriasis, el paradigma del tratamiento ha cambiado, especialmente desde la aprobación de las terapias dirigidas anti-IL-17 y anti-IL-23, debido a su mayor efectividad1,2.
Los últimos consensos de expertos publicados contemplan nuevos objetivos terapéuticos diferenciando entre el objetivo óptimo y el objetivo clínicamente adecuado3 y proponen el PASI absoluto como la medida con una mayor utilidad, evitando el empleo del PASI relativo debido, en gran parte, al elevado porcentaje de pacientes que actualmente alcanzan una respuesta PASI 0. En estos pacientes se plantea, además, la posibilidad de realizar una optimización de la dosis4–6, bien mediante una disminución de la dosis administrada o bien aumentando el intervalo de tiempo entre dosis. De esta manera se consigue individualizar aún más el tratamiento al paciente, con una mejoría de la seguridad y del perfil de coste-efectividad de estas terapias, consideradas como de un impacto económico alto. También se contempla la intensificación de la dosis en los pacientes con una respuesta insuficiente.
Por otro lado, existe una discrepancia acerca del momento adecuado para realizar una optimización de dosis, tanto en la bibliografía publicada como en la práctica clínica. Se ha publicado un Consenso Delphi7 que propone como momento ideal para optimizar el tratamiento cuando el paciente alcance ≥6 meses de tratamiento y ≥6 meses con una baja actividad de la enfermedad (PASI ≤5 y/o PGA 0-2 y DLQI ≤5), con la excepción de los pacientes con una artritis psoriásica concomitante, en los que la decisión debe ser consensuada con el reumatólogo.
En este consenso se excluyeron los nuevos tratamientos biológicos dirigidos contra la IL-17 e IL-23 debido a la baja evidencia existente. Sobre estos tratamientos se está llevando a cabo un ensayo clínico con el objetivo de evaluar la actividad de la enfermedad tras la reducción de la dosis8.
El secukinumab es un anticuerpo monoclonal dirigido contra la IL-17A cuya dosis aprobada en la ficha técnica para la fase de mantenimiento del tratamiento es de 300mg cada 4 semanas9.
Realizamos un estudio observacional, retrospectivo, unicéntrico en el cual se revisaron todos los pacientes tratados en el Hospital Universitario Doctor Peset con el secukinumab entre enero de 2015 y enero de 2023 y se incluyeron en el estudio aquellos que hubieran recibido una dosis optimizada con el objetivo de comunicar nuestra experiencia clínica tras la optimización de dosis.
La optimización de la dosis se realizó en los pacientes que alcanzaron un PASI 0 y que persistieron como mínimo hasta la semana 52 desde inicio del tratamiento con PASI 0, sin que existiesen fluctuaciones en la actividad de la enfermedad en las últimas visitas de seguimiento.
Se recogieron las características demográficas iniciales y los índices de gravedad de la enfermedad en la primera visita incluyendo PASI, Body Area Surface (BSA) y Dermatology Life Quality Index (DLQI) y la evolución de la gravedad de la enfermedad medida en el PASI en el momento de iniciar el secukinumab a la dosis habitual y a las 8, 16, 24 y 52 semanas tras el inicio y, finalmente, el valor del PASI al momento de cambiar a la dosis optimizada de secukinumab y a las 16, 24 y 52 semanas desde la optimización de dosis.
Se consideró como un criterio de éxito de la optimización el propuesto por Llamas-Velasco y Daudén4 en otras terapias biológicas, basado en la persistencia de la estrategia optimizada del tratamiento a los 6 meses desde la modificación de dosis.
Se identificaron 86 pacientes que habían recibido secukinumab en nuestro centro (63 se mantienen en tratamiento activo), 12 de los cuales recibieron una dosis optimizada. Uno de estos últimos se excluyó del trabajo debido a su participación dentro del estudio OPTIMISE.
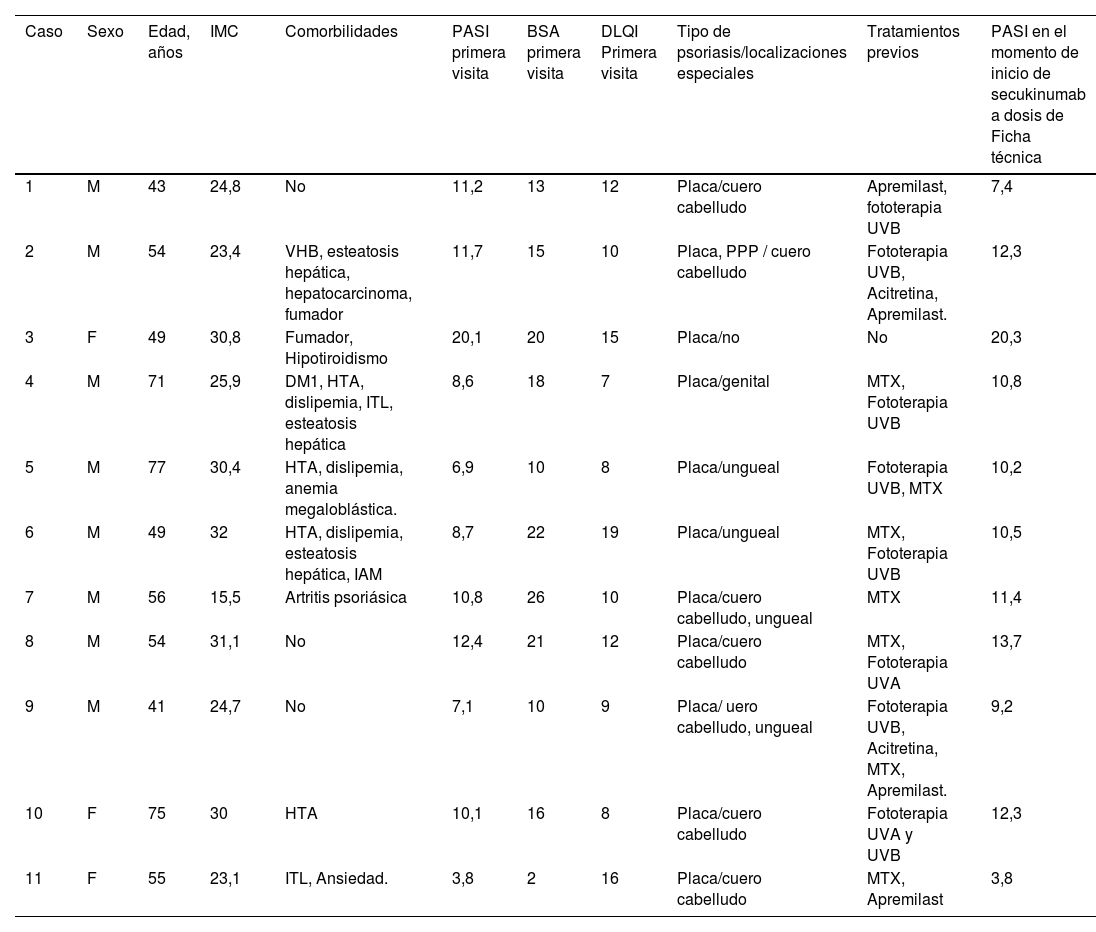
Las características epidemiológicas, de gravedad y tiempos de seguimiento se resumen en las tablas 1 y 2.
Características demográficas y clínicas en la primera visita registrada en nuestro servicio y en el momento de inicio de secukinumab a dosis de ficha técnica
| Caso | Sexo | Edad, años | IMC | Comorbilidades | PASI primera visita | BSA primera visita | DLQI Primera visita | Tipo de psoriasis/localizaciones especiales | Tratamientos previos | PASI en el momento de inicio de secukinumab a dosis de Ficha técnica |
|---|---|---|---|---|---|---|---|---|---|---|
| 1 | M | 43 | 24,8 | No | 11,2 | 13 | 12 | Placa/cuero cabelludo | Apremilast, fototerapia UVB | 7,4 |
| 2 | M | 54 | 23,4 | VHB, esteatosis hepática, hepatocarcinoma, fumador | 11,7 | 15 | 10 | Placa, PPP / cuero cabelludo | Fototerapia UVB, Acitretina, Apremilast. | 12,3 |
| 3 | F | 49 | 30,8 | Fumador, Hipotiroidismo | 20,1 | 20 | 15 | Placa/no | No | 20,3 |
| 4 | M | 71 | 25,9 | DM1, HTA, dislipemia, ITL, esteatosis hepática | 8,6 | 18 | 7 | Placa/genital | MTX, Fototerapia UVB | 10,8 |
| 5 | M | 77 | 30,4 | HTA, dislipemia, anemia megaloblástica. | 6,9 | 10 | 8 | Placa/ungueal | Fototerapia UVB, MTX | 10,2 |
| 6 | M | 49 | 32 | HTA, dislipemia, esteatosis hepática, IAM | 8,7 | 22 | 19 | Placa/ungueal | MTX, Fototerapia UVB | 10,5 |
| 7 | M | 56 | 15,5 | Artritis psoriásica | 10,8 | 26 | 10 | Placa/cuero cabelludo, ungueal | MTX | 11,4 |
| 8 | M | 54 | 31,1 | No | 12,4 | 21 | 12 | Placa/cuero cabelludo | MTX, Fototerapia UVA | 13,7 |
| 9 | M | 41 | 24,7 | No | 7,1 | 10 | 9 | Placa/ uero cabelludo, ungueal | Fototerapia UVB, Acitretina, MTX, Apremilast. | 9,2 |
| 10 | F | 75 | 30 | HTA | 10,1 | 16 | 8 | Placa/cuero cabelludo | Fototerapia UVA y UVB | 12,3 |
| 11 | F | 55 | 23,1 | ITL, Ansiedad. | 3,8 | 2 | 16 | Placa/cuero cabelludo | MTX, Apremilast | 3,8 |
BSA: Body Surface Area; DLQI: Dermatology Life Quality Index; DM1: diabetes mellitus 1; F: femenino; HTA: hipertensión arterial; IAM: infarto agudo de miocardio; ITL: infección tuberculosa latente; M: masculino; MTX: metotrexato; PASI: Psoriasis Area Severity Index; PPP: psoriasis palmoplantar pustulosa; UVA: ultravioleta A; UVB: ultravioleta B; VHB: virus hepatitis B.
Tiempo medio de seguimiento y mantenimiento de la dosis optimizada e índices medios de gravedad en primera visita y PASI medio previo al inicio de secukinumab (n=11)
| Tiempo medio de seguimiento | 90,54 meses [43-126] |
|---|---|
| Número de pacientes con las diferentes estrategias de optimización empleadas | |
| 300mg cada 5 semanas | 7 |
| 300mg cada 6 semanas | 3 |
| 150mg cada 4 semanas | 1 |
| *El único paciente optimizado a 150mg cada 4 semanas se debía a un IMC extremadamente bajo de 15,8 | |
| Tiempo medio de mantenimiento de la dosis optimizada | 22,6 meses [6-46] |
| IMC medio | 26,5 |
| BSA media primera visita | 15,7 |
| PASI media primera visita | 10,1 |
| DLQI media primera visita | 11,45 |
| PASI media al inicio de secukinumab | 11,2 |
BSA: Body Area Surface; DLQI: Dermatology Life Quality Index; IMC: Índice de Masa Corporal; PASI: Psoriasis Area Severity Index.
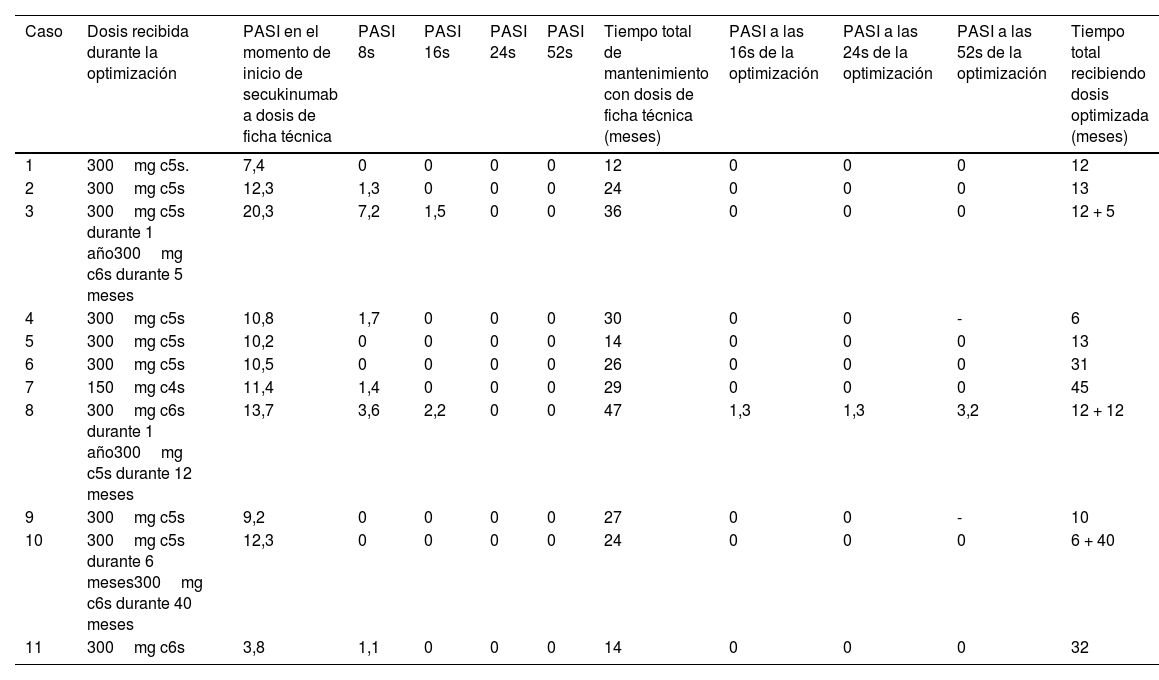
La dosis optimizada recibida en cada caso y la evolución clínica del PASI previa y durante la optimización de dosis se muestra en la tabla 3.
Evolución clínica con secukinumab recibiendo dosis de mantenimiento aprobada en ficha técnica y la dosis optimizada. Se describe también la dosis recibida por cada uno de los pacientes
| Caso | Dosis recibida durante la optimización | PASI en el momento de inicio de secukinumab a dosis de ficha técnica | PASI 8s | PASI 16s | PASI 24s | PASI 52s | Tiempo total de mantenimiento con dosis de ficha técnica (meses) | PASI a las 16s de la optimización | PASI a las 24s de la optimización | PASI a las 52s de la optimización | Tiempo total recibiendo dosis optimizada (meses) |
|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 300mg c5s. | 7,4 | 0 | 0 | 0 | 0 | 12 | 0 | 0 | 0 | 12 |
| 2 | 300mg c5s | 12,3 | 1,3 | 0 | 0 | 0 | 24 | 0 | 0 | 0 | 13 |
| 3 | 300mg c5s durante 1 año300mg c6s durante 5 meses | 20,3 | 7,2 | 1,5 | 0 | 0 | 36 | 0 | 0 | 0 | 12 + 5 |
| 4 | 300mg c5s | 10,8 | 1,7 | 0 | 0 | 0 | 30 | 0 | 0 | - | 6 |
| 5 | 300mg c5s | 10,2 | 0 | 0 | 0 | 0 | 14 | 0 | 0 | 0 | 13 |
| 6 | 300mg c5s | 10,5 | 0 | 0 | 0 | 0 | 26 | 0 | 0 | 0 | 31 |
| 7 | 150mg c4s | 11,4 | 1,4 | 0 | 0 | 0 | 29 | 0 | 0 | 0 | 45 |
| 8 | 300mg c6s durante 1 año300mg c5s durante 12 meses | 13,7 | 3,6 | 2,2 | 0 | 0 | 47 | 1,3 | 1,3 | 3,2 | 12 + 12 |
| 9 | 300mg c5s | 9,2 | 0 | 0 | 0 | 0 | 27 | 0 | 0 | - | 10 |
| 10 | 300mg c5s durante 6 meses300mg c6s durante 40 meses | 12,3 | 0 | 0 | 0 | 0 | 24 | 0 | 0 | 0 | 6 + 40 |
| 11 | 300mg c6s | 3,8 | 1,1 | 0 | 0 | 0 | 14 | 0 | 0 | 0 | 32 |
c4s: cada 4 semanas; c5s: cada 5 semanas; c6s: cada 6 semanas; PASI: Psoriasis Area Severe Index; S: semanas.
De nuestra serie, 2 pacientes no alcanzan todavía las 52 semanas de seguimiento tras la optimización. El 100% de los pacientes alcanzaron el éxito terapéutico con la optimización de dosis basada en el criterio propuesto.
En publicaciones sobre la práctica clínica en la optimización de la dosis con los fármacos anti-TNF y el ustekinumab4–6 se constata la efectividad de estas posologías. Es preciso seleccionar los candidatos, planteando las variables a tener en cuenta: el tiempo de evolución de la enfermedad, la persistencia previa con el mismo tratamiento biológico, la presencia de artritis psoriásica, el índice de masa corporal (IMC) o haber recibido previamente otras terapias biológicas.
Recientemente, en el estudio OPTIMISE se evaluó la eficacia y la seguridad de dosis diferentes del secukinumab en la fase de mantenimiento con el objetivo de demostrar que no había una inferioridad de estas respecto a la dosis indicada en la ficha técnica. En este estudio se observó un peor mantenimiento de la respuesta en los pacientes que recibieron el secukinumab 300mg cada 6 semanas (evaluado mediante PASI 90) a la semana 5210.
Estos resultados contrastan con nuestra experiencia clínica. A excepción de un caso que mantuvo un PASI medio de 1,9 durante las 52 primeras semanas tras la optimización, todos los pacientes mantuvieron no solo una respuesta relativa PASI 90 sino una respuesta PASI 0.
El IMC medio en ambas poblaciones fue similar (26,5 en nuestra serie, 28,5 en estudio OPTIMISE) y en ambas series se incluyeron solo pacientes no tratados con un biológico previamente.
Las poblaciones difieren en el valor medio de PASI inicial, más alto del OPTIMISE, si bien esto es habitual al comparar las poblaciones de los ensayos clínicos con las de la práctica clínica habitual.
Como aspecto diferencial, en nuestra serie todos los pacientes habían mantenido una respuesta completa al tratamiento durante un mínimo de 52 semanas, a diferencia del estudio OPTIMISE en el que se plantea la optimización de dosis a las 24 semanas en pacientes con respuesta PASI 90. La elección de unos criterios más estrictos de control de la enfermedad tanto en cuanto al tiempo previo de exposición al fármaco (un mínimo de 52 semanas en vez de 24 semanas) como en términos de efectividad clínica (PASI 0 en vez de PASI 90 relativo) podrían ser claves para justificar las diferencias observadas en la respuesta tras optimización.
En conclusión, en nuestra experiencia, la optimización de la dosis del secukinumab en pacientes con una persistencia del aclaramiento completo tras un mínimo de 52 semanas desde inicio del tratamiento es una buena alternativa posológica, dado que hemos obtenido una respuesta PASI 0 mantenida en 10 de los 11 pacientes incluidos en nuestra serie al menos durante 6 meses. Estos pacientes seleccionados tienen un IMC entre 25 y 30 y no han recibido previamente ningún tratamiento biológico previo, y con la disminución se mejoró, además, la ratio coste-efectividad del tratamiento con el secukinumab.
Son necesarios estudios con mayor tamaño muestral que permitan determinar si estas variables se relacionan de forma estadísticamente significativa con una buena respuesta mantenida tras la optimización de dosis y estudios comparativos para evaluar si el empleo de criterios de optimización más estrictos, como en nuestra serie, se asocia a una mejor respuesta tras optimización de dosis.
FinanciaciónNo se ha recibido financiación para la preparación de este manuscrito.
Contribución de los autoresTodos los autores han contribuido intelectualmente al manuscrito, cumplen las condiciones de autoría y han aprobado la versión final del mismo.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.