La oruga procesionaria del pino es la forma larvaria del lepidóptero nocturno Thaumetopoea pityocampa (TP). Supone una plaga forestal en los países mediterráneos y se está expandiendo hacia el norte de Europa por el calentamiento global. Durante sus tres últimos estadios larvarios presenta unos pelos urticantes de pequeño tamaño, que se desprenden con facilidad y pueden ser transportados por el viento. Estos pelos pueden producir distintas patologías, entre las que destaca la afectación cutánea que se manifiesta fundamentalmente como urticaria de contacto y dermatitis papulosa. También son capaces de clavarse e irritar la mucosa conjuntival y de penetrar en la vía respiratoria produciendo manifestaciones a este nivel. En los últimos años se han descrito varios casos de reacciones anafilácticas por este insecto.
Los mecanismos patogénicos implicados incluyen el mecánico o irritativo y el alérgico por hipersensibilidad mediada por IgE, donde las reacciones son inmediatas, repetidas y progresivamente más graves.
The pine processionary caterpillar is the larval form of the Thaumetopoea pityocampa moth. Mediterranean forests regularly suffer plagues of this insect, which has been moving north as a result of global warming. When the small urticating hairs that develop during the last 3 larval stages are shed and can become airborne. If they come in contact with skin, they can cause a variety of reactions, notably contact urticaria and papular rashes. Irritation can also occur if the hairs lodge in the mucosa of the conjunctiva or in the respiratory tract. Several cases of anaphylactic reactions have been reported in recent years. Mechanical (irritative) mechanisms may be involved in the pathogenesis of lesions, or immunoglobulin E-mediated allergic hypersensitivity reactions may be implicated when the process is rapid, recurrent, and progressively more severe.
Los lepidópteros constituyen uno de los grupos de insectos más numerosos del mundo, con cerca de 150.000 especies descritas1. Las orugas son las formas larvarias de estos insectos y las causantes de la mayor parte de las reacciones patológicas por lepidópteros en humanos, aunque también se han descrito tras el contacto con el insecto adulto (polillas o mariposas). Esto sucede porque las orugas, objetivo de múltiples predadores, disponen de mecanismos de defensa como verdaderas espinas punzantes, pequeños pelos irritantes y diversas sustancias tóxicas2–4.
La terminología empleada para describir las reacciones por lepidópteros es confusa y en ocasiones contradictoria. Propiamente hablando, el término erucismo procede del latín eruca (oruga), por lo que debería reservarse a cualquier patología ocasionada por la oruga o fase larvaria de estos insectos. La palabra lepidopterismo deriva del griego lepis (escamas) y pteron (alas) y su empleo se restringiría a las reacciones originadas exclusivamente por las fases adultas reproductoras de los lepidópteros: polillas y mariposas. Sin embargo, con frecuencia se emplean incorrectamente estos términos, aplicando la palabra erucismo para referirse a la afectación exclusivamente cutánea producida por los lepidópteros en cualquier fase de su desarrollo y lepidopterismo cuando hay afectación distinta de la cutánea. Siguiendo el criterio de una reciente revisión2 no usaremos esta terminología y nos referiremos directamente al tipo de manifestación clínica y a su causa (por ejemplo urticaria de contacto por Thaumetopoea).
El presente artículo se centra en la patología cutánea ocasionada por la oruga procesionaria del pino (Thaumetopoea pityocampa [TP]), una de las principales plagas forestales del sur de Europa y de otros países mediterráneos5–7 y la causa más frecuente de reacciones adversas a lepidópteros en España. Estudios recientes apuntan además la posibilidad de su expansión hacia el norte, en relación con el calentamiento global, así como la mayor incidencia de patología en humanos debido al crecimiento de zonas residenciales en la periferia de las ciudades, muchas de ellas en la proximidad de pinares infestados por procesionaria5,8,9. La TP se alimenta de las acículas de diferentes especies de coníferas, incluyendo el pino piñonero (Pinus pinea), del que se obtienen los piñones para consumo humano y de los que España es el principal productor mundial (fig. 1).
En su estadio larvario las orugas están repletas de pelillos urticantes microscópicos que son capaces de penetrar en la epidermis y en las membranas mucosas. La clínica ocasionada con mayor frecuencia es la cutánea, aunque también se han descrito casos de afectación ocular, rinitis e incluso manifestaciones respiratorias y anafilaxia. Los mecanismos propuestos como causantes de estas reacciones incluyen los mecánicos o irritativos, los químicos o tóxicos tras la liberación de sustancias (actualmente en entredicho) y el desencadenamiento de una reacción alérgica mediada por IgE frente a diversas proteínas de la oruga2,3,10–21.
El mejor conocimiento por el dermatólogo de la biología y patología ocasionada por la TP permitirá diagnosticar y tratar correctamente las reacciones desencadenadas por este insecto.
BiologíaLa polilla procesionaria del pino (TP) es un lepidóptero nocturno de la familia Thaumetopoeidae (Notodontidae) (fig. 2). Se distribuye por parte de Europa, Norte de África y Oriente Medio. En Europa hay tres especies de Thaumetopoea: en el norte predomina Thaumetopoea pinivora, en la zona centro Thaumetopoea processionea y en la zona mediterránea Thaumetopoea pityocampa22. En España está presente en toda la península y en las islas Baleares, aunque se encuentra fundamentalmente en la zona centro y en el sur. Afecta a todas las especies de pino, tanto locales como introducidas (Pinus pinaster, P. silvestris, P. halapensis, P. nigra, P. pinea, P. radiata, P. ponderosa y P. canariensis) y también a los cedros7.
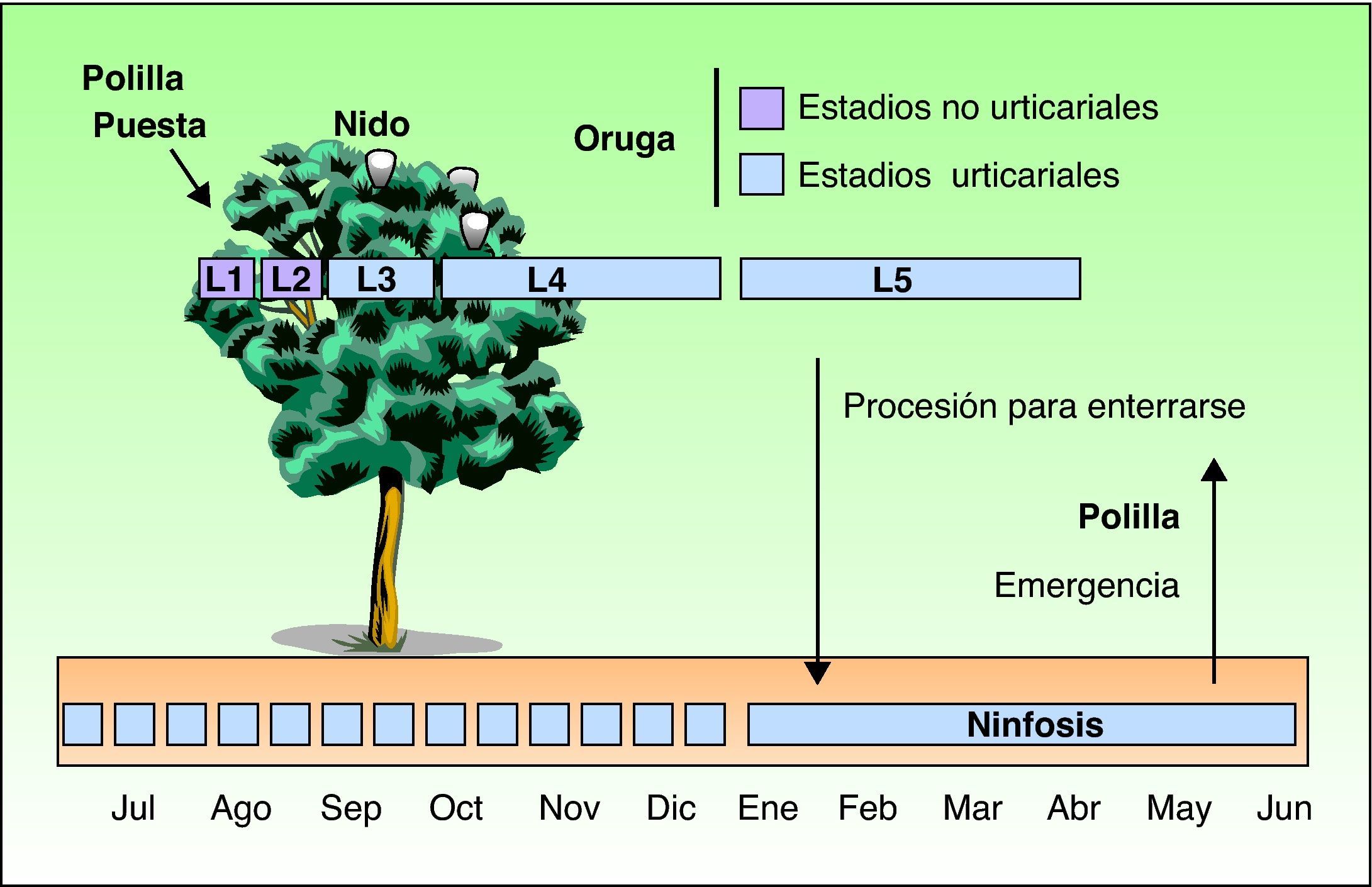
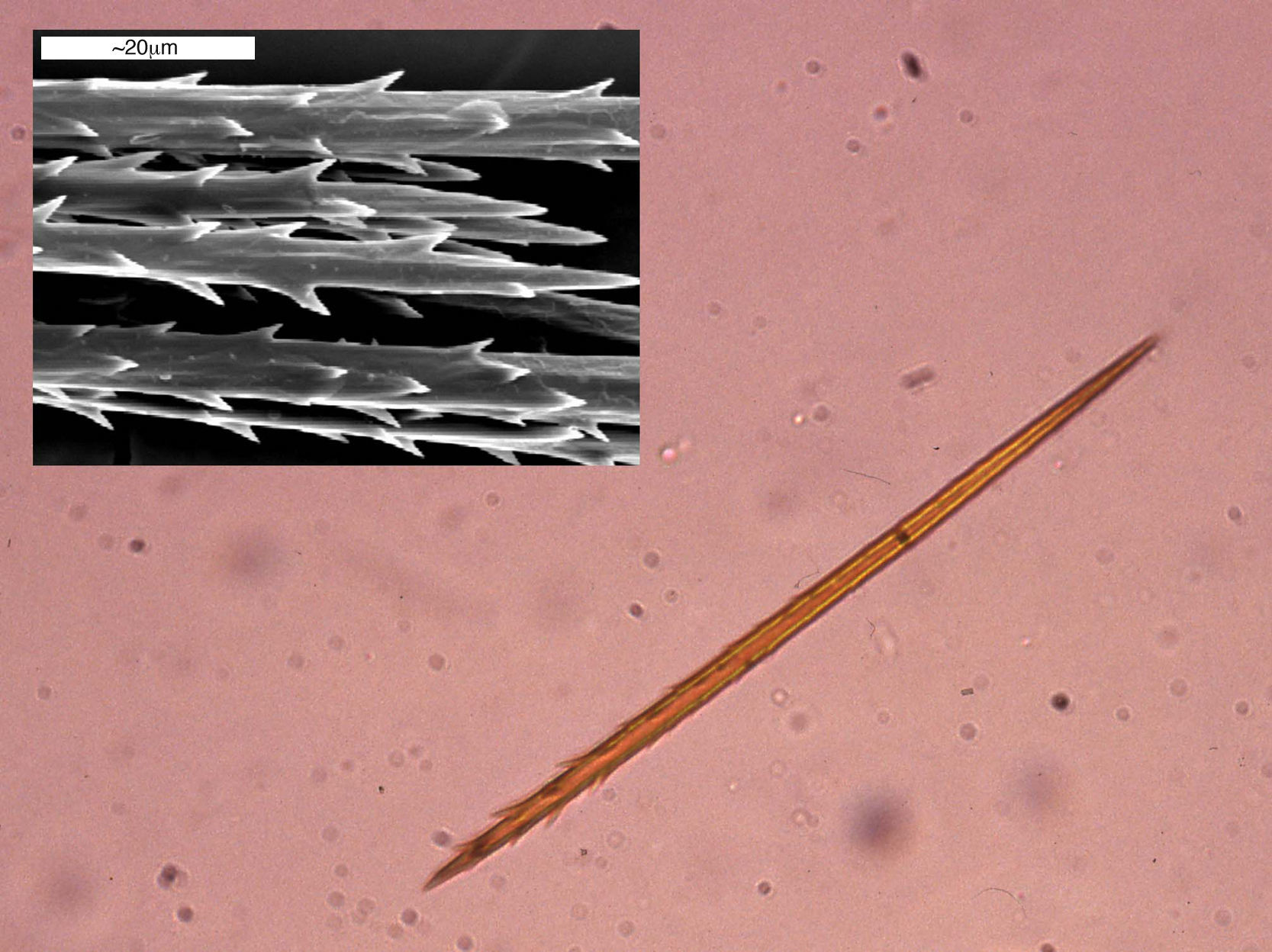
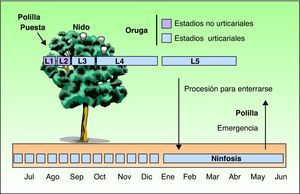
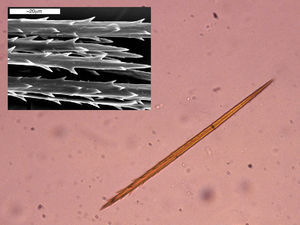
Como todos los lepidópteros, TP pasa por cuatro fases de desarrollo: polilla, huevo, larva y crisálida. Su ciclo biológico (fig. 3) está muy condicionado por el clima, motivo por el cual se está estudiando la expansión de este insecto hacia el norte como modelo biológico en el contexto del cambio climático. Las polillas representan la fase adulta reproductora del insecto. Tras la fecundación depositan los huevos en las acículas de los pinos de los que eclosionarán las orugas a los 30 o 40 días. Las orugas se desarrollan pasando por 5 estadios larvarios, teniendo desde el principio un comportamiento gregario y una característica forma de desplazarse en fila, una detrás de otra como en procesión, de donde les viene su nombre. A partir del tercer estadio larvario (L3), que tiene lugar según el clima durante los meses de septiembre a noviembre, la colonia forma bolsones o nidos de invierno fácilmente visibles en la copa de los pinos (fig. 4). Aunque las orugas desde su nacimiento ya tienen grandes pelos macroscópicamente visibles, en el estadio L3 aparecen, además, otros pelillos microscópicos en 8 receptáculos anaranjados ubicados en el dorso. Estos elementos microscópicos similares a pelillos (llamados en la literatura científica “setae”) tienen entre 150-200 micras de longitud y 5 micras de diámetro y, a diferencia de los verdaderos pelos, carecen de conexión neuronal y se desprenden fácilmente del tegumento con cualquier tipo de agresión o estimulación mecánica10. A partir de L3, con cada muda se producen nuevos pelillos permaneciendo los antiguos en los restos larvarios. Igualmente, los capullos en donde se produce la pupación bajo la tierra están también recubiertos de pelillos urticantes10. Son verdaderos arpones capaces de clavarse en la piel o en las mucosas ocular y respiratoria (fig. 5). Además, se ha comprobado su presencia en el aire mediante técnicas para detectar polen o diversos microorganismos aerotransportados23, por lo que pueden ocasionar problemas sin un contacto directo con las orugas. La abundancia de los pelillos en el aire se relaciona con la distancia a las zonas de producción, las condiciones meteorológicas (más cantidad y se desplazan a mayor distancia los días de viento) y el momento del ciclo biológico (aumentan progresivamente desde el estadio L3, llegando a tener cada oruga en su quinto o último estadio —L5— más de 1.000.000)24. Pueden engancharse en objetos (madera, piñas, ropa, etc.) o en el pelo de animales (mascotas o ganado) y ocasionar síntomas fuera de los pinares. Además, son capaces de permanecer durante largos periodos de tiempo, incluso años, en el medio ambiente, con lo que los pacientes pueden presentar reacciones a lo largo de todo el año13,25. En los primeros días francamente primaverales (dependiendo zonas y años entre los meses de enero y mayo), las orugas maduras (L5) abandonan los pinos en procesión, encabezadas por una hembra, para dirigirse a los lugares de enterramiento (bordes o claros del monte en hábitats fríos o templados y zonas sombreadas en las áreas más cálidas) (figs. 6 y 7). Es por tanto en esos momentos, durante el estadio final del desarrollo de la oruga (L5), cuando se produce el mayor número de reacciones a este insecto: la posibilidad de contacto con las orugas es mayor y el número de pelillos y la alergenicidad de las orugas es máximo26. Bajo el suelo las orugas pasan a la fase de crisálida (fig. 8) en la que existe un periodo de diapausa o detenimiento del desarrollo, que puede tener una duración muy variable (desde menos de un mes hasta 4 años, según las condiciones climáticas)7. Este hecho justifica la dificultad para controlar la plaga y la presencia en el suelo de pelillos y restos de las orugas durante todo el año con las consiguientes repercusiones clínicas en visitantes o trabajadores que remueven la arena de un pinar. Finalmente, las polillas emergen del suelo en los días de verano para iniciar un nuevo ciclo.
Grupo de orugas enterrándose en el suelo. Obsérvese que presentan pelos de gran tamaño (2-3mm de longitud) y otros mucho más numerosos y pequeños (0,2-1mm) localizados en el dorso, que dan el característico color marrón de la oruga procesionaria del pino y que son los responsables de la patología que ocasiona.
En la actualidad la importancia de la patología por TP está subestimada tanto en la clínica como en la literatura científica. El motivo quizá sea que la mayoría de las reacciones son leves y pasajeras, y muchas veces el mismo paciente conoce la causa y no le da importancia o simplemente se automedica. Sin embargo, en ocasiones la sospecha clínica no es tan evidente y los diagnósticos diferenciales son múltiples. Además, no conviene perder de vista la posibilidad de reacciones más graves que muchas veces se tratan sintomáticamente sin llegar a diagnosticar su causa, o sin aportar al paciente la información necesaria para que no se repitan.
Otro factor a tener en cuenta es que, si bien lo habitual es la afectación de individuos aislados, en ocasiones se presentan verdaderas epidemias relacionadas con la exposición a zonas de pinares con gran infestación, con el ciclo biológico de la oruga (febrero a abril) y con las condiciones metereológicas, sobre todo el viento fuerte que facilita la dispersión de los pelos urticantes. Además, la procesionaria del pino puede permanecer en forma de crisálida durante varios años si la situación climática no es favorable, y puede acontecer la aparición simultánea de varias generaciones de orugas con mayor riesgo de una afectación epidémica por TP25.
Hay pocos datos epidemiológicos publicados con respecto a las reacciones provocadas por TP. Recientemente se ha realizado en la provincia de Valladolid (un área endémica con amplias zonas de pinares deforestadas por TP) un estudio transversal, aleatorizado y estratificado por edad, sexo y hábitat en 1.224 participantes9. Se detectó una prevalencia de reacciones cutáneas por TP del 12% en áreas rurales, del 9,6% en áreas semiurbanas con pinares cercanos y del 4,4% en el área urbana. Se objetivó que el riesgo de reacciones cutáneas por TP está en relación directa con la exposición a la oruga, y no con la edad o la constitución atópica, por lo que los trabajadores de zonas de pinares representan el colectivo más expuesto a patología por procesionaria (riesgo 5 veces mayor). Además, muchos de estos trabajadores tienen una sensibilización mediada por IgE y con ello la posibilidad de reacciones más graves. Las profesiones de mayor riesgo son los recolectores de piñas y leñadores, seguidos a más distancia de recolectores de resina, agricultores, ganaderos, guardas forestales, jardineros, albañiles o transportistas que trabajan en áreas de pinares9,12–14,17. Conviene tener en cuenta que los síntomas pueden presentarse también en otras fechas, coincidiendo con el inicio de las labores de poda y recolección de piñas durante el otoño o con la recogida de leña o arena en los meses de verano.
La población infantil es especialmente susceptible a la afectación por los lepidópteros, seguramente por la curiosidad de los niños que les lleva a tocar las orugas o por jugar con la arena o la vegetación que contiene a estos insectos15,19,27. Un estudio sobre la prevalencia de las reacciones cutáneas por TP en niños de una zona rural endémica mostró que el 9,2% de los niños tenían antecedentes de esta patología15. Esta prevalencia puede aumentar cuando se trata de áreas urbanas periféricas o semiurbanas con pinos infestados muy próximos, o incluso dentro de las propias parcelas donde viven los niños.
Mecanismos patogénicosLa naturaleza irritante de las larvas de Thaumetopoea es bien conocida desde la antigua Grecia10, y existen referencias de que ya los romanos arrojaban a los reos en zanjas llenas de procesionarias como pena muy severa28. Sin embargo, las primeras descripciones de la procesionaria del pino fueron hechas por Reamur en 1736 y posteriormente por Fabre en 190029. Desde entonces y durante años se ha aceptado que las reacciones por TP eran ocasionadas por el factor mecánico-irritativo que supone clavarse en la piel los pelos de la oruga junto a la liberación de sustancias tóxicas o irritantes.
El mecanismo tóxico ha sido demostrado en las orugas de diversos lepidópteros. La penetración en la piel de los pelos urticantes produce una degranulación de los basófilos con la consiguiente liberación de histamina. En el caso de la TP esta degranulación independiente de IgE se ha relacionado con una proteína presente en los pelos de la oruga denominada Thaumetopoeina30. Sin embargo, este mecanismo ha sido puesto en entredicho recientemente en un estudio que demuestra la lentitud en la aparición de las lesiones cutáneas después de la exposición intracutánea a los pelillos de otra especie urticante de Thaumetopoea (T. pinivora) y que contradice el papel que puedan desempeñar mediadores rápidos como la histamina22. Este hecho, junto con el dato de que el pretratamiento de los pelillos con diversos productos químicos o tras calentamiento no modifica su acción inflamatoria, desmiente, según algunos autores, la participación de un mecanismo tóxico en la patología por Thaumetopoea10.
La presencia en algunos individuos de reacciones más intensas, inmediatas, sin un contacto directo con la oruga y en condiciones de exposición similares a otros con mínima clínica, o incluso sin ella, ha llevado a la sospecha de la participación en estos pacientes de un mecanismo alérgico mediado por IgE. En 1993 Werno et al encontraron anticuerpos IgE frente a thaumetopoein (28-kDa) en el 20% de un grupo de trabajadores expuestos21. Moneo et al purificaron una proteína de 15-kDa (Tha p1) que fue reconocida por anticuerpos IgE de pacientes alérgicos a TP31. Este mecanismo ha sido ya demostrado en numerosos trabajos mediante la detección de IgE específica por el método de immunoblot, así como por la presencia de pruebas cutáneas positivas realizadas por punción con extracto total de larva a concentraciones no irritativas (previamente probadas en controles)12–20.
En áreas endémicas, mediante prueba cutánea de punción con extracto de cuerpo entero de oruga, se han encontrado positividades en el 53 y 58% de individuos con sospecha de reacciones por TP13. Aunque esta técnica es muy sensible, su especificidad es baja. Sin embargo, los resultados del IgE-immunoblotting fueron positivos en el 72% de los pacientes con pruebas cutáneas positivas, demostrando así la utilidad de dichas pruebas13. Teniendo en cuenta estos resultados, parece que las reacciones alérgicas por hipersensibilidad mediada por IgE frente a este insecto son al menos tan importantes como en las que no se demuestra un mecanismo alérgico.
De momento no hay evidencias concluyentes sobre la participación de otros tipos de mecanismos de hipersensibilidad, aunque es probable la implicación de la inmunidad celular en algunos casos. También parece que la quitina y sus productos de degradación, potentes promotores y reguladores de las reacciones inmunes, pueden desempeñar un papel en la sensibilidad variable a este insecto10.
En resumen, podemos decir que la irritación mecánica de la piel sería la causa de la patología tras el contacto con la TP que ocurre en todos los individuos expuestos, y que en algunos individuos susceptibles se desencadenaría una reacción alérgica IgE mediada de mayor gravedad. Queda sin embargo por demostrar la presencia de un mecanismo tóxico por liberación de sustancias químicas y la participación de otras vías de la inmunidad en la patología por TP.
Anatomía patológicaAunque los hallazgos histopatológicos tras el contacto con lepidópteros no son específicos, se han descrito distintos patrones que pueden variar según las especies implicadas. Algunas incluyen fenómenos necróticos localizados, formación de vesículas, reacciones granulomatosas de cuerpo extraño, infiltrados inflamatorios de predominio linfocitario, presencia de eosinófilos, etc.32.
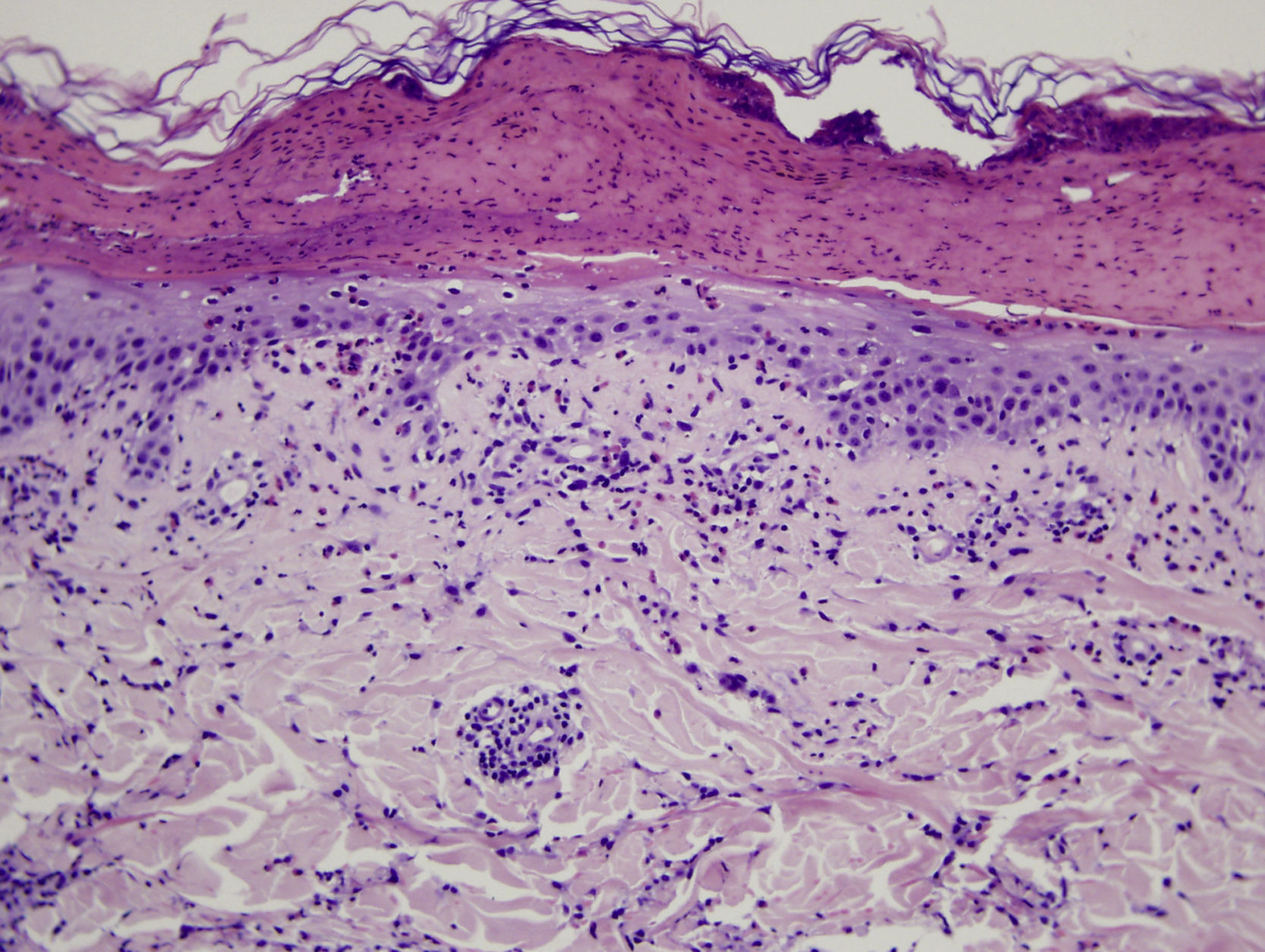
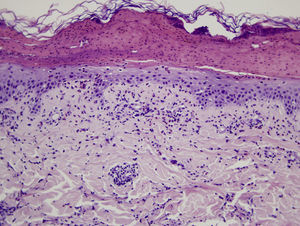
La valoración microscópica de las distintas reacciones cutáneas por TP también es inespecífica y no es diagnóstica. Se han descrito diferentes tipos de reacciones cutáneas por TP: urticaria de contacto y distintos tipos de dermatitis (papulosa, vesiculosa y pustulosa16,33). La afectación vesículo-pustulosa es más frecuente en niños y no hay descripciones histopatológicas. Se ha descrito el patrón microscópico de la clínica cutánea más característica, la dermatitis papulosa. Se observa una reacción inespecífica inflamatoria con edema epidérmico y un infiltrado linfohistiocitario perivascular con eosinófilos, similar a las picaduras o reacciones a otros insectos (fig. 9).
Imagen histológica en la que se observa una vesícula con restos de leucocitos y suero coagulado. En la epidermis que forma su base se aprecia leve espongiosis y exocitosis de eosinófilos, y en dermis superficial un infiltrado predominantemente perivascular de linfocitos y eosinófilos.
La afectación cutánea es la manifestación clínica más frecuente por la exposición a TP. También son habituales las manifestaciones oculares y, ya más raramente, los síntomas respiratorios e incluso las reacciones anafilácticas12–20,33.
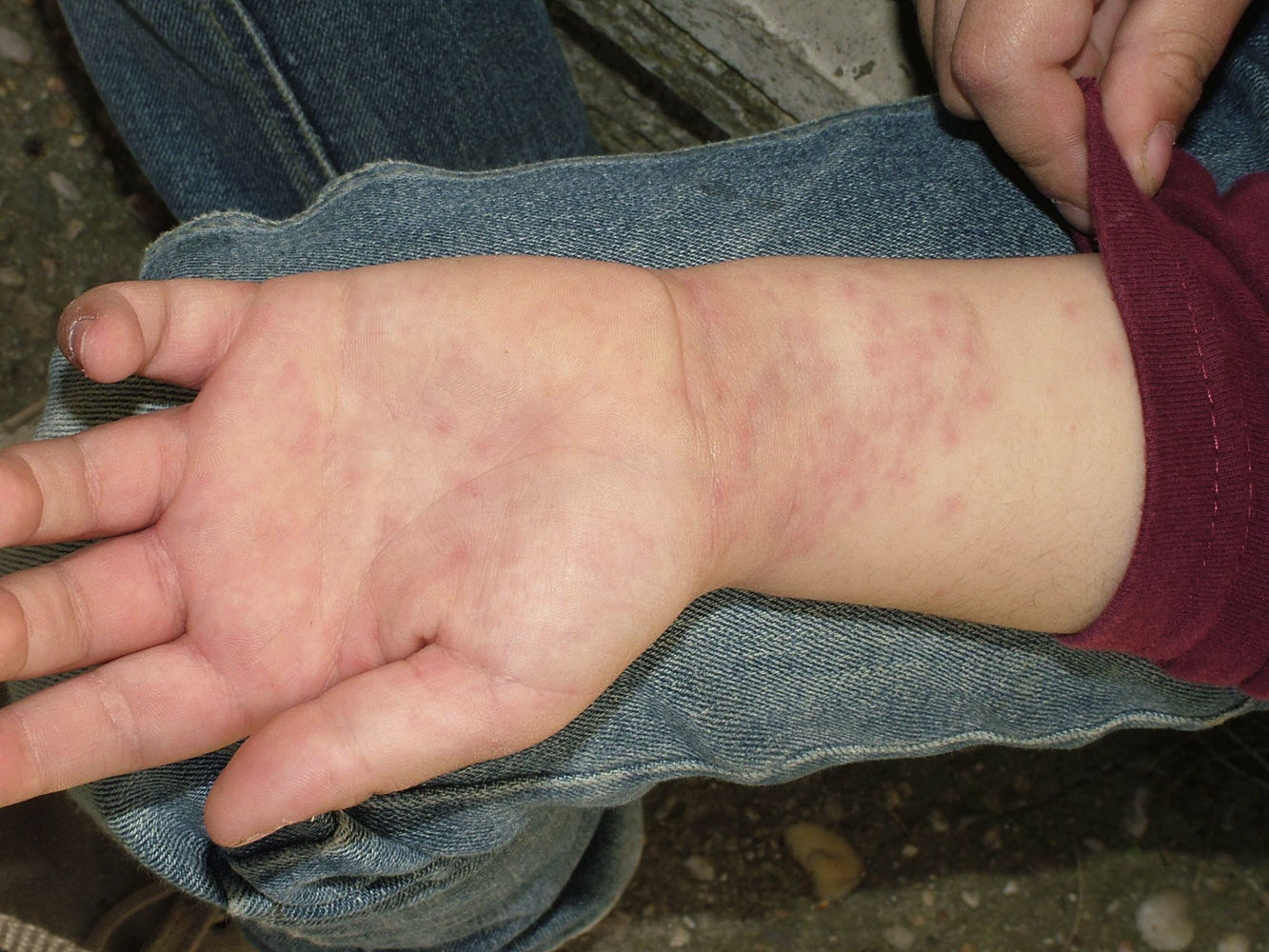
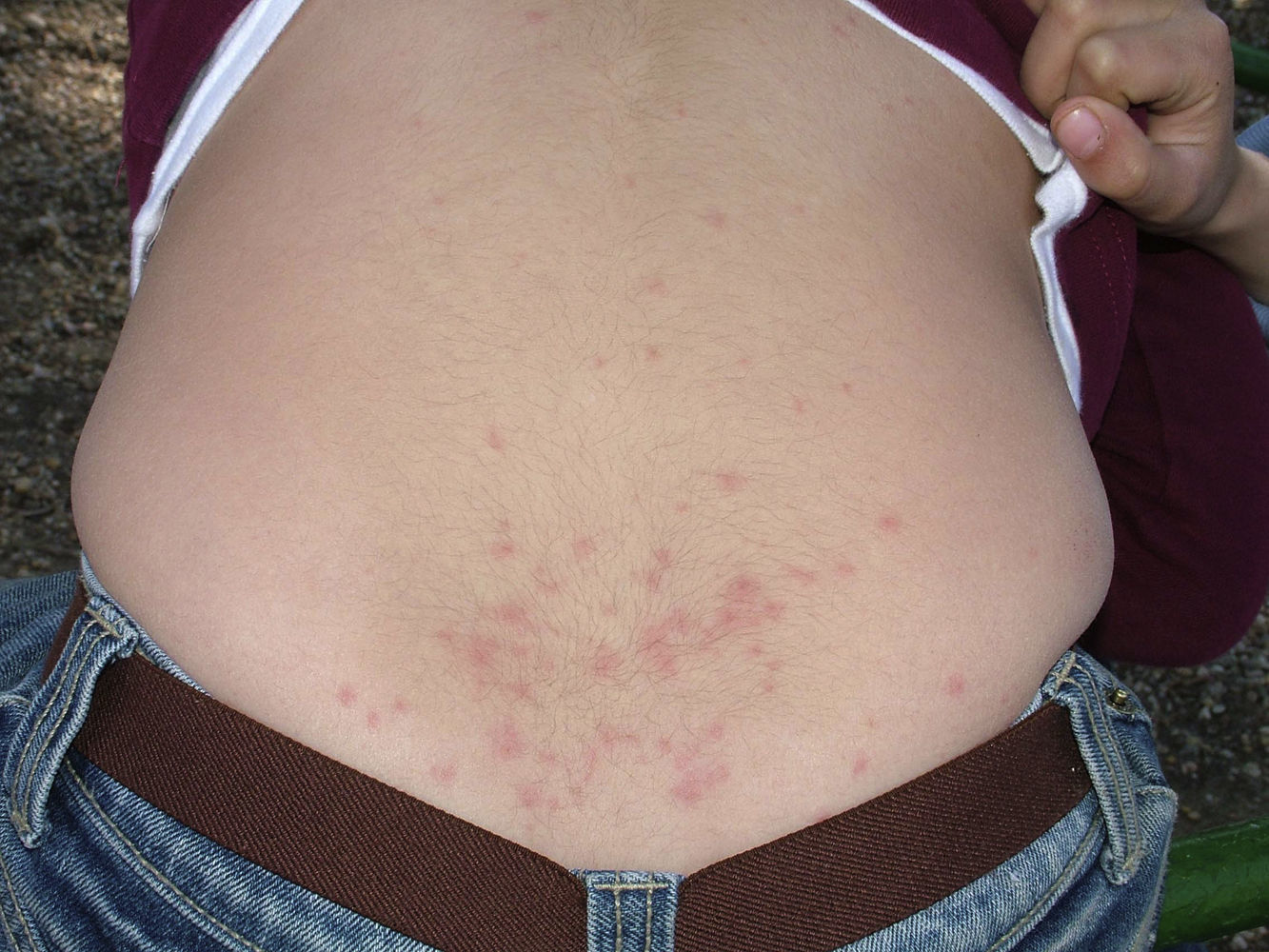
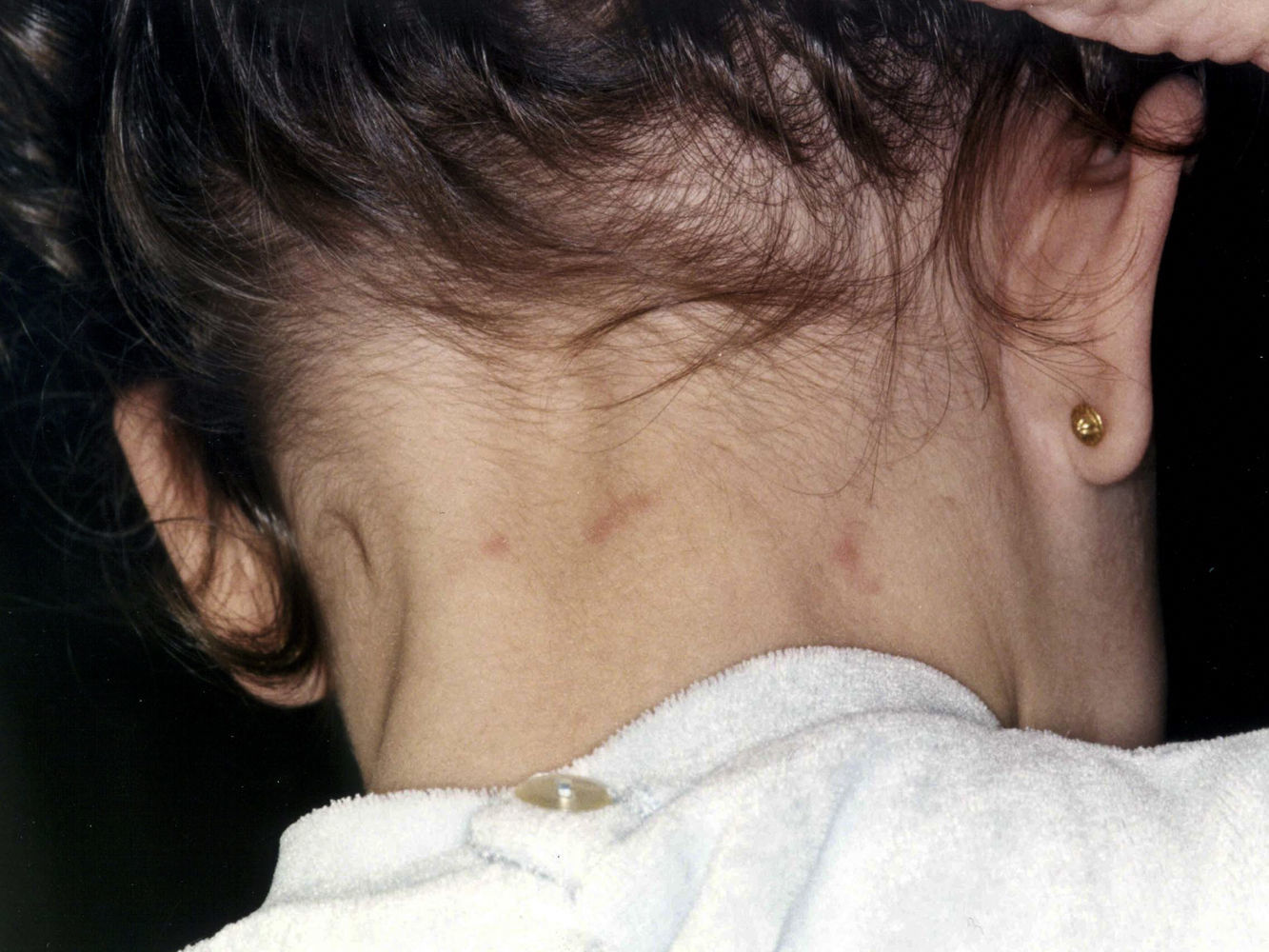
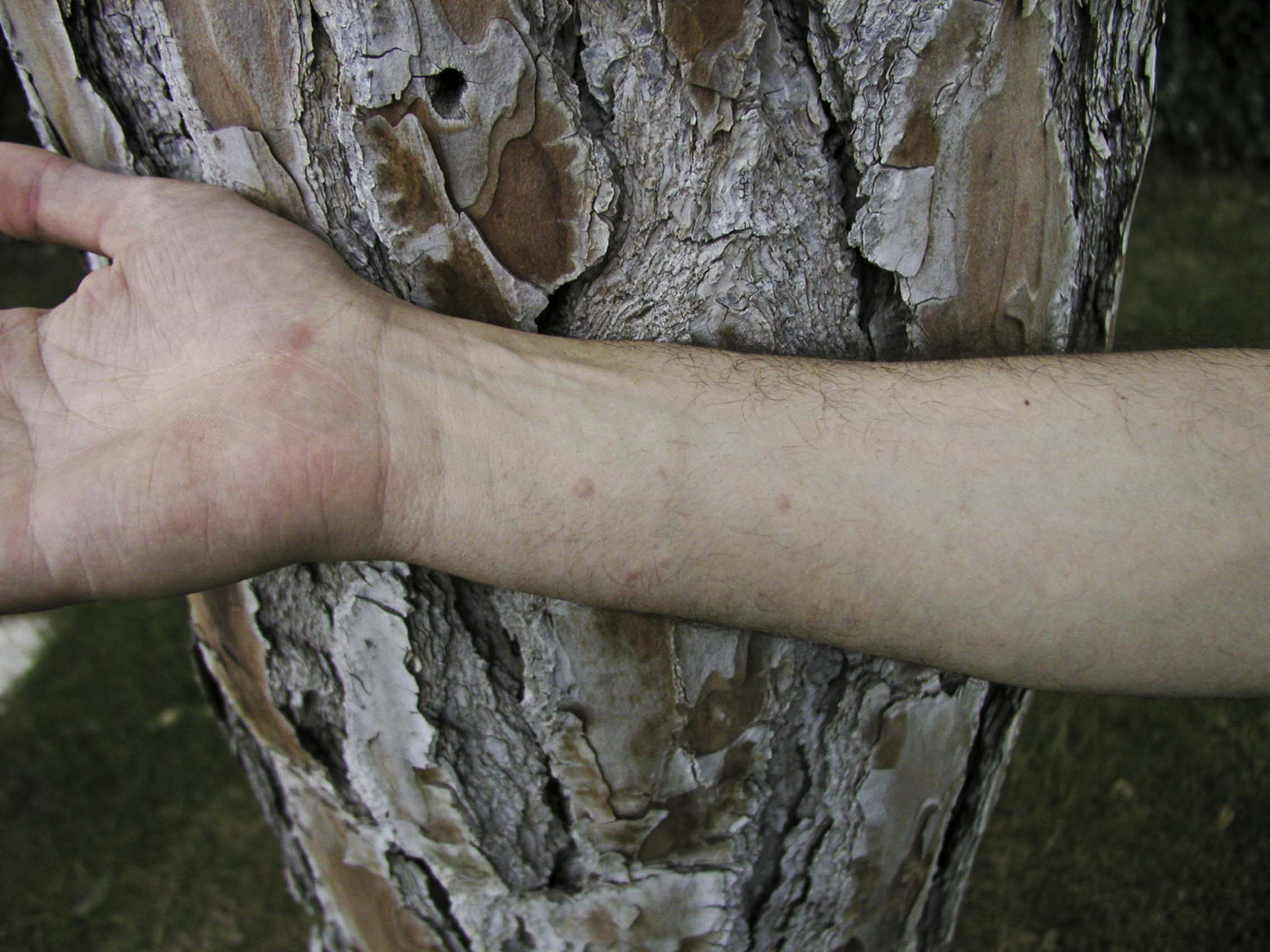
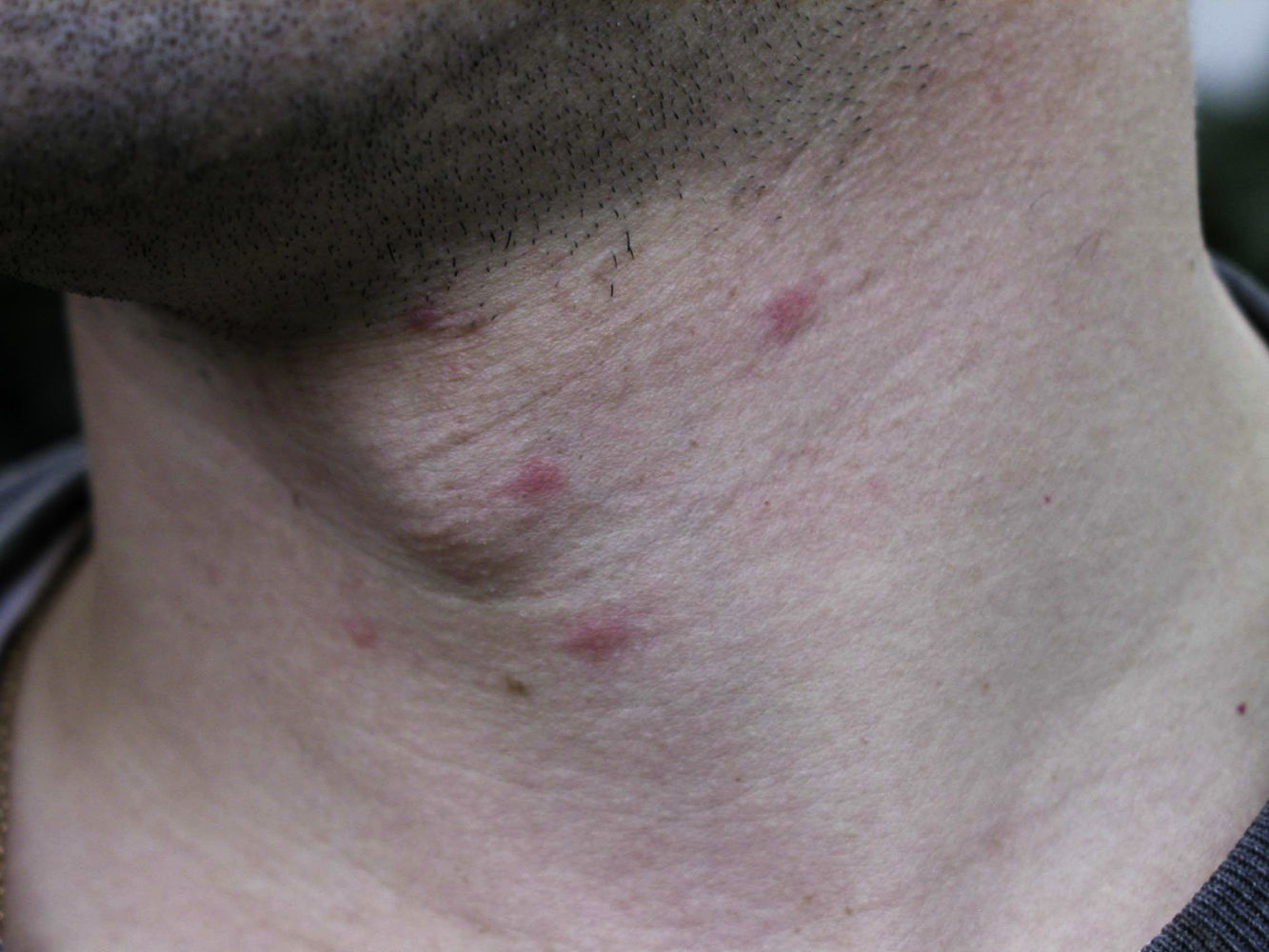
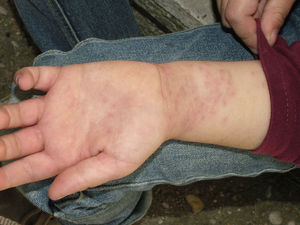
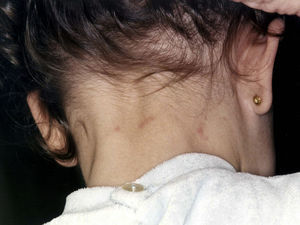
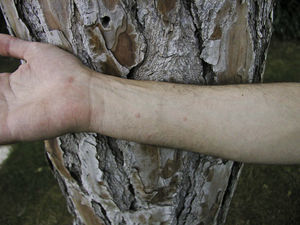
Las lesiones cutáneas se localizan con mayor frecuencia en las zonas expuestas, siendo característica la afectación del cuello y de las extremidades, sobre todo muñecas, antebrazos y tobillos, aunque también es posible la localización en áreas cubiertas. Las palmas de las manos y los espacios interdigitales se afectan con mayor frecuencia en los niños, probablemente por el contacto directo con la oruga al jugar en terrenos infestados15. La actividad física y el rascado son factores que aumentan la intensidad de la dermatosis.
La reacción cutánea a TP puede adoptar diversos patrones. Los más frecuentes son la dermatitis papulosa y la urticaria de contacto. Se han descrito erupciones vesículo-pustulosas y pápulas infiltradas similares a picaduras de insecto de días de duración.
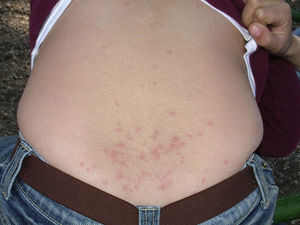
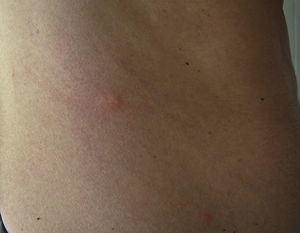
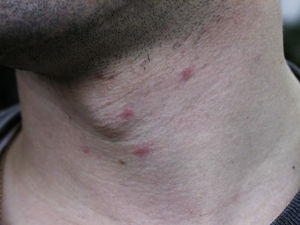
La dermatitis papulosa se caracteriza por la aparición de una erupción papulosa y eritematosa, con mucho prurito y numerosas lesiones de rascado y zonas eccematizadas (figs. 10-13). Estas lesiones suelen aparecer horas después del contacto y persisten durante varios días.
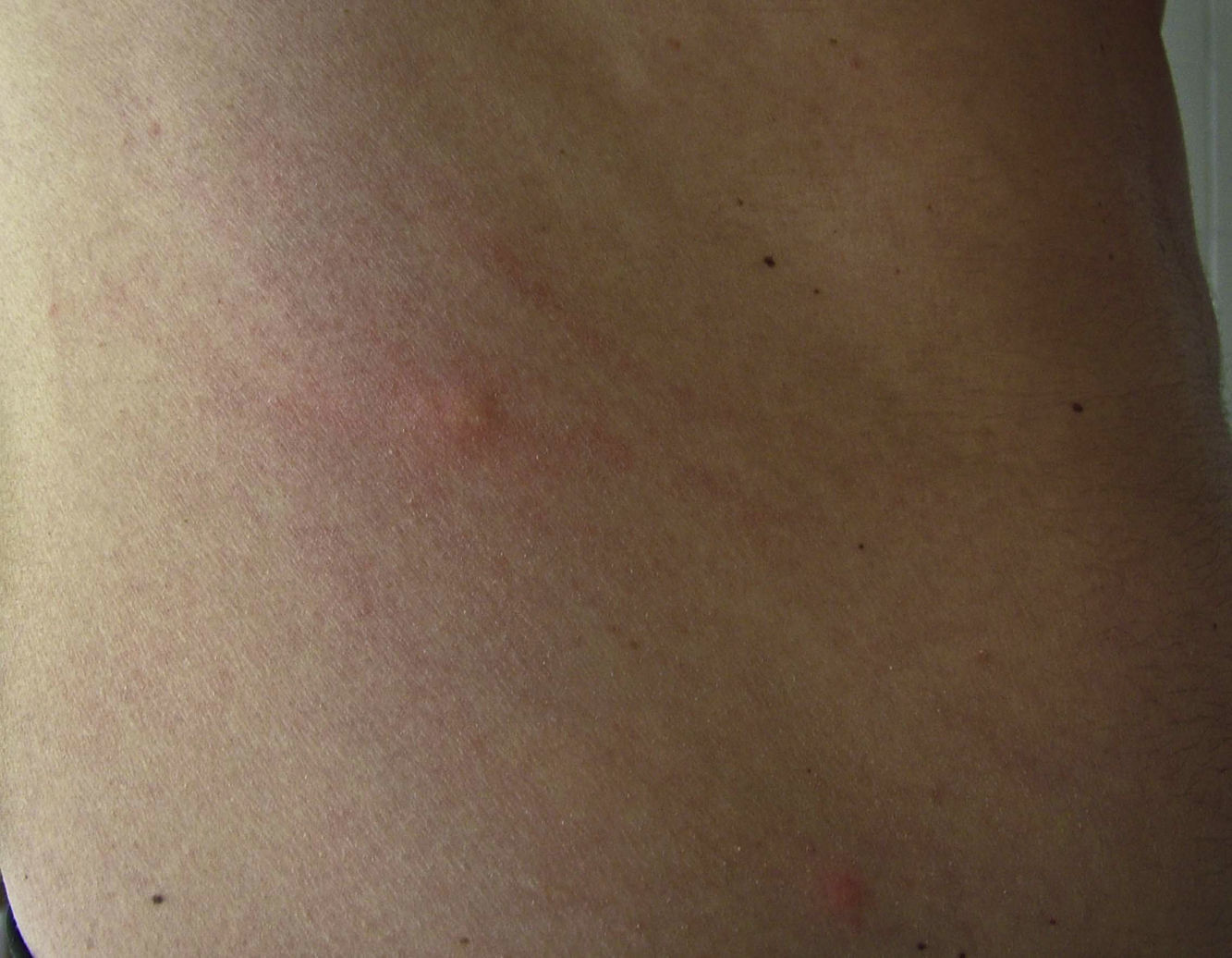
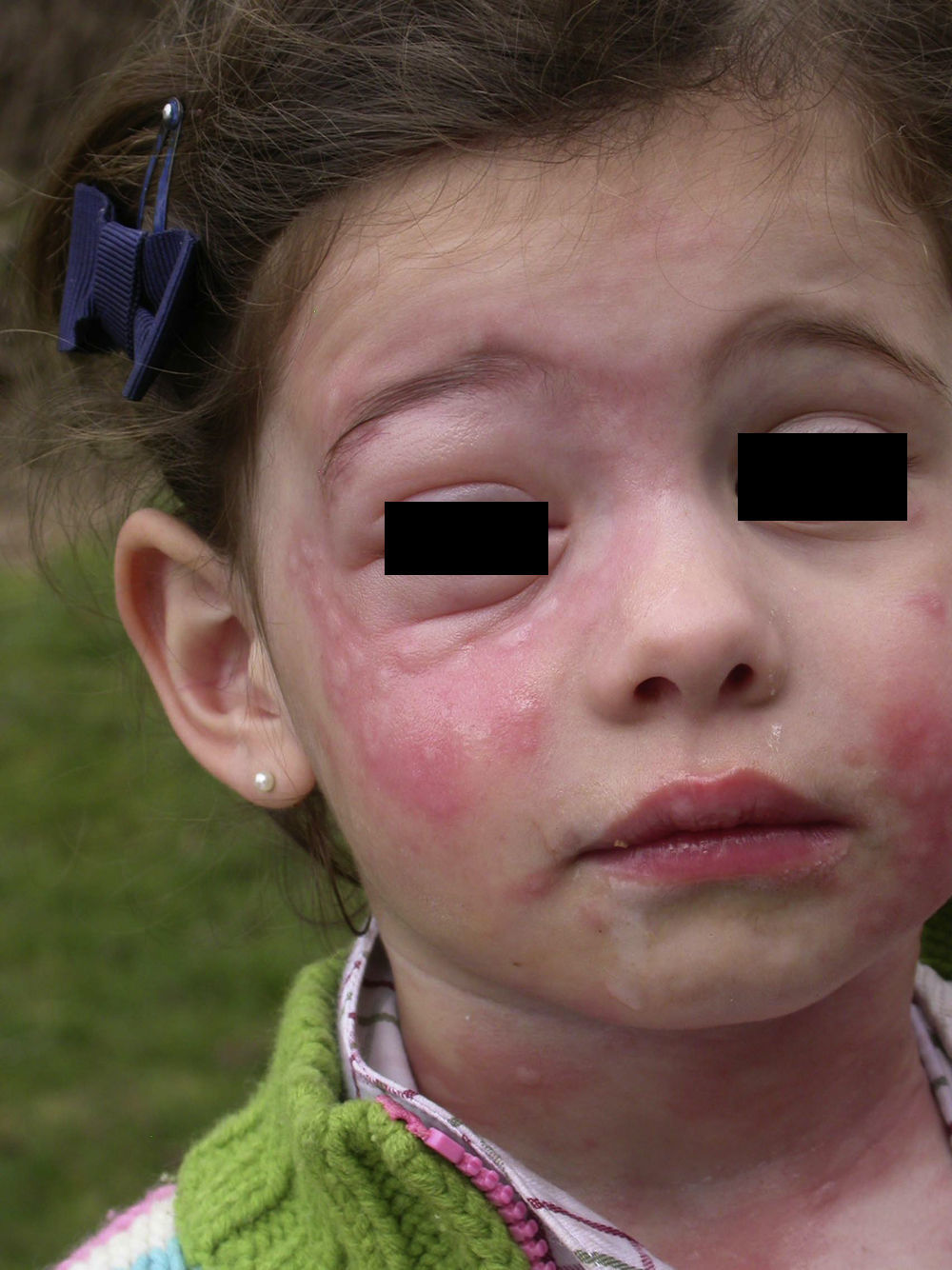
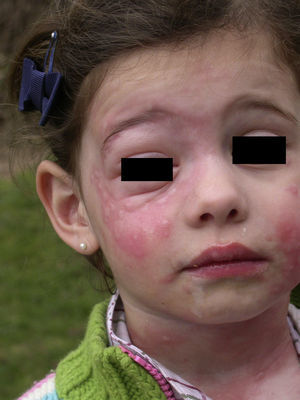
La urticaria de contacto cursa con lesiones habonosas evanescentes de unos minutos o pocas horas de duración frecuentemente asociada a angioedema, sobre todo en párpados (fig. 14)14. Las lesiones urticariformes en ocasiones tienen cierta infiltración, con una morfología de urticaria papulosa, por lo que pueden persistir durante varios días (fig. 15).
Con menor frecuencia pueden observarse lesiones papulovesiculosas e incluso pustulosas, descritas fundamentalmente en las palmas de las manos de niños pequeños16. En general, las lesiones se acompañan de intenso prurito y tienden a desaparecer a los pocos días.
La afectación ocular característica es la conjuntivitis, también agravada por el rascado, que aumenta la penetración y el roce de los pelos urticantes. Se han descrito casos más raros de queratitis y oftalmía nodosa. Poco frecuente es la afectación respiratoria, manifestada sobre todo por disnea, en ocasiones asociada a una reacción anafiláctica con afectación multiorgánica de la que existen varios casos descritos en la literatura12–15,17,20.
En pacientes no alérgicos la manifestación más frecuente consiste en la dermatitis papulosa pruriginosa anteriormente descrita, aunque también es posible la aparición de una urticaria de contacto, en general más localizada. Con menor frecuencia la TP origina una reacción cutánea retardada que puede durar varios días y que se manifiesta en forma de pequeñas pápulas infiltradas, papulovesículas o pústulas (fig. 16).
El patrón clínico de los pacientes alérgicos a TP (con pruebas cutáneas y/o serológicas positivas y con reacción tras la exposición) muestra diferencias significativas con respecto a los no sensibilizados. Se trata de pacientes con reacciones incluso tras mínimas exposiciones (pasear por un pinar sin tener un contacto evidente con las orugas), con clínica inmediata aunque de menor duración y progresivamente más intensa (más casos de urticaria generalizada, angioedema y anafilaxia)12–20.
En los pacientes alérgicos la afectación cutánea característica es la urticaria de contacto acompañada de angioedema en la mitad de los casos. Como en otras urticarias alérgicas de contacto, las lesiones aparecen tras un contacto que puede ser mínimo, poco tiempo después de la exposición a la oruga, en general durante la primera hora, y con frecuencia se extienden a zonas cubiertas del cuerpo e incluso se generalizan. En los alérgicos a TP aparecen con mayor frecuencia síntomas respiratorios, y es donde se han descrito los casos de reacciones anafilácticas. Estas reacciones son más frecuentes y más graves en los profesionales con contacto estrecho y repetido con TP.
DiagnósticoNo hay ningún signo clínico específico de las reacciones por TP. La sospecha diagnóstica de una reacción cutánea por TP se basa en los siguientes datos:
- 1.
Antecedentes de exposición en las 24 horas previas en una zona con pinos infestada con TP en cualquier época del año, si bien son más frecuentes durante los meses de febrero a abril. En trabajadores en contacto con los pinos la exposición está condicionada por el tipo de tareas que realizan. Así, los recolectores de piñas tienen la máxima incidencia de reacciones entre los meses de octubre y diciembre. También hemos observado reacciones en pleno verano en trabajadores que extraen arena de los pinares durante esos meses, en los que no hay orugas urticantes pero sí restos o capullos en la arena.
- 2.
Presencia de una erupción habonosa, con o sin angioedema, o de una dermatitis papulosa, ambas muy pruriginosas y localizadas preferentemente en el cuello y la zona distal de las extremidades. En los niños habrá que buscar las lesiones sobre todo en las palmas y los espacios interdigitales.
- 3.
Identificación, siempre que sea posible, de los pelillos urticantes en la piel o en la ropa del paciente mediante la aplicación de una tira adhesiva (celofán o esparadrapo) o directamente en la piel mediante el empleo de la dermatoscopia. Esta técnica se ha utilizado recientemente en el diagnóstico de diversas infestaciones cutáneas (entodermoscopia) y puede considerarse como una herramienta útil en el diagnóstico diferencial de las erupciones papulosas y eritematosas34,35.
- 4.
Las reacciones no deben aparecer en otras circunstancias, y hay que excluir otros diagnósticos diferenciales que puedan originar un cuadro clínico similar (reacción a picaduras de otros insectos, prurigo nodular o atópico, escabiosis, otros eccemas y urticarias de contacto, etc.).
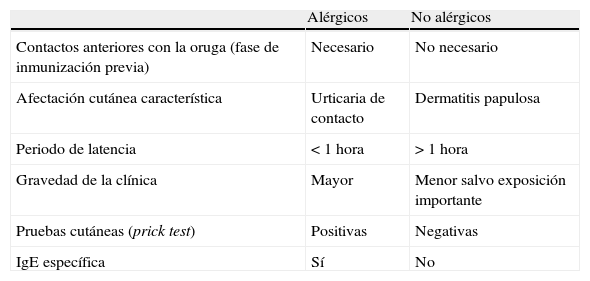
Ya hemos comentado en el apartado anterior los criterios clínicos que sugieren la participación de un mecanismo alérgico mediado por IgE. La confirmación del mismo se hará mediante la positividad de las pruebas cutáneas y/o de la IgE específica en suero frente al extracto de la oruga (tabla 1).
Diferencias entre individuos con reacción por Thaumetopoea pityocampa alérgicos y no alérgicos a este insecto
| Alérgicos | No alérgicos | |
| Contactos anteriores con la oruga (fase de inmunización previa) | Necesario | No necesario |
| Afectación cutánea característica | Urticaria de contacto | Dermatitis papulosa |
| Periodo de latencia | < 1 hora | > 1 hora |
| Gravedad de la clínica | Mayor | Menor salvo exposición importante |
| Pruebas cutáneas (prick test) | Positivas | Negativas |
| IgE específica | Sí | No |
En ciertas zonas este insecto se ha convertido en una verdadera plaga, con la infestación de múltiples árboles e incluso pinares enteros. Se están empleando distintas técnicas para tratar de controlar esta plaga, entre las que se encuentran medidas mecánicas (colocar bandas adhesivas impregnadas de insecticida alrededor de los árboles o destruir directamente los nidos), la fumigación con distintos productos químicos o biológicos, el empleo de feromonas, potenciar el incremento de sus depredadores naturales, etc.7,36.
En la tabla 2 citamos algunas medidas de prevención frente a este insecto. Una vez que aparecen los síntomas el tratamiento es meramente sintomático: antihistamínicos orales para controlar el prurito y los casos de urticaria de contacto y angioedema, y corticoides tópicos para las lesiones eccematosas y de dermatitis papulosa. En casos extensos o rebeldes pueden emplearse corticoides orales. En la medida de lo posible hay que evitar el rascado, porque aumenta la sintomatología al clavar y rozar las espículas de la oruga en la piel o en las mucosas. En las reacciones anafilácticas es preciso un diagnóstico precoz y un tratamiento inmediato con adrenalina además de corticoides y antihistamínicos.
Consejos para evitar reacciones por oruga de la polilla procesionaria del pino, de especial importancia para pacientes alérgicos al insecto
| Durante los meses en los que la oruga desciende en procesiones de los pinos (si el invierno es frío: febrero-abril; si el invierno es más suave: enero-marzo) y especialmente en días de viento, es preferible que no pasee por pinares infestados por procesionaria y que tampoco lo hagan sus mascotas (por ejemplo perros). |
| Si existen procesiones de orugas: alejar a los niños, NUNCA molestarlas, tocarlas ni barrerlas (se levantan miles de dardos urticantes). Si están en su parcela, una vez enterradas puede mojar la zona para fijar los pelillos de las orugas al suelo. |
| Evite recoger objetos (piñas, leña, etc.) de los pinares infestados o tocar los nidos de las orugas. Si vive en una parcela con pinos durante los últimos meses del invierno y en primavera no tienda a secar la ropa al aire libre |
| Evite remover la tierra en pinares o márgenes de los mismos |
| En los casos de exposición profesional deben extremarse las medidas de precaución cuando trabajen en pinares con esta plaga. Es importante que tengan la menor superficie cutánea posible expuesta, usando para ello prendas adecuadas: camisas y pantalones que cubran las extremidades, botas, etc., y si van a realizar tareas en la copa de los pinos usar gafas protectoras e incluso mascarilla. Los pacientes alérgicos a la oruga no deberían trabajar en pinares infestados por ella |
La polilla procesionaria del pino supone una plaga en expansión, sobre todo en los países mediterráneos. Aparte de la deforestación que origina, con el consiguiente perjuicio medioambiental y económico, en su estadio larvario es causa de reacciones patológicas en el hombre, frecuentemente infradiagnosticadas por el dermatólogo.
Los pelos urticantes de esta oruga son capaces de producir diversa patología cutánea, conjuntival, respiratoria e incluso reacciones anafilácticas graves. Aunque se considera una patología de importancia estacional durante los meses de febrero a abril, puede originar síntomas a lo largo de todo el año. El antecedente de la exposición a la oruga en visitantes y residentes de zonas de pinares y, sobre todo en trabajadores relacionados con la explotación del pino, es fundamental para el diagnóstico. Los criterios para sospechar un componente alérgico mediado por IgE incluyen reacciones inmediatas, repetidas y progresivamente más intensas, incluso con una mínima exposición.
Creemos conveniente que el dermatólogo se familiarice con la patología originada por TP, ya que la afectación cutánea es sin duda la más frecuente y en muchas ocasiones la única manifestación clínica. El correcto diagnóstico y la adecuada información que enfatice las medidas preventivas reducirá la incidencia y la gravedad de estas reacciones.
FinanciaciónEste trabajo ha sido financiado en parte por el proyecto URTICLIM de la Agencia Nacional de Investigación Francesa.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.